2 professionals
Coup d'œil du congrès GERDA 2025
Coup d'œil du congrès GERDA 2025
Comptes-rendus par Dr Laure Bellange (Allergologue Lyon) et Lou Faltot (Interne en dermatologie, Service d'Immuno-allergologie, Lyon Sud)

Sujets liés
Compte-rendu par Dr Laure Bellange (Allergologue Lyon)
F. Giordano (Toulouse), N. Raison-Peyron (Montpellier), E. Collet (Dijon)
La lanoline, aussi appelée cire de laine, graisse de laine, ou suife de laine, est obtenue à partir des sécrétions des glandes sébacées du mouton. Cela lui sert à se protéger de l’humidité et de la moisissure. Elle représente 5 à 25% du poids de la laine. On l’utilise depuis l’Antiquité. Les grecs anciens disaient qu’il fallait laver la laine plusieurs fois afin d’en extraire la couche huileuse. La production industrielle date du 19ème siècle, avec un brevet de méthode de centrifugation. Aujourd’hui, on purifie et modifie la graisse pour en obtenir différents produits.
Elle est une bonne base lipophile anhydre, hydratante, avec un pouvoir de ralentissement de la perte d’eau transépidermique. Elle est présente partout, dans les cosmétiques, et les médicaments, mais aussi dans de nombreux usages industriels (agent anti corrosif de certains métaux par exemple).
C’est une substance naturelle, donc sa composition dépend de la zone géographique du mouton, de la race, de la méthode d’extraction etc... La lanoline brune peut être séparée en une forme solide et une forme liquide.
En tant qu’allergène, le premier cas d’eczéma de contact date de 1922. Le premier patch test positif date de 1929. Selon les études, 1,2 à 6,9% des malades avec eczéma de contact ont une allergie à la lanoline. Dans la population générale, cette allergie touche 0,4%. Le risque de sensibilisation est augmenté quand utilisé sur des plaies ou autres zones endommagées de la peau. Les personnes exposées aussi régulièrement dans leur travail sont plus à risque de devenir allergique. En fait, il y a un paradoxe de la lanoline, c’est un allergique faible dans la population générale, mais c’est un allergène fort dans certaines populations exposées. Les médicaments contenant de la lanoline paraissent plus sensibilisants que les cosmétiques en contenant. Et étrangement, les patients qui ne tolèrent pas la lanoline sur des zones de peau lésée, la tolèrent sur leurs zones de peau saine.
Il faut savoir que les patchs tests sont souvent négatifs. Est-ce parce que les ingrédients ajoutés à la lanoline lors de sa transformation sont sensibilisants ? Est-ce parce que la composition de la lanoline n’est pas la même selon les produits ? Est-ce parce qu’on teste en peau saine ?
Il y a aussi des résultats faussement positifs car il est souvent irritatif.
L’allergène est probablement contenu dans les alcools de lanoline.
On peut compléter le test à la lanoline classique, avec un test lanoline+parrafine. Mais certains pensent que ce mélange peut aussi fausser les résultats. Le test idéal n’est donc toujours pas trouvé. Concernant les produits personnels des patients, les ROAT tests sont les plus pertinents.
L’éviction est facile dans les cosmétiques, grâce à la liste INCI. Le nom lanoline sera toujours présent. Pour les médicaments, c’est plus compliqué car les dénominations sont diverses. A l’heure actuelle, il y a 37 spécialités en contenant.
Compte-rendu par Dr Laure Bellange (Allergologue Lyon)
C. Lafforgue (Chatenay-Malabry), M. Avenel-Audran (Angers), A. Barbaud (Paris), M.-C. Houle (Québec, Canada)
Beaucoup de cosmétiques impactent l’environnement. L’idée aujourd’hui est d’obtenir des produits les plus écologiques possibles. On sait que les produits capillaires par exemple, ne sont pas bons pour les animaux marins. Des études ont comparé les eaux qui sortent des salons de coiffure des autres eaux, et les espèces marines meurent plus dans l’eau issue des salons de coiffure. Le problème c’est que le constat est fait après commercialisation des produits. Comme on ne teste pas sur les animaux, on constate in fine qu’ils sont néfastes pour eux, mais on ne peut pas le prévoir avant. Concernant les filtres solaires, on a beaucoup dit qu’ils étaient responsables du blanchiment des coraux. C’est exact, mais ce ne sont pas les seuls responsables. Le réchauffement climatique est aussi en cause. On ne sait pas si ce sont les filtres minéraux ou organiques qui sont le plus responsables. Certains ont été arrêtés par précaution, d’autant plus qu’ils sont perturbateurs endocriniens. Par contre, le problème est mondial. Les normes européennes ne sont pas les mêmes que les normes américaines ou asiatiques. Là-bas, on utilise encore des vieux filtres écotoxiques. En Europe, l’idée est d’avoir de plus en plus de filtres biodégradables. Mais que faut-il mieux ? Biodégradable ou durable ? Biodégradable veut dire que ça se décompose, mais il reste des éléments. Durable veut dire que c’est capable d’être maintenu à un niveau stable sans endommager la nature. En cosmétique, afin de limiter l’impact environnemental, il y a des publicités « zéro déchet ». Cela revient à « zéro emballage ». Il y a l’idée des recharges de réutilisation. La mise en place est plus ou moins simple pour des raisons de norme. Dans les ingrédients purs et durs, on pourrait penser que les ingrédients naturels sont les meilleurs pour l’environnement. Mais ils ne sont pas toujours renouvelables ni durables. Par exemple, l’huile d’argan est naturelle et pleine de vertus, mais elle vient d’une toute petite zone dans un seul pays, donc ce n’est pas renouvelable. Idem pour l’encens. La biotech est la technique utilisée en cosmétique pour faire du durable et renouvelable. Les microalgues sont utilisées dans la « blue cosmetic ». Leur intérêt c’est qu’elles consomment du CO2 et libèrent de l’énergie. La fermentation est aussi à la mode. Cela donne des substances actives et des micro-organismes.
Le problème, c’est que même si les industries font des efforts pour améliorer les produits, les tendances vont à l’encontre de l’écologie et il y a un grand rôle à jouer du côté des consommateurs. Par exemple, c’est la mode de la skin care coréenne. Elle se déroule en huit étapes. Il faut donc mettre huit produits différents sur la peau. Cela est énorme et coûteux en énergie et matières premières, donc pas écologique. La nouvelle tendance de la skin care nordique parait plus appropriée car elle n’a que trois étapes, et elle prend en compte l’environnement et la naturalité. Là on ira peut-être vers une cosmétique plus propre. Il y a aussi le skinimalisme qui veut associer les soins durables, avec des ingrédients multifonctionnels. On obtient des formules courtes et très efficaces.
Compte-rendu par Dr Laure Bellange (Allergologue Lyon)
M.-T. Le Cam (Créteil), M.-N. Crepy (Paris), P. Marcant (Lille)
Les plantes et les bois sont responsables de dermatose professionnelle. Les cas sont fréquents et sous-estimés, avec de nombreuses professions exposées. Il y a des milliers de plantes, mais finalement, peu posent problème.
Il y a différents tableaux cliniques.
Il y a en premier des dermites irritatives de contact, comme avec les cactus et ses épines, ou les jonquilles et ses cristaux d’oxalate de calcium, ou les euphorbes.
Il y a aussi bien sûr la dermatite allergique de contact. On peut les classer par familles d’allergènes. La première famille est le noyau alpha methylène-y-butyrolactone (lactones sesquiterpéniques). Les principales plantes présentant cet allergène font partie de la famille des asteracées (arnica) mais on le retrouve aussi dans les jubulaceae, les magnolias, les lauriers, les alstroemeriaceae (cette plante est fréquemment manipulée par les fleuristes car rentre dans de nombreuses compositions de bouquets), les tulipes hollandaises. Les aspects peuvent être extrêmement sévères avec des atteintes des mains et du visage. Il y a des aspects kératiformes. La deuxième famille est les quinones. On les retrouve dans les primevères.
Aujourd’hui, par génie génétique on a pu faire des plantes sans allergène. On le retrouve aussi dans les bois tropicaux dont le pao ferro (charpentiers, ébénistes, instrumentistes). L’éruption peut être érythème polymorphe like. Les instrumentistes à vent peuvent déclencher de fortes chéilites. Une troisième famille est représentée par les phénols. On retrouve peu ces plantes dans nos contrées, plutôt en Amérique. L’eczéma est souvent bulleux. Il y a aussi des cas très sévères avec des laques japonaises. D’autres allergènes non classés dans ces trois familles peuvent se rencontrer. L’ail contient notamment du diallyl disulphite, responsable de pulpite. Le lierre grimpant est aussi allergisant, avec le falcarinol. Chez les jardiniers, on retrouve un aspect linéaire comme on retrouve sur l’implantation de la plante.
Un autre tableau clinique est représenté par les photodermatoses, mais il s’agit surtout de phototoxicité. Les barmans avec le citron vert sont souvent touchés.
Un dernier tableau clinique est celui des urticaires de contact ou dermite de contact aux protéines. On connait tous la réaction aux orties. Le latex est aussi bien connu, mais l’épidémie est terminée à ce jour. Dans les saunas, les bois utilisés peuvent aussi être en cause. Récemment, un cas a été décrit avec de la laitue rouge.
Afin de faire le diagnostic, certains de ces allergènes sont dans la batterie standard européenne ou la batterie plante, notamment les lactones. Pour le bois, on peut tester les sciures diluées. Pour tester les plantes, on ne peut pas toutes les tester. Il faut être sûr de la famille botanique et de l’absence de toxicité.
Comment prévenir les cas d’allergie, surtout chez les professionnels ? Selon les métiers, on peut utiliser des protections mécaniques, mais parfois cela est difficile comme pour les musiciens. Il y a quelques cas de traitements systémiques chez des allergiques au lactone, même si l’éviction est à préférer.
Compte-rendu par Dr Laure Bellange (Allergologue Lyon)
D. Pin (Lyon)
Comme nous, les animaux peuvent déclencher des allergies. Heureusement, ils ne sont pas allergiques à l’Homme.
Concernant les allergies respiratoires, l’asthme a été décrit chez le chat et le cheval. Chez ce dernier, cela a été assez bien étudié, et les stades sont globalement similaires à ceux de l’Homme. Le chien a une structure bronchique qui ne permet pas d’asthme.
Concernant les allergies alimentaires, il faut plutôt parler d’intolérance. L’allergie est rarement prouvée. Les mécanismes sont les mêmes chez le chien et la souris. Il peut y avoir des syndromes oraux, mais aussi de l’anaphylaxie. Il y a eu quelques cas décrits chez le chien, notamment un cas d’allergie aux arachides, et un autre d’allergie aux acariens contenus dans les croquettes. Il existe aussi des oesophagites oesinophiliques chez le chat et le chien, et des gastro-entérites lymphocytaires.
Concernant les allergies cutanées, les allergies les plus fréquentes sont les dermatites par allergie aux piqûres d’insectes, notamment les puces. Chez le chat, c’est pléiomorphe. Chez le chien, les symptômes sont beaucoup plus typiques avec des lésions cutanées sur le dos et du prurit. En théorie c’est saisonnier, mais en pratique pour les animaux domestiques c’est per annuel. Il faut traiter les animaux avec des corticoïdes, mais il faut aussi traiter les autres animaux autour avec des répulsifs. Pour le cheval, l’allergie aux insectes la plus fréquente est due aux culicoïdes. C’est une symptomatologie saisonnière, qui s’aggrave d’année en année. On peut faire le diagnostic par dosage d’IgE. Le traitement est le « zéro piqure » donc répulsifs, vêtements protecteurs, limitation des zones infestées.
Les animaux peuvent aussi faire de l’urticaire. Quand elle est aigue, la cause est souvent médicamenteuse. Comme chez l’Homme, l’urticaire peut se chroniciser, non allergique aussi. Le traitement sera les antihistaminiques au long cours.
L’eczéma chez le chien est aussi très fréquent. Quand on explore, dans un tiers des cas, on ne trouve rien. On peut donc penser que c’est intrinsèque comme la dermatite atopique de l’Homme. Il y a des facteurs génétiques en cause, car certaines races et certaines lignées sont plus atteintes que d’autres. Il n’y a pas de prédisposition de sexe. L’évolution se fait par poussées au début, puis saisonnier et per annuel. Dans la recherche, toute la physiopathologie immunologique du chien est comparable à celle de l’Homme. Le traitement se compose des dermocorticoïdes, mais aussi les traitements systémiques. On peut faire de l’immunothérapie, des corticoïdes, de la ciclosporine, du méthotrexate, des JAKinb. Dans le futur, on aimerait pouvoir le traiter par vaccination anti-cytokine. Le chien est la seule espèce animale à faire une dermatite atopique spontanée.
Compte-rendu par Dr Laure Bellange (Allergologue Lyon)
A. Goossens (Leuven, Belgique)
Dix articles ont été présentés en une minute chacun, avec un point clé à retenir. Voici les messages importants de la session :
Vitamine K1 oxydée : elle a remplacé la vitamine K1, interdite en 2009 en cosmétique. Mais plusieurs cas d’allergie ont été décrits. Il y a une épidémie croissante en Espagne, où 37 cas ont été publiés depuis 2017, dont un cas induit par le soleil. Il y a un risque avec les dérivés de la vitamine K, et du coup contre-indication au traitement systémique. Les tests sont souvent négatifs, y compris avec les préparations amenées par les patients.
Concernant les produits dépigmentants, les dérivés de la vitamine C sont de plus en plus utilisés. Plusieurs cas graves ont été signalés à l’ANSES en 2024. Il n’y a pas de réaction croisée démontrée entre ces dérivés.
Le Tinosorb est un filtre uv photostable à large spectre, autorisé en Europe depuis 2022. Il est souvent combiné à des écrans solaires classiques, et stabilise d’autres filtres UV. 3 cas de dermatite de contact ont été rapportés en France, et un cas a été déclaré à l’ANSES. Il est nouveau, mais semble quand même moins sensibilisant que d’autres filtres solaires.
Les allergies aux teintures capillaires naturelles sont peu connues en Europe. Il y a deux cas décrits aux US et en Australie, 1 cas en Indonésie, et 3 cas de dermatite de contact en France. Dans un contexte professionnel, des cas d’asthme et de rhinite ont été rapportés. L’indigo naturel est l’allergène le plus fréquent.
On note une épidémie mondiale d’allergie aux cosmétiques pour ongles. HEMA a causé des réactions pustuleuses du visage et des mains. Il y a des réactions croisées avec le diméthacrylate d’éthyleneglyol. Maintenant, il faut un étiquetage « réservé à un usage professionnel. Peut provoquer une réaction allergique ». Mais peu tiennent compte de cet étiquetage. Cela nécessite une législation plus stricte, comme pour les acrylates et isocyanates. Des cas d’angio-oedèmes des lèvres et des paupières ont été décrites.
Un cas d’urticaire, évoluant vers une dermatite de contact et oedème facial sévère a été décrit avec de l’huile de graine de citrouille. C’est une dermite de contact aux protéines. C’est un phénomène rare pour les cosmétiques. Il y a quelques cas rapportés par inhalation.
Compte-rendu par Dr Laure Bellange (Allergologue Lyon)
C. Lafforgue (Chatenay-Malabry), M. Baeck (Bruxelles, Belgique), M. Braire-Bourrel (Lyon), F. Hacard (Lyon), F. Berard (Lyon), I. Boccon-Gibod (Grenoble)
Il est intéressant de s’intéresser aux perturbateurs endocriniens (PE) car c’est un enjeu croissant de santé publique, un sujet d’intérêt majeur dans le débat public, avec une exposition omniprésente dans notre vie quotidienne. Il y a des impacts cliniques documentés. Les médecins ont un rôle important à jouer pour prévenir les patients.
Un perturbateur endocrinien est une substance naturelle ou synthétique interférant avec le système endocrinien. L’OMS les définit comme altérant une ou plusieurs fonctions endocriniennes avec des effets délétères sur la santé. Ils agissent de plusieurs façons : mimétisme hormonal, antagonisme hormonal, modulation enzymatique, et perturbation du transport ou de la clearance hormonale. Il y a des périodes de vulnérabilité comme la grossesse, la période néonatale, l’enfance et la puberté. Doit-on réellement s’inquiéter ? Il y a une complexité d’analyse des données scientifiques, avec de nombreux biais. C’est aussi un sujet controversé et parfois polarisant, à l’interface entre science, opinion publique et battement médiatique.
Sur la libido, ils entrainent chez l’homme une diminution de la concentration et de la morphologie des spermatozoïdes, des anomalies congénitales, et un hypogonadisme fonctionnel. Chez la femme, ils entrainent une baisse de la réserve ovarienne, et des troubles du cycles.
Concernant le métabolisme, certains PE sont obésogènes. Ils modifient aussi le fonctionnement de la thyroïde.
Pendant la grossesse, le cerveau est en développement et les PE peuvent entrainer des TDAH et TSA, des troubles cognitifs, des perturbations du fonctionnement autonome.
Il y a aussi un risque de cancer, avec modification de l’expression des gênes et stress oxydatifs.
Les sources de ces PE sont multiples et permanentes dans notre quotidien. Avec les cosmétiques, les gros soucis concernent les filtres solaires, et les produits naturels (phyto-oestrogènes de soja).
Le principe de précaution nous fera plutôt limiter les plastiques, utiliser des cosmétiques « PE-free », utiliser des produits ménagers simples, manger une alimentation bio, bien aérer nos intérieurs. Il faut quand même garder une attitude rationnelle et raisonnée.
Concernant les cosmétiques, il faut bien s’assurer qu’on utilise des produits conformes à la réglementation européenne, notamment sur les produits vendus sur internet. Il faut aussi faire attention à l’exposition à la chaleur et au soleil qui modifient la composition des produits, et les interactions entre les ingrédients et le contenant.
Les dernières actualités montrent qu’il y a une propagation transgénérationnelle des effets. Il y aurait peut-être un lien génétique. Il y a plusieurs modélisations pour essayer de quantifier l’exposition cumulative. Il y a une modification de la législation sur certains produits cosmétiques et alimentaires pour interdire les bisphénols, PFAS. Il reste encore beaucoup de choses à découvrir et à modifier au niveau de la législation et de notre mode de vie.
Compte-rendu par Lou Faltot (Interne en dermatologie, Service d'Immuno-allergologie, Lyon Sud)
I - Best-of des 10 articles récents de recherche dans la dermato-allergologie – Audrey Nosbaum
1. Gribonika. Nature 2025 - Organes lymphoïdes tertiaires (OLT) : aussi dans la peau
La peau contient des organes lymphoïdes tertiaires qui après contact avec Staphylococcus epidermidis, produisant des anticorps IgG spécifiques pour contrôler le microbiote local.
La peau est un organe lymphoïde autonome redéfini comme une barrière et un compartiment immunologique complet.
Implication majeure pour la physiopathologie, la vaccination transcutanée, les traitements ciblants les OLT cutanée.
2. Liu et al. Science 2025 - Se gratter protège… tout en activant l’inflammation cutanée
Le grattage dans l’eczéma active une boucle neuro-immunitaire bénéfique, intégrant des réponses innées et adaptatives via les neurones MRGPRA3 et TRPV1
Prurit et grattage aggrave les eczémas mais pourraient également avoir un rôle bénéfiqueGrattage = évolution bénéfique intégrant les réponses innées et adaptative via l’axe neuro-immun
3. Manurung et al. Science advances 2025 - Immunité : les villes et les champs ne se ressemblent pas
Analyse multi-omique approfondie du profil immunitaire le long d’un gradient rural/urbain comparant les populations sénégalaises et néerlandaises
Dans la population rurale augmentation des cellules NK productrices d’interférons et métabolisme orienté vers la glycolyse.
L’inflammation systémique est accrue en milieu rural, il est important de considérer les conditions environnementales pour interpréter la réponse immunitaire.
4. Mara-buch et al. Nature 2025 - Effet inhibiteur de l’IL4 sur la formation des TRM (lymphocytes T résidents mémoires) CD8+ cutanés
Il y a une inflammation de type 2 dans la dermatite atopique avec une augmentation de l’IL4. Il y a par ailleurs une susceptibilité accrue aux infections virales. Il y a un rôle clé des lymphocytes T résidents mémoire (TRM) CD8+ dans la défense cutanée.
L’IL4 inhibe la formation des CD8+ TRM via un blocage de la voie du TGF béta.
L’IL4 altère la mémoire antivirale cutanée. Par ailleurs le blocage de l’IL-4R par le dupilumab pourrait être une stratégie potentielle pour restaurer les TRM CD8+ et l’immunité antivirale cutanée
5. BRAUN C. JACI 2024 - TRM spécifiques de S. AUREUS dans la DA : des agents doubles
Modèle murin sans barrière cutanée altérée
Les TRM entraînent une diminution de la colonisation bactérienne (protection) mais une augmentation des rechutes inflammatoires.
Cela suggère que moduler sélectivement ces TRM pourrait diminuer les rechutes sans affaiblir la défense microbienne, cette double fonction des TRM ouvre une voie pour des stratégies thérapeutiques ciblées.
6.Waizman DA Sci immunol 2025 - Inflammation cutanée peut provoquer une allergie alimentaire à distance
Il existe un lien mécanistique entre la dermatite atopique et les allergies alimentaires car l’inflammation cutanée détourne la tolérance orale vers une sensibilisation allergique.
Une hypothèse innovante démontre que l’inflammation cutanée peut sensibiliser à des antigènes alimentaires à distance via la diffusion de cytokines alarmines comme IL33, modifiant la tolérance orale
Les perspectives sont des cibles thérapeutiques ou vaccinales via le contrôle des alarmines.
7.Seremet et al. Nature communication 2024
264 biopsies → analyse transcriptomique → identification de 7 modules immunologiques
Chaque pathologie à une signature immunitaire dominante ce qui permet un diagnostic de précision (meilleure classification des dermatoses), une orientation thérapeutique ciblée (choix des biothérapies selon le module dominant), et un outil décisionnel robuste (stable dans le temps).
8.Fukushima et al. Nature 2025 - Signatures transcriptomiques et biomarqueurs de réponse dans la DA
L’analyse de 951 biopsies de peau de 1mm avant et/ou en cours de traitement a permis l’identification de 29 ensembles de gènes.
Association des types 2 et 17 avec les lésions d’érythème et d’induration, du type 1 avec les formes chroniques de DA.
Ils ont découvert que les mauvais répondeurs gardent une signature inflammatoire de type 17, liée à une résistance au traitement.
Cette compréhension des profils moléculaires complexes aide à adapter les stratégies thérapeutiques.
Le travail éclaire les mécanismes sous-jacents de la dermatite atopique et ses variations cliniques.
9.Quaade et al. J allergy 2025 - Eczéma chronique des mains (ECM) : un profil immunitaire commun à tous les patients
L’objectif était de caractériser les profils moléculaires des ECM selon les sous-types (allergique, irritant et atopique).
L’IL1-béta a été identifiée comme molécule inflammatoire majeure transversale.
L’étude a retrouvé un endotype commun suggérant des cibles thérapeutiques universelles (IL4, IL-1bétat, JAK/STAT).
10.Nodrmann et al. Nature 2024 – Inhibiteurs de janus kinase dans la NET
La voie JAK/SYAT est le moteur central de l’inflammation et de la cytotoxicité dans le TEN. Cette voie pourrait être une cible thérapeutique clé.
Compte-rendu par Lou Faltot (Interne en dermatologie, Service d'Immuno-allergologie, Lyon Sud)
Aurélie Du Thanh
1.Pyatilova P. JACI 2024
Etude de registre international de 2521 patients qui montre que 31% des patients ont un symptômes extra-cutané. Cela est corrélé avec la sévérité, les angiooedèmes, le syndrome inflammatoire biologique et la réponse au traitement.
2.Kolkhir P. Mortality in adult patient with UCS JACI 2025
Etude de registre 270 000 patients montrant une mortalité accrue à 3 mois, 1 an, 5 ans surtout pour les jeunes et un phototype clair. Cela met en évidence le risque psychiatrique et la nécessité d’investiguer les comorbidités psychiatriques.
3.Pereira AS. Contact dermatitis 2023
ll s’agit d’un cas clinique décrivant une fixed drug eruption (FDE) due à la cétirizine.
Les auteurs documentent une réaction croisée avec la lévocétirizine et l’hydroxyzine (mêmes familles chimiques/structures apparentées)
4.Soria A. Paradoxical urticaria to h1-antihistamines JEADV 2025
Au moins à 2 classes différentes et plus de 5h après la prise. Les tests cutanés sont négatifs et le test de provocation oral positif en dehors d’une crise d’urticaire spontanée ou d’une anaphylaxie.
5.Sanchez J. Prognostic Calculator of the Clinical Response to Antihistamines in Chronic Spontaneous Urticaria. JACI pract 2025
Cet article présente un outil de calcul du pronostic clinique pour évaluer la réponse aux antihistaminiques chez les patients souffrant d'urticaires chroniques spontanées (UCS). Les auteurs ont développé un calculateur basé sur des facteurs cliniques afin d'identifier les patients susceptibles de répondre positivement au traitement antihistaminique.
6.Ye YM. Distinct cytokines profiles in UCS refractory anti-H1 histamine compary to healthy controls. Clin exp allergi 2025
Qui sont les patients réfractaires aux antiH1 ? Cette étude met en évidence une activation accrue d’IL-17A et IL-4. Les résultats suggèrent que ces altérations immunologiques pourraient contribuer à la persistance des symptômes malgré un traitement antihistaminique standard.
7.Zhang DG JEADV 2025
Etude sur l’optimisation de l’OMALIZUMAB, rétrospective et monocentrique.
Une réponse rapide et un UCT élevé permettent une réduction de dose
8.Ceravalls J. actas dermo-sifiliograficas 2025
Quand arrêter l’OMALIZUMAB ? Cette étude rétrospective suggère qu’il faut être en réponse complète pendant au moins 12 mois sous 300/4sem avant d’arrêter progressivement sur 18mois.
9.Dan Y. JACI 2025 – MRGPRX2 et urticaire chronique
Si présence du variant N62S, non réponse aux AH1et sévérité plus importante. N62S associé à une activation des mastocytes.
10.Riddler SA. High Frequency of Chronic Urticaria Following an Investigational HIV-1 BG505 MD39.3 Trimer mRNA Vaccine in a Phase 1, Randomized, Open-Label Clinical Trial (HVTN 302) Ann Intern Med 2025
Vaccins VIH avec ARNm associés à de l’urticaire. Il va falloir développer ses stratégies visant à atténuer ces effets indésirables dans les futurs essais de vaccins à base d'ARNm contre le VIH-1
Compte-rendu par Lou Faltot (Interne en dermatologie, Service d'Immuno-allergologie, Lyon Sud)
Pauline Pralong
1.
Stephan Weidinger JACI 2025
Essai randomisé de phase 2b d’un antiOX40, l’ AMLITELIMAB
Résumé : l’essai a évalué l’efficacité et la tolérance de Amlitelimab (un anticorps anti-OX40L) chez des adultes atteints de dermatite atopique modérée à sévère sur 52 semaines. Résultat : amélioration significative des scores EASI vs placebo, tolérance acceptable.
2.
Muller Allergy 2024
Traitements récents de la dermatite atopique, incluant les anticorps monoclonaux (dupilumab, tralokinumab, lebrikizumab) et les inhibiteurs de JAK (upadacitinib, abrocitinib). Il décrit les mécanismes d’action, l’efficacité clinique et les profils de tolérance de ces nouvelles thérapies. Enfin, il souligne les perspectives futures : traitements ciblant OX40L, IL-33 et TSLP, prometteurs pour des formes plus sévères.
3.
Fyhrquist JACI 2025
Différents endotypes moléculaires de la dermatite atopique, fondés sur des profils immunologiques et transcriptomiques distincts.
Plusieurs sous-types dominés par les voies Th2, Th17 et Th22, expliquant les variations cliniques et thérapeutiques entre patients. Les auteurs soulignent l’importance d’une médecine personnalisée pour optimiser le choix des biothérapies ciblées.
4.
Beyrouti JACI 2025
Les symptômes oculaires et manifestations tête et cou du traitement par DUPILUMAB sont mieux améliorés par un relais par JAKi que par un relais par TRALOKINUMAB.
5.
Strizzolo WAO Journal 2024
Prise en charge en vie réelle des patients atteints de dermatite atopique ne répondant pas au dupilumab.Les stratégies alternatives, incluant augmentation de dose ou association avec CsA, MTX ou itraconazole, ont permis une amélioration chez 69 % des patients après 3 mois.Cependant, les patients sans réponse initiale n’ont jamais atteint de réponse complète.
6.
Réseau français GREAT / Société Française de Dermatologie JEADV
Efficacité et tolérance du DUPILUMAB chez les patients obèses → efficace dans cette population. Il y a quand même une tendance à moindre efficacité et à un gain de poids (non significatif).
7.
Guillemin C. JAAD 2025
Dupilumab efficace chez les patients avec déficits immunitaires avec un bon profil de tolérance.
8.
R. Ardern-Jones BJD 2024
Consensus multidisciplinaire (dermatologues & ophtalmologues) pour la gestion des troubles de la surface oculaire liés à Dupilumab chez les patients atteints de DA.
9.
Albert F. Yang JAMA dermato 2025
Capteur portable avec IA pour réduire le grattage nocturne chez des adultes atteints de dermatite atopique légère. Il a diminué de 28 % le nombre d’épisodes et de 50 % la durée moyenne de grattage, sans affecter le sommeil. Cela suggère outil non pharmacologique prometteur en complément des traitements classiques.
10.
Wang Allergy 2024
Revue de la littérature évaluant l’impact des changements climatiques sur la DA. Les dangers climatiques (réchauffement, pollution, feux de forêt, sécheresses) sont majoritairement associés à une aggravation des symptômes par des mécanismes directs (augmentation sueur, alétartion barrière, alétartion système immunitaire, contamination eau) ou indirects.
Compte-rendu par Lou Faltot (Interne en dermatologie, Service d'Immuno-allergologie, Lyon Sud)
I. Les hypersensibilités retardées médicamenteuses atypiques – Angèle Soria
Syndrome DRESS et ses variantes cliniques
Le syndrome DRESS présente une variabilité clinique importante, avec des formes sans atteinte cutanée et des délais d’apparition parfois courts, ce qui complique son diagnostic.
• Une méta-analyse de 172 patients a montré que 5 patients n’avaient pas d’atteinte cutanée, soulignant que celle-ci n’est pas toujours présente.
• Les formes cliniques identifiées par une équipe anglaise chez 27 patients incluent des lésions en pseudo-cocardes, associées à des atteintes hépatiques plus sévères.
• Elle a insisté sur le fait que même un délai de moins de 15 jours après le traitement peut correspondre à un DRESS, souvent lié à des antibiotiques ou produits de contraste, tandis que des délais plus longs impliquent des médicaments comme la carbamazépine. DRESS chez les patients avec une maladie de Still Le DRESS associé à la maladie de Still présente des particularités graves, notamment un syndrome d’activation macrophagique et des atteintes pulmonaires, justifiant une recherche HLA spécifique.
• Ces patients portent fréquemment l’allèle *HLA-DRB15*, qui oriente les investigations génétiques.
• L’utilisation d’inhibiteurs d’IL1 et d’IL6 dans ce contexte est fréquente, ils peuvent déclencher des formes sévères de DRESS. PEAG et IL-36 La PEAG partage une signature génétique proche du psoriasis pustuleux, ouvrant la voie à l’utilisation d’anticorps ciblant l’interleukine 36, une avancée potentielle en traitement.
• Une analyse transcriptomique de 13 000 gènes a révélé une expression quasi identique entre PEAG et psoriasis pustuleux induit par médicaments, avec seulement 2 gènes différant significativement.
• L’implication de l’IL-36 est centrale, justifiant l’essai d’anticorps anti-IL36 comme le spézolimab dans les formes sévères.
Hypotensions et troubles hémodynamiques dans les toxidermies sévères
Les troubles hémodynamiques, bien que rares, surviennent dans plusieurs toxidermies sévères, notamment le DRESS et la PEAG, nécessitant une prise en charge urgente et adaptée.
• Une étude anglaise sur 125 patients PEAG a montré que 22 avaient une instabilité hémodynamique, dont certains en état de choc.
• La mortalité atteint près de 50% chez les patients DRESS admis en soins intensifs avec états de choc, selon une cohorte de 21 patients.
Nouveau syndrome SCORTCH et hypotensions retardées
Le syndrome SCORCH, identifié récemment, se manifeste par un exanthème généralisé associé à des hypotensions retardées, un profil atypique qui le distingue des réactions allergiques classiques.
• Sept patients ont été diagnostiqués avec SCORTCH suite à la prise de cotrimoxazole, avec des hypotensions survenant de 2 heures à 11 jour après traitement.
• Conjonctivite est aussi un critère spécifique.
• Une étude interne rapporte 8-9 cas similaires avec divers médicaments et délais d’apparition d’hypotension allant de 3 à 15 heures, et une tendance à un raccourcissement du délai après réintroduction.
• L’hypothèse est un relargage cytokinique.
II.Anaphylaxies médicamenteuses atypiques – Kathrin Scherer Hofmeier
Atypie temporelle :
L’anaphylaxie aux IPP peut avoir lieu entre 1h et 7h chez 10% des patients. Cette variabilité temporelle est liée à des facteurs métaboliques et génétiques, notamment les variations du gène CYP2C19. Ce délai atypique complique la surveillance post-administration et nécessite des protocoles d’observation étendus.
Il y a eu des cas d’anaphylaxie au LOPERAMIDE 10h après la prise.
L’anaphylaxie biphasique, bien que rare, présente un risque important de récidive grave sans nouvelle exposition.
Environ 4,7% de toutes les réactions anaphylactiques sont biphasique, avec un risque plus élevé chez les femmes selon un registre. Le risque augmente notamment avec certains déclencheurs comme les agents de contraste et les exercices physiques en cofacteur. Cette récurrence rend la surveillance post-réaction critique durant plusieurs heures.
Atypie clinique :
Une douleur intense au bas est évocatrice d’une anaphylaxie liée à la chimiothérapie pour un cancer gynécologique. L’urticaire bleue est un signe fréquent lors d’anaphylaxie aux colorants bleus. Le syndrome de Kounis est un syndrome coronarien aigu concomitant à une réaction d’hypersensibilité immédiate.
Mécanismes atypiques :
L’activation des mastocytes peut suivre plusieurs voies, influençant la nature des réactions allergiques.
Outre l’activation classique par IgE, certains médicaments activent les mastocytes via des récepteurs alternatifs, causant des libérations rapides de médiateurs comme le récepteur MRGPRX2. Cette activation non spécifique explique certains cas d’anaphylaxie atypique où la cause n’est pas claire.
III.Eczéma induit par les médicaments – Florence Tetart
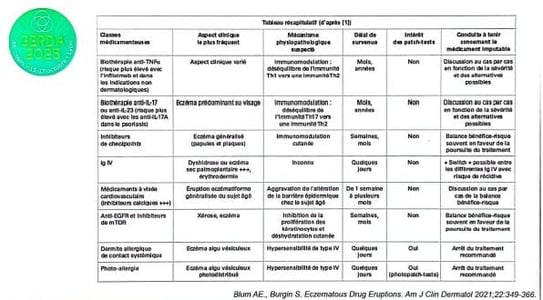
La gestion des eczémas médicamenteux repose sur une évaluation fine des symptômes pour équilibrer arrêt du traitement et poursuite selon la sévérité.
La décision d’arrêter ou poursuivre la biothérapie dépend de la sévérité de l’éruption et de la pathologie sous-jacente, illustrée par le cas d’une patiente avec une éruption sévère stoppant le traitement (toxidermie sous BIMEKIZUMAB), versus un patient avec un eczéma localisé continuant la biothérapie (eczéma palpébral sous anti-TNF)...
Les eczémas induits par médicaments résultent de mécanismes immunologiques complexes et d’altérations de la barrière cutanée. Le switch immunitaire entre réponses Th1 et Th2 ou Th17 et Th1/2 explique la survenue d’eczémas paradoxaux sous biothérapies, avec un rôle clé du terrain atopique favorisant ces réactions. Les biopsies cutanées peuvent être utiles dans ce contexte. Il y a une perturbation des boucles de rétrocontrôle négatif qui peut entraîner une surproduction de cytokines. L’effet secondaire est lié à une réponse immunitaire contre le médicament. Les inhibiteurs de checkpoint sont de plus en plus nombreux avec de plus en plus d’indications. Ils peuvent causer des dermatoses allant du simple prurit jusqu’au NET. Ils sont souvent à l’origine de réactions eczématiformes. Le DUPILUMAB peut être utile dans cette indication. L’arrêt systématique des médicaments chez les sujets âgés lors d’une réaction eczématiforme est déconseillé, la balance bénéfice-risque devant guider la décision.
• Une étude montre que l’arrêt des médicaments améliore l’évolution dans seulement 17,5% des cas, avec 45% d’aggravations liées à d’autres comorbidités.
• La complexité des ordonnances chez les patients âgés nécessite une chronologie médicamenteuse rigoureuse pour évaluer les causes des éruptions et éviter des arrêts inutiles. Les Ig IV sont régulièrement à l’origine de réaction eczématiforme. Il y a une prédominance masculine et cela est surtout dans les pathologies neurologiques. Les formes cliniques sont 1/3 dishydrose, 1/3 eczéma sec, il y a 5% d’érythrodermie. Cela peut être rapide après la première cure et cela peut persister plusieurs mois après la dernière cure.
Compte-rendu par Lou Faltot (Interne en dermatologie, Service d'Immuno-allergologie, Lyon Sud)
I.Eruptions de l’enfant, quand s’inquiéter, quand tester ? B.MILPIED, C.BERNIER
Reconnaissance et gestion des réactions cutanées chez l’enfant
L’intervention a souligné l’importance cruciale de différencier les réactions allergiques réelles des réactions virales ou médicamenteuses bénignes chez l’enfant pour protéger leur avenir thérapeutique et ne pas les priver de l’utilisation de médicaments.
•Moins de 10% des enfants présentant une éruption suite à la prise de bêtalactamines ont une allergie confirmée ;
oReconnaître les médicaments à haut risque, notamment les antiépileptiques comme la carbamazépine et la lamotrigine, phénytoïne est essentiel pour cibler les investigations. Les autres médicaments très pourvoyeurs sont les antibiotiques (bétalactamines, sulfamides).
oCette distinction évite d’interrompre inutilement des traitements indispensables et préserve l’arsenal thérapeutique futur.
•Les réactions cutanées chez l’enfant ont des délais et signes spécifiques à connaître pour orienter le diagnostic ;
oUne urticaire apparaissant plusieurs jours après le début d’un traitement est très probablement virale et non allergique.
oUne réaction survenant en moins d’une heure avec signes associés (respiratoires, digestifs voire choc anaphylactique) nécessite un test allergologique en explorations immédiate.
oLa différenciation entre exanthème maculopapuleux infectieux et toxique repose sur des critères comme la localisation initiale du rash (sur le tronc pour une origine toxique, sur le visage pour une origine virale) et la présence (viral) ou absence (toxique) de fièvre. La présence d’un prurit est plutôt en faveur d’une origine toxique.

Cas cliniques illustrant les décisions d’explorations allergologique et d’hospitalisation
•Les cas bénins comme une urticaire fugace ou un exanthème maculopapuleux sans signe de gravité ne nécessitent pas de test.
oUn garçon de 2 ans traité par antibiotique présente une urticaire isolée après plusieurs jours de traitement et sur une durée de 3 jours, sans autre signe extra-cutané → pas de test.
oUne fillette de 8 mois avec fièvre modérée, rash peu étendu, et sans altération de l’état général ni signe de gravité, à 8jours du début d’un traitement par AMOXICILLINE est plus probablement infectieuse → Réintroduction médicamenteuse à distance sans test.
•Les cas avec signes graves comme fièvre élevée, atteinte étendue (>50% de la surface corporelle), ou altération de l’état général nécessitent hospitalisation et une exploration allergologique
oCas clinique d’un enfant avec fièvre à 40°C, rash étendu, hépatomégalie et adénopathies, oedème du visage → DRESS. A été hospitalisé et confirmé allergique aux sulfamides via la réalisation de tests à distance.
oEn cas de réaction toxidermie grave, le médicament suspect doit être stoppé et les enfants hospitalisés dans des centres spécialisés.
oLa réalisation des tests allergologiques se fait souvent après une réunion de concertation pluridisciplinaire (RCP) pour discuter du rapport bénéfice/risque.
Décision stratégique sur les tests allergologiques et protocoles de suivi
•Les tests sont systématiques en cas de réactions immédiates avec symptômes d’anaphylaxie, et différés pour les réactions sévères avec altération générale
CONCLUSION
II.Vaccinations et biothérapie chez l’enfant. J.PASTEUR
La vaccination doit être planifiée avant la biothérapie pour sécuriser le traitement et limiter les risques infectieux. Les vaccins inactivés sont généralement sûrs, alors que les vivants atténués posent des risques spécifiques. La coordination entre pédiatres, allergologues et parents est essentielle pour un suivi optimal. Le Dupliumab est autorisé dès 6 mois, ce qui améliore la qualité de vie des enfants et parents, mais soulève des questions sur la tolérance vaccinale et l’efficacité. Les vaccins inactivés sont autorisés et efficaces sous biothérapie. Pas de possibilité d’effectuer des vaccins vivants. Il est crucial d’anticiper la vaccination avant le début de la biothérapie pour éviter les interruptions et maintenir un schéma vaccinal complet En ce qui concerne les vaccins vivants : délai minimum de 3 semaines entre la vaccination et le début de la biothérapie. Les décisions sur les vaccins vivants doivent être prises en collégialité, parfois avec arrêt temporaire de la biothérapie
La varicelle, vaccin vivant dès 12 mois, doit être envisagée avant le traitement chez les enfants non immunisés. La sérologie varicelle peut être réalisée en pré-thérapeutique pour guider la décision Le calendrier vaccinal comprend 11 vaccins obligatoires, majoritairement inactivés, sauf le ROR, ce qui complique la vaccination sous Dupilumab (peut être initié à l’âge de 6 mois). Il faut systématiquement interroger les familles sur les projets de voyage pour anticiper les vaccins spécifiques comme la fièvre jaune
En pratique :
DUPILUMAB / LEBRIKIZUMAB / TRALOKINUMAB → pas de possibilité d’effectuer de vaccins vivants pendant le traitement. En ce qui concerne les AntiJAK il faut éviter les vaccins vivants 4 semaines avant ou après.
Si un enfant est candidat à une biothérapie :
-Vérifier son carnet vaccinal (faire des sérologies si doute) ;
-Regarder si a déjà eu la varicelle ;
-Rattrapage vaccinal des vaccins vivants à effectuer avant le traitement ;
-Vaccin vivant délai de 3 semaines minimum avant biothérapie.
III. Est-ce possible de modifier la trajectoire atopique chez l’enfant ? C.BRAUN
La dermatite atopique précoce et sévère augmente significativement le risque d’évolution vers des maladies atopiques plus graves.Les biomarqueurs prédictifs existent pour les cohortes, mais aucun n’est fiable à l’échelle individuelle, limitant leur usage en clinique. Vivre en ville constitue un facteur aggravant de la sévérité atopique, mais cela reste difficile à modifier en pratique.
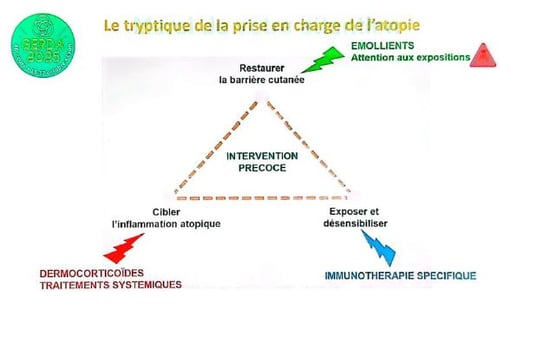
Le traitement précoce est la clé pour influencer positivement la trajectoire atopique. Cette intervention repose sur un triptyque :
- Restauration de la barrière cutanée ;
- Traitement ciblé de l’inflammation ;
- Exposition/désensibilisation aux allergènes. Restauration de la barrière cutanée Restaurer efficacement la barrière cutanée avec les bons émollients est essentiel pour prévenir et limiter la dermatite atopique. L’efficacité des émollients dépend fortement de leur composition. De nombreuses études montrent une efficacité partielle due à la diversité des émollients et protocoles testés. Certaines huiles comme l’huile d’olive ou de tournesol favorisent la pénétration antigénique, ce qui aggrave plutôt la maladie. Une application quotidienne sur l’ensemble du corps est nécessaire pour observer un effet positif sur la barrière cutanée. Erreurs courantes d’exposition à des irritants, comme l’usage de bains à la farine de blé, qui aggravent la poly sensibilisation. Ciblage de l’inflammation atopique
Traiter l’inflammation atopique de façon proactive peut réduire la sensibilisation allergique et améliorer la trajectoire atopique.
• Un traitement proactif avec dermocorticoïdes réduit la sensibilisation aux acariens comparé au traitement au coup par coup.
o Une étude menée montre que le traitement régulier améliore le score clinique et la qualité de vie.
o Cela agit sur la sensibilisation, pas encore sur les symptômes cliniques comme la rhinite. Exposition précoce et désensibilisation L’introduction précoce des allergènes alimentaires et la désensibilisation allergénique sont des leviers prometteurs pour modifier la trajectoire atopique.
• La recommandation française préconise une exposition aux allergènes alimentaires entre 4 et 6 mois, même en cas de dermatite atopique sévère.
o Cette recommandation vise à limiter la sensibilisation et à favoriser la tolérance alimentaire.
o La désensibilisation orale immédiate après réaction allergique aiguë est déjà pratiquée pour certains patients.
• L’immunothérapie allergénique pourrait prévenir l’apparition de l’asthme chez les patients avec rhinite allergique.
o La rhinite allergique apparaît aujourd’hui plus tôt, vers 2 ans contre 6 ans auparavant, justifiant un traitement plus précoce.
o Une hypothèse émergente est de désensibiliser les patients atopiques même avant l’apparition des symptômes de rhinite, ouvrant une piste pour les 5 à 10 prochaines années. Pour conclure nécessité d’une intervention précoce sur la barrière cutanée, l’inflammation et l’exposition allergénique pour changer durablement la trajectoire atopique.
Compte-rendu par Lou Faltot (Interne en dermatologie, Service d'Immuno-allergologie, Lyon Sud)
Andreas Bircher

L’IA est présente depuis des années, son développement est un processus irréversible et elle entraîne des intérêts économiques considérables. Les êtres humains ont des limites quand il faut traiter rapidement un grand volume de données et l’intelligence artificielle peut être un outil redoutable. Elle est de plus en plus sophistiquée, capable de raisonnement, d’apprentissage…. Les applications d'IA sont déjà très répandues et ont investi pratiquement tous les domaines de la vie quotidienne de plus, elles sont accessibles à pratiquement toute personne ayant des connaissances de base en informatique et un accès à Internet (démocratisation). En dépit de leurs nombreux aspects positifs, ces outils peuvent conduire à de la discrimination ou être détournés à des fins malveillantes. Bien que les applications assistées par IA dans le domaine médical visent entre autres à décharger le personnel soignant et à améliorer la prise en charge des patients, la rapide augmentation et la diffusion de ces applications s'accompagne de nouveaux défis à relever. La mise à disposition de données validées pour l'entraînement des modèles, l'évitement des biais et des inégalités, les aspects éthiques, l'instauration de la confiance dans les applications assistées par IA chez le personnel soignant et les patients, ainsi que la gestion des erreurs et des hallucinations seront des éléments centraux. Cela dit, les médecins en particulier ont l'habitude de faire face à des problématiques complexes, à des incertitudes diagnostiques, à des données manquantes, ainsi qu'à des variantes et des évolutions différentes de maladies. Ils connaissent en outre bien les effets indésirables des interventions et des médicaments, et sont ainsi prédestinés à gérer les défis posés par les applications de l'IA en médecine et leurs effets indésirables à condition de se familiariser suffisamment avec le sujet pour être prêts à y faire face.
ECZEMA de contact et IA – Marine-Alexia Lefèvre
3 axes d’application de l’IA dans l’eczéma de contact :
-Lecture de patch-test (standardisation, limité la variabilité inter-lecteurs, ouvrir la voie à une lecture à distance) ;
-Biomarqueurs diagnostics discriminants eczéma de contact allergique ou irritant (analyse transcriptomique et machine learning) ;
-Modèles prédictifs cliniques (anticiper la probabilité de test positifs, comprendre les patterns de sensibilisation, prioriser les bilans).
a/ Lecture assistée des patch tests L’intelligence artificielle peut standardiser et automatiser la lecture des patch tests pour réduire la variabilité des cliniciens.
• Les réseaux de neurones ont atteint plus de 90% de précision dans la lecture automatique des patchs, selon cinq études recensées.
o La méthode débute par une simple photo prise avec un smartphone, suivie d’un prétraitement automatisé pour normaliser la lumière et les contrastes.
o Le modèle apprend à reconnaître des motifs visuels complexes comme les papules et vésicules.
o Mais ces modèles rendent aujourd’hui des scores binaires (positif ou négatif), limitant la finesse du diagnostic.
• L’objectif est d’aboutir à une lecture rapide, standardisée et compatible avec la télé-expertise. b/ Identification et validation de biomarqueurs cliniques prédictifs L’intérêt principal et de distinguer eczéma allergique et eczéma d’irritation. Ils ont des signatures moléculaires différents.
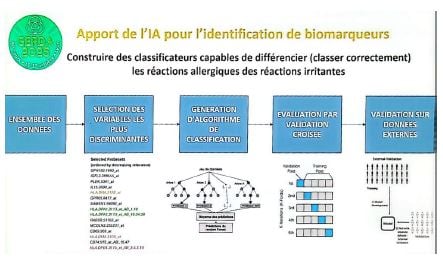
Les biomarqueurs identifiés sont notamment IGFL3 → eczéma de contact irritant, et HLA-DRA → eczéma de contact allergique.
Il y a un score de probabilité avec ces deux biomarqueurs
Cela pourrait éviter un adressage en centre expert si eczéma uniquement irritant, pourrait aider pour la lecture des patch-tests (aide à l’interprétation).
c/ Modèles prédictifs cliniques Implications stratégiques et perspectives pour la médecine de précision
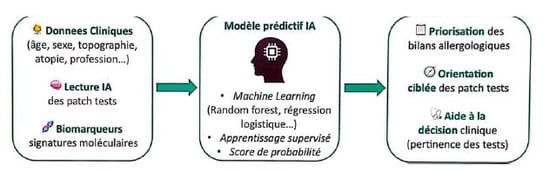
Les modèles prédictifs développés à partir de données cliniques et de l’intelligence artificielle permettent d’anticiper la probabilité de sensibilisation, d’optimiser les bilans et de renforcer la pertinence clinique des tests allergologiques.
III.Dermatite atopique et intelligence artificielle - Delphine Staumont-Sallé L’IA permet de rendre le diagnostic et l’évaluation de la dermatite atopique plus précis et rapides, même dans des contextes cliniques complexes. Le diagnostic de la dermatite atopique n’est pas forcément facile pour le médecin généraliste ou lors de cas compliqués.
• L’utilisation du deep learning améliore la précision du diagnostic différentiel entre dermatite atopique, psoriasis et autres eczémas.
o Les banques d’images alimentent ces modèles pour une meilleure spécificité.
o Le diagnostic visuel, traditionnellement subjectif, devient plus objectif et reproductible grâce à l’analyse d’images.
o Cette approche aide particulièrement en soins primaires ou pour des peaux foncées souvent sous-représentées.
• Le scoring automatique de la sévérité via photo analyse améliore la mesure de l’étendue et de l’intensité des lésions.
o Une équipe espagnole a développé un outil mesurant précisément la surface corporelle atteinte et les types de lésions.
o Ce système intègre aussi des données sur le sommeil et la qualité de vie pour une vision globale. Medela A, Mac Carthy T, Aguilar Robles SA, Chiesa-Estomba CM, Grimalt R. Automatic SCOring of Atopic Dermatitis Using Deep Learning: A Pilot Study. JID Innov. 2022 L’IA ouvre la voie à une classification fine des patients selon des signatures moléculaires & environnementales pour personnaliser les traitements :
• Evaluation des différents endotypes par une machine learning non supervisé permet d’identifier des endotypes basés sur gènes, microbiote, environnement.Ces classifications aident à proposer des traitements adaptés à chaque profil.L’intégration de données biologiques et environnementales améliore la compréhension des endotypes.
•Pour prédire la sévérité de la DA, il y a eu l’analyse de 130 facteurs par une méthode de machine learning. Les facteurs mis en évidence sont l’âge, une apparition plutôt tardive, la présence d’une chéilite, d’un dermographisme, un tabagisme actif, une activité sportive réduite et la perte du tiers externe du sourcil (signe d’Hertoghe).
L’IA contribue à identifier les patients à risque de non-réponse ou d’effets secondaires. L’analyse prédictive des échecs thérapeutiques a montré que la consommation d’anti-inflammatoires comme l’ibuprofène prédit une mauvaise réponse au dupilumab chez environ un tiers des patients. L’IA permet aussi de développer des solutions non médicamenteuses pour améliorer la qualité de vie des patients. L’intégration de programmes d’ETP via outils connectés aide à réduire le prurit et les poussées. L’appli ATOPIC APP permet de déclencher des exercices de méditation et de gestion du stress en cas de poussée. Un capteur placé au niveau de la main émet une vibration pour interrompre le grattage avant qu’il ne devienne excessif. Cette approche réduit les réveils nocturnes liés au prurit. Yang AF et al. Artificial Intelligence-Enabled Wearable Devices and Nocturnal Scratching in Mild Atopic Dermatitis. JAMA Dermatol 2025
IV.IA et toxidermie – Marie Tauber
La médecine de précision offre des outils innovants pour anticiper et diagnostiquer les hypersensibilités médicamenteuses souvent imprévisibles et graves.
Une étude pilote de 2022 a identifié une signature transcriptomique spécifique du DRESS aux antibiotiques dans deux cohortes. Une shortlist de 6 gènes discriminants a été établie avec une très bonne sensibilité et spécificité. Cette signature n’a pas été retrouvée dans des dermatoses inflammatoires contrôles, soulignant sa spécificité diagnostique. Cette méthode pourrait devenir un outil d’aide au diagnostic rapide par simple prise de sang dans des cas complexes.
Teo YX et al. Potential Biomarker Identification by RNA-Seq Analysis in Antibiotic-Related Drug Reaction with Eosinophilia and Systemic Symptoms (DRESS): A Pilot Study. Toxicol Sci. 2022
Une équipe lyonnaise a développé une méthode simple basée sur un panel réduit de 14 gènes pour guider la prise en charge des dermatoses médicamenteuses complexes. Ils réalisent une biopsie cutanée en zone lésée et saine, suivie d’une RT-QPCR ciblée sur ce panel ; Une cartographie de signatures permet de comparer les profils des patients à des dermatoses types comme psoriasis ou eczéma atopique ;
Cette méthode a permis d’orienter le traitement chez un patient de 72 ans atteint de prurigo avec un profil IL-13 élevé, qui a bénéficié d’un inhibiteur JAK hors AMM avec une amélioration notable ; Un autre patient de 64 ans avec une dermatite atopique a vu son traitement ajusté après analyse transcriptomique car signature IL-13 élevée restant persistante après traitement par TRALOKINUMAB, passant à anti-JAK avec une très bonne efficacité.
L’IA démontre une performance supérieure à celle des experts pour certains diagnostics d’exanthèmes médicamenteux :
-Une étude japonaise a analysé plus de 25 000 images d’exanthèmes de 123 patients pour distinguer des formes graves comme le LYELL / SJS : l’IA a surpassé les performances de 10 dermatologues experts et 24 internes dans la reconnaissance des formes précoce.
-L’IA améliore aussi la prédiction des allergies aux bêtalactamines par rapport aux scores classiques comme le PENFAST : elle reste performante même avec des données cliniques incomplètes, ce qui est crucial en situation d’urgence ou lorsque les tests allergologiques ne sont pas disponibles. Cela facilite la prise de décision thérapeutique quand les tests biologiques manquent.
Créez en toute simplicité votre compte professionnel
Je crée mon compteAméliorez vos connaissances professionnelles en profitant de nombreux services exclusifs dans le domaine de la dermatologie : plus de 500 visuels de pathologies, des cas cliniques, des vidéos d’experts…
Bénéficiez d’options uniques telles que l’offre de contenus audio et de supports à proposer à vos patients.
Restez informé(e) des événements et des webinaires à venir, des dernières publications scientifiques et des innovations produit.