2 professionals
Coup d'œil du congrès EHRS 2025
Coup d'œil du congrès EHRS 2025
Rapports rédigés par le Dr Lidiya Todorova (dermatologue, Bulgarie) et le Dr Nicolas Kluger (dermatologue, Finlande).

Sujets liés
Compte rendu rédigé par le Dr Lidiya Todorova (dermatologue, Bulgarie)
Intervenante : Prof. Lidia Rudnicka, Pologne
La trichoscopie est une technique de diagnostic non invasive qui permet de visualiser des éléments bien précis du cuir chevelu qui ne sont pas visibles à l’œil nu. Les principales structures trichoscopiques sont les tiges capillaires, les orifices folliculaires (appelés « points »), la surface de la peau et les vaisseaux sanguins. Chacune de ces structures fournit des indices précieux pour le diagnostic des affections au niveau des cheveux et du cuir chevelu, par exemple la pelade, l’alopécie androgénétique et les alopécies cicatricielles.
Les anomalies fondamentales observées à la trichoscopie au niveau des tiges capillaires sont les suivantes :
L’anomalie la plus connue au niveau de la tige capillaire est probablement le « cheveu en point d’exclamation ». Cette anomalie se caractérise par une terminaison distale normale et une terminaison proximale plus fine, signe d’une faible activité mitotique des cellules. À la trichoscopie, les anomalies de la tige capillaire peuvent être utilisées comme un outil précieux pour diagnostiquer différentes maladies du cheveu :
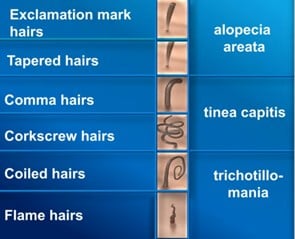
La deuxième structure importante à la trichoscopie est la perte d’épaisseur, qui peut être généralisée (toutes les tiges capillaires ont le même diamètre), ce qui est typique de l’effluvium télogène, ou non généralisée (variation du diamètre de la tige capillaire, anisotrichie), ce qui est caractéristique de l’alopécie androgénétique.
En ce qui concerne le nombre de cheveux par unité folliculaire, en temps normal, un follicule pileux contient 1 à 3 tiges capillaires. En cas d’alopécie androgénétique, par exemple, on observe principalement un cheveu par unité, alors que dans la folliculite en touffes, on trouve plus de cinq tiges capillaires par unité folliculaire.
À la trichoscopie, les orifices folliculaires dépourvus de tige capillaire sont appelés des « points ». Les « points jaunes » sont des follicules pileux vides remplis de sébum et/ou de substance kératosique. Quand ils sont multiples et régulièrement répartis, ils sont typiques d’une pelade de longue durée. Les « points noirs » indiquent des follicules pileux qui sont remplis de résidus de la tige capillaire après que celle-ci a été détruite ou cassée (en cas de pelade active, de trichotillomanie ou de teigne du cuir chevelu).
Lorsque l’on examine le cuir chevelu à la trichoscopie, il faut également évaluer la surface de la peau et juger si les changements sont diffus ou s’ils concernent uniquement la zone périfolliculaire. La desquamation diffuse, par exemple, se rencontre dans le psoriasis, la dermatite séborrhéique et le lupus discoïde, tandis que la desquamation périfolliculaire est typique du lichen plan pilaire, de l’alopécie frontale fibrosante et de la folliculite décalvante.
Enfin, les vaisseaux sanguins sont également importants pour l’évaluation de la pathologie. Les vaisseaux télangiectatiques, qui forment des îlots distincts d’érythème sur le cuir chevelu, peuvent être le signe d’un trouble capillaire émergent. Des vaisseaux arborescents épais sont fréquemment observés dans le lupus et le lichen plan pilaire, tandis que des vaisseaux arborescents fins et régulièrement répartis peuvent être normaux.
La trichoscopie est devenue un outil essentiel dans l’évaluation des troubles capillaires et du cuir chevelu. Grâce à son travail pionnier, le professeur Rudnicka a permis de définir et de normaliser ces critères de diagnostic, facilitant ainsi un diagnostic et un suivi plus précoces et plus précis des troubles liés à la perte de cheveux dans la pratique clinique.
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Marta Kurzeja, Pologne
La trichoscopie est une technique de diagnostic non invasive, réalisée en cabinet, qui utilise la dermoscopie pour examiner le cuir chevelu et les cheveux. Cette technique permet un grossissement des tiges capillaires et des follicules pileux, mais aussi du cuir chevelu, ce qui fournit des informations essentielles sur les différents troubles capillaires et du cuir chevelu. La trichoscopie peut éviter les biopsies du cuir chevelu ou permettre de choisir le meilleur endroit pour une biopsie, de surveiller la progression de la maladie et la réponse au traitement.
La trichoscopie nécessite l’utilisation d’un dermoscope ou d’un vidéodermoscope portatif, réglés sur un grossissement généralement compris entre 10x et 70x. Elle permet aux dermatologues d’identifier des schémas spécifiques, tels que :
Il faut préalablement indiquer au patient de ne pas se laver les cheveux pendant 2 à 3 jours avant la trichoscopie.
La trichoscopie peut être à sec ou humide (avec l’application d’une huile d’immersion). La trichoscopie à sec permet d’évaluer la présence de squames avant la trichoscopie humide. Une faible pression est appliquée lors de l’évaluation des vaisseaux sanguins.
En cas de perte de cheveux diffuse, le cuir chevelu est examiné en trois endroits :
Il est recommandé de prendre des photos selon un grossissement de x20 et x70.
En cas d’alopécie en plaques, la zone est examinée en deux endroits :
Les artefacts peuvent être dus au fond de teint, au maquillage permanent (sur les sourcils), à la teinture dans les cheveux et aux saletés chez les enfants.
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Daniel Asz Sigall, Mexique
L’alopécie induite par les produits de comblement est une forme rare de perte de cheveux qui constitue une complication des injections de produits de comblement dermiques, généralement à base d’acide hyaluronique. Cette forme d’alopécie a également été signalée après d’autres actes médicaux impliquant des injections, par exemple d’acide désoxycholique, de graisse, d’acide poly-L-lactique ou dans le cadre d’une mésothérapie. Cette complication survient lorsque le produit de comblement est accidentellement injecté dans ou comprime un vaisseau sanguin, ce qui compromet l’irrigation sanguine du cuir chevelu ou du front, endommageant ainsi les follicules pileux et provoquant une chute de cheveux localisée. Le mécanisme est double : non cicatriciel par compression vasculaire locale et cicatriciel par thrombose vasculaire conduisant à la nécrose. Les signes et symptômes apparaissent entre un jour et une semaine après l’intervention et peuvent inclure un érythème local, un œdème local, une douleur, une ulcération, une nécrose et des plaques d’alopécie irrégulières. La trichoscopie rappelle l’effluvium anagène, puisqu’elle montre des points noirs, des cheveux cassés, des cheveux effilés, des zones rouge laiteux et des ulcères. En cas de suspicion d’AF, une échographie doppler doit être réalisée pour évaluer l’étendue des lésions vasculaires. La prise en charge comprend l’injection de hyaluronidase (en cas d’injection d’acide hyaluronique), l’injection de triamcinolone, l’application de compresses chaudes, la prise orale de sildénafil pour la vasodilatation et la prise d’acide salicylique. Si le traitement est précoce, la perte de cheveux peut parfois être inversée. La repousse dépend de l’étendue de la nécrose. Le seul facteur de risque semble être la quantité injectée : il est fortement conseillé d’injecter moins de 1 ml par site pour éviter ces effets indésirables. Avec l’augmentation des actes de médecine esthétique, cet effet indésirable est appelé à devenir plus fréquent.
Compte rendu rédigé par le Dr Lidiya Todorova (dermatologue, Bulgarie)
Intervenante : Ana-Waskiel-Burnat, Pologne
La pelade est une perte de cheveux courante, à médiation immunitaire, non cicatricielle, caractérisée par l’apparition soudaine de plaques d’alopécie bien délimitées, le plus souvent sur le cuir chevelu, mais pouvant toucher n’importe quelle partie du corps qui comporte une pilosité. La pelade concerne environ 1 à 2 % de la population générale et peut se manifester à tout âge. Cette affection résulterait d’une attaque auto-immune au niveau des follicules pileux en phase anagène (croissance), ce qui entraîne un dysfonctionnement folliculaire sans destruction permanente.
Sur le plan clinique, la pelade peut prendre différentes formes, allant de l’alopécie en plaques à des formes plus étendues telles que l’alopécie totalis (perte complète des cheveux sur le cuir chevelu) ou l’alopécie universelle (perte totale des cheveux et des poils). Le rôle de la susceptibilité génétique, des déclencheurs environnementaux et des associations avec d’autres maladies auto-immunes (par exemple, la thyroïdite, le vitiligo) ont été démontrés dans sa pathogenèse.
La trichoscopie permet de visualiser en détail les caractéristiques de la maladie telles que les points jaunes, les points noirs, les cheveux point d’exclamation et les cheveux cassés. Ces caractéristiques facilitent le diagnostic précoce, l’évaluation de l’activité de la maladie et le diagnostic différentiel par rapport à d’autres types de pertes de cheveux.
En cas de chute active des cheveux dans le cadre d’une pelade, des points noirs sont fréquemment observés à la trichoscopie. Ce signe n’est pas pathognomonique, car il est également visible dans la cellulite disséquante, la trichotillomanie et la teigne du cuir chevelu. Quand la maladie est active, on peut également observer des cheveux en point d’exclamation, qui sont également présents en cas de trichotillomanie, de teigne du cuir chevelu et d’alopécie chimio-induite. Les cheveux sont alors des brins courts et cassés, plus épais à l’extrémité et plus étroits à la base, ressemblant à un point d’exclamation. Les cheveux effilés sont des cheveux terminaux plus longs que les cheveux point d’exclamation, présentant une extrémité proximale plus fine et une extrémité distale plus épaisse. Ces cheveux sont visibles à l’œil nu et sont souvent présents autour des lésions, indiquant l’activité de la maladie. Les cheveux cassés sont également un signe de pelade active. Les constrictions de Pohl-Pinkus, rétrécissements irréguliers le long de la tige capillaire, bien que rarement observées en cas de pelade, peuvent indiquer une maladie active ou des poussées, et sont également associées à d’autres affections telles que l’alopécie chimio-induite et certaines maladies systémiques.
Lorsque la pelade entre dans une phase chronique, les principaux marqueurs à la trichoscopie sont les points jaunes et le vellus ; tandis que dans la phase de repousse des cheveux, on observe typiquement un vellus, des cheveux enroulés (en tire-bouchon) et des cheveux repoussant à la verticale. Des points jaunes sont également observés en cas d’alopécie androgénétique, de cellulite disséquante et de lupus érythémateux discoïde. D’autre part, les cheveux enroulés sont couramment observés dans toute repousse de cheveux après, par exemple, un effluvium télogène aigu ou chronique.
Tableau 1 : tableau - trichoscopie en fonction de l’activité de la maladie
| Signes à la trichoscopie en cas de pelade active | Signes à la trichoscopie en cas de pelade chronique | Signes à la trichoscopie lors de la repousse des cheveux en cas de pelade |
|
|
|
|
|
|
|
|
|
|
||
|
Compte tenu de son évolution imprévisible, de son impact psychologique et de sa réponse variable au traitement, la pelade reste un sujet de recherche clinique et translationnelle, l’accent ayant été mis récemment sur les traitements immunomodulateurs. Comme approche thérapeutique, le professeur Waskiel-Brunat a évoqué les directives fournies dans la déclaration de consensus des experts européens en ce qui concerne le traitement systémique de la pelade, directives qui ont été publiées dans le JEADV*.
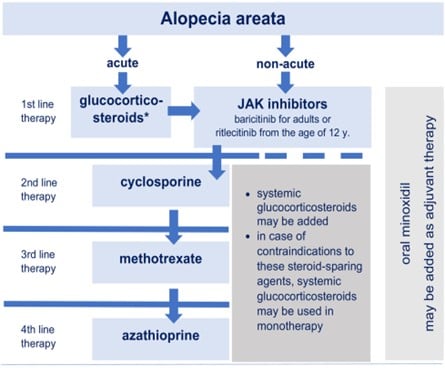
Figure 1. Proposition d’algorithme thérapeutique pour le traitement systémique de la pelade*.
* Rudnicka, L, Arenbergerova, M, Grimalt, R, et al. European expert consensus statement on the systemic treatment of alopecia areata. J Eur Acad Dermatol Venereol 2024; 38: 687-694. https://doi.org/10.1111/jdv.19768
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : David Saceda Corralo, Espagne
Le score SALT (Severity of ALopecia Tool) est un système standardisé qui permet de quantifier l’étendue de la perte de cheveux chez les patients atteints d’une pelade. Cet outil a été élaboré par Olsen et al en 1999 (Olsen EA, Hordinsky M, McDonald-Hull S, et al. Alopecia areata investigative guidelines. J Am Acad Dermatol. 1999;40:242–246). Il fournit une mesure objective pour suivre la progression de la pelade, évaluer la réponse au traitement et faciliter l’évaluation des essais cliniques.
Le cuir chevelu se divise en 4 régions, chacune correspondant à un pourcentage de la surface totale du cuir chevelu :
| Région du cuir chevelu | % du cuir chevelu total |
| Vertex (sommet) | 40 % |
| Profil droit | 18 % |
| Profil gauche | 18 % |
| Postérieure (arrière) | 24 % |
Pour chaque région, l’observateur doit estimer le pourcentage de perte de cheveux dans cette zone, puis multiplier par le poids de la région et additionner les résultats pour obtenir le score SALT total.
Score SALT = Σ (% de perte de cheveux dans chaque région × % de poids de la région)
|
Aucune perte de cheveux | |||||
|
Perte de cheveux légère | |||||
|
Perte de cheveux modérée | |||||
|
Perte de cheveux sévère | |||||
|
Perte de cheveux très sévère | |||||
|
Perte totale des cheveux (alopécie totalis) | |||||
Les inhibiteurs de JAK sont actuellement indiqués face à la pelade modérée à sévère, à savoir un score SALT de 50 ou plus.
Compte rendu rédigé par le Dr Lidiya Todorova (dermatologue, Bulgarie)
Intervenante : Adriana Rakowska, Pologne
Qu’est-ce qu’un cheveu normal ? C’est un cheveu dont l’épaisseur est uniforme, dont la plupart des tiges capillaires ont une épaisseur supérieure à 50 µg et dont la majorité des unités folliculaires comportent trois tiges capillaires. L’alopécie androgénétique (AAG) touche 80 % des hommes et 40 % des femmes au cours de leur vie. Elle se définit par une miniaturisation progressive du follicule pileux. En raison d'une prédisposition génétique et de l’activité de la dihydrotestostérone (DHT), à chaque cycle pilaire, la tige capillaire devient de plus en plus mince jusqu’à ce qu’elle se transforme en vellus. L’AAG se caractérise donc par une hétérogénéité de plus de 20 % au niveau de l’épaisseur de la tige capillaire, c’est-à-dire une anisotrichie.
À la trichoscopie, l’AAG se traduit également par la présence de plus de 10 % de vellus et de points jaunes. Un autre marqueur de l’AAG est le signe péripilaire, conséquence de la micro-inflammation périfolliculaire provoquée par les lymphocytes T activés autour de la partie supérieure des follicules pileux. Comme évoqué précédemment, les personnes en bonne santé ont normalement une moyenne de trois cheveux dans chaque unité folliculaire, alors qu’en cas d’AAG, les unités folliculaires contiennent généralement un seul cheveu.
La perte de cheveux chez la femme étant plus complexe que chez l’homme, il existe des critères majeurs et mineurs pour son évaluation.
Critères majeurs :
Critères mineurs :
Le diagnostic est posé lorsqu’un patient présente 2 critères majeurs, ou 1 critère majeur et 2 critères mineurs.
Les objectifs thérapeutiques face à l’alopécie androgénétique sont de stopper la progression de la maladie et d’améliorer l’épaisseur et la densité des cheveux. Seul un traitement prolongé permet d’atteindre ce dernier objectif.
Le professeur Rakowska a souligné qu’il est recommandé de pratiquer une trichoscopie tous les six mois pour évaluer le traitement et, si nécessaire, le modifier. Elle a également suggéré l’approche thérapeutique suivante :
| AAG / perte de cheveux chez l’homme | AAG / perte de cheveux chez la femme | |
|
Traitement de première ligne |
Minoxidil oral à faible dose 1 - 5 mg + Finastéride 1 mg OU dutastéride 0,5 mg |
Minoxidil oral à faible dose 0,5 - 1 mg + Finastéride 2,5 - 5 mg OU dutastéride 0,5 mg + Spironolactone 25-50 mg |
| Traitement supplémentaire | Minoxidil topique 2-5 %, finastéride topique, plasma riche en plaquettes, traitement laser de faible intensité | |
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Ozlem Dicle, Turquie
L’alopécie frontale fibrosante (AFF) est une alopécie cicatricielle lymphocytaire primaire décrite pour la première fois en 1994 par Kossard. Elle se caractérise par une récession frontotemporale progressive de la ligne d’implantation des cheveux, souvent accompagnée d’une perte des sourcils, des cils et des poils sur le reste du corps. Considérée comme une variante clinique du lichen plan pilaire, l’AFF a connu une augmentation spectaculaire de son incidence au cours des 20 dernières années, en particulier chez les femmes ménopausées. Des signalements de plus en plus nombreux chez les hommes et les patients jeunes suggèrent toutefois un spectre démographique plus large. Cette affection nuit considérablement à la qualité de vie des patients concernés1.
Quand l’AFF progresse activement, le dermatologue doit avoir connaissance de la récession de la ligne d’implantation frontotemporale des cheveux, de l’hyperkératose périfolliculaire et de l’érythème. À la trichoscopie, les signes caractéristiques de l’AFF sont les « cheveux isolés » observés dans la zone touchée. Il s'agit de cheveux terminaux seuls situés dans la bande alopécique. La dermoscopie ne révèle pas de vellus, mais plutôt des follicules pileux vides ou des points blancs indiquant les follicules pileux fibrosants.
Encore une fois, cette affection se traduit par une perte des sourcils, phénomène courant chez de nombreux patients (73 à 95 %)1. Dans 39 % des cas, la chute des sourcils précède celle des cheveux2. La perte des poils peut également toucher les favoris, le cuir chevelu occipital, les cils, le corps et, chez les hommes, la barbe et la moustache3,4. En cas d’atteinte des favoris par rapport à la récession frontotemporale, la desquamation et l'érythème périfolliculaires sont moins importants, et les tiges capillaires proximales transparentes sont prédominantes (79,2 %)3.
Cette affection est également associée à des lésions faciales, dont les dermatologues doivent avoir conscience : papules faciales, hyper- ou hypopigmentation, éruptions de type rosacée et veines faciales proéminentes (atrophie de la peau sus-jacente)5.
La récession de la ligne d’implantation des cheveux suit plusieurs schémas qui permettent également de prédire le pronostic de la maladie...
Le professeur Dicle a ajouté plusieurs caractéristiques trichoscopiques supplémentaires de l’AFF qui ne sont pas pathognomoniques...
L’approche thérapeutique des dermatologues qui prennent en charge des cas d’AFF doit s'appuyer sur deux grands points...
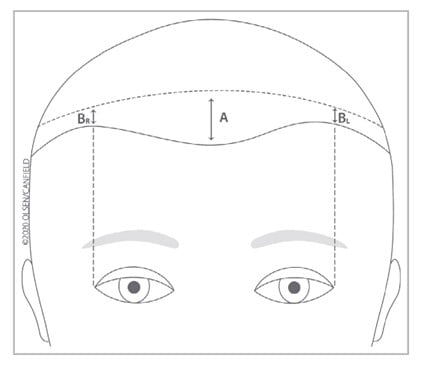
Figure 2. Mesure quantitative de la récession de la ligne d’implantation frontale et temporale des cheveux.
« A » désigne l’importance ou le degré de récession de la ligne d’implantation frontale des cheveux, c’est-à-dire la distance en centimètres, à une décimale près, au centre de la ligne d’implantation frontale des cheveux, entre le bord supérieur des rides du front lorsque le patient hausse les sourcils et une zone située juste derrière la ligne d’implantation, où la densité des cheveux est la plus confluente et homogène. Ce chiffre sera utilisé directement, et non par catégorie, dans les mesures séquentielles, afin que les informations les plus fiables soient recueillies en ce qui concerne cette caractéristique très importante de l’AFF. Pour les patients à la peau claire qui ont reçu des injections de botox ou qui nécessitent une aide supplémentaire, la fin du photodommage peut être utilisée à la place du bord supérieur des rides du front lorsqu’ils haussent les sourcils.
« B » désigne l’importance ou le degré de récession de la ligne d’implantation temporale des cheveux, c’est-à-dire la distance en centimètres au centre de chaque zone temporale (à savoir le point d’alignement supérieur du canthus latéral), entre le bord supérieur des rides du front lorsque le patient hausse les sourcils et une zone située juste derrière cette zone, où la densité des cheveux est la plus confluente et homogène. Pour les patients à la peau claire qui ont reçu des injections de botox ou qui nécessitent une aide supplémentaire, la fin du photodommage peut-être utilisée à la place du bord supérieur des rides du front lorsqu’ils haussent les sourcils. La récession capillaire temporale doit être mesurée séparément à gauche et à droite1.
Pour éliminer l’inflammation, la première étape consiste à évaluer si le processus inflammatoire est léger, modéré ou intense. S’il est léger, le traitement recommandé comprend des corticoïdes topiques une à deux fois par semaine et du pimécrolimus crème 1 % (ou du tacrolimus en pommade 0,1 %). L’inflammation modérée est traitée elle aussi par ce traitement topique, auquel s’ajoute de l’acétonide de triamcinolone intralésionnel 4 mg/ml, toutes les 6 à 8 semaines, avec/sans hydroxychloroquine orale 200 mg/jour. En cas de processus intense, les traitements topiques peuvent être complétés par de l’acétonide de triamcinolone intralésionnel 4 mg/ml toutes les 6 à 8 semaines avec/sans corticoïdes systémiques (c’est-à-dire du triamcinolone intramusculaire) et de l’hydroxychloroquine orale 200 - 400 mg/jour ou de la doxycycline orale 100 - 200 mg/jour.
Pour contrôler la progression de la maladie chez les femmes en âge de procréer, l’intervenante a suggéré du dutastéride par voie orale 0,5 mg par jour ou du finastéride par voie orale 2,5 à 5 mg par jour. Chacun de ces traitements peut être associé à des anti-inflammatoires topiques et oraux ou à de l'acétonide de triamcinolone intralésionnel.
Pour améliorer l’épaisseur des cheveux, il est conseillé d’utiliser du minoxidil topique 2-5 % ou du minoxidil oral à faible dose (0,5-2 mg/jour). En ce qui concerne les papules faciales, le plan de traitement comprend l’isotrétinoïne 5 à 10 mg par jour.
D’autres options thérapeutiques doivent être envisagées en fonction de la réponse du patient aux traitements précédents et de la disponibilité des médicaments : ciclosporine, méthotrexate, pioglitazone, naltrexone, isotrétinoïne, inhibiteurs de JAK.
Il est essentiel pour les dermatologues de reconnaître rapidement l’AFF, car cette maladie entraîne une destruction folliculaire irréversible. En raison de sa progression souvent subtile et lente, l’AFF peut être confondue avec une perte d’épaisseur des cheveux liée à l’âge ou avec d’autres formes d’alopécies. Il est essentiel de connaître ses caractéristiques trichoscopiques et cliniques distinctes, telles que l’érythème périfolliculaire, l’hyperkératose folliculaire et l’absence d’orifice folliculaire, afin de mettre rapidement en place un traitement visant à stopper la progression de la maladie et à préserver la densité capillaire.
Littérature :
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Maria Fernanda Gavazzoni Diaz, Brésil
L’alopécie fibrosante avec distribution de type lichen plan pilaire est une forme distincte d’alopécie cicatricielle qui présente à la fois des caractéristiques de l’alopécie androgénétique (AAG) et du lichen plan pilaire (LPP). Sur le plan clinique, elle se caractérise par une perte de cheveux selon un certain schéma et des cheveux clairsemés au centre du cuir chevelu. La trichoscopie et l’histopathologie révèlent toutefois un érythème périfolliculaire, une hyperkératose et une fibrose, caractéristiques de l’alopécie cicatricielle lymphocytaire. D’abord décrite comme une variante du LPP, cette alopécie fibrosante est de plus en plus reconnue comme une entité distincte présentant des caractéristiques communes avec l’alopécie inflammatoire et l’alopécie influencée par les hormones.
Les symptômes et signes cliniques de l’alopécie fibrosante avec distribution de type lichen plan pilaire sont les suivants :
Un tableau clinique très typique est des cheveux clairsemés et une ligne d’implantation frontale inchangée.
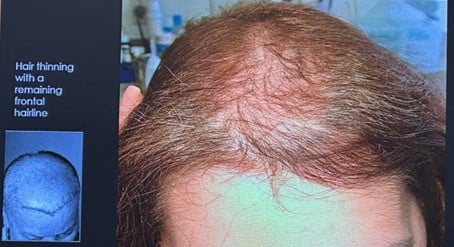
Figure 3. Cheveux clairsemés et ligne d’implantation frontale inchangée. Image tirée de la conférence de Maria Fernanda Gavazzoni Diaz, Brésil.
La trichoscopie montre :
L’intervenante s’est particulièrement intéressée aux « îlots rouges », dernière découverte en date dans l’alopécie fibrosante avec distribution de type lichen plan. À ce sujet, elle a décrit des plaques rouges comportant des vaisseaux arborescents ou des points rouges et des stries blanches.
Tous les marqueurs trichoscopiques cités peuvent être observés non seulement sur le cuir chevelu, mais aussi au niveau de la barbe. Lorsqu'ils évaluent un patient à la peau sombre, les dermatologues doivent savoir que la dermoscopie du cuir chevelu foncé atteint d’alopécie fibrosante avec distribution de type lichen plan révèle un réseau pigmenté asymétrique et irrégulier, un halo pigmenté périfolliculaire, des points blancs répartis de manière irrégulière, une absence d’ostia folliculaires et une anisotrichie (les îlots rouges sont rares).
En termes de diagnostic différentiel entre l’alopécie androgénétique (AAG), l’alopécie fibrosante avec distribution de type lichen plan et le lichen plan pilaire, voici quelques points à retenir :
Le traitement suggéré face à l’alopécie fibrosante avec distribution de type lichen plan comprend le dutastéride 0,5 mg/jour ou le finastéride 1 mg/jour (hommes) et 5 mg/jour (femmes) associé à de l’hydroxychloroquine 400 mg/jour et/ou à de la doxycycline 100 mg/jour plus du minoxidil oral 0,25-5 mg/jour. L’autre protocole thérapeutique recommandé comprend du minoxidil topique 5 % associé à du clobétasol topique et/ou à du tacrolimus, plus de l’acétonide de triamcinolone intralésionnel 25 mg/ml toutes les 6 semaines.
Dans un contexte où la prévalence de l’alopécie fibrosante avec distribution de type lichen plan semble augmenter, en particulier chez les femmes, une sensibilisation accrue est essentielle pour une intervention opportune et de meilleurs résultats pour les patients. Les dermatologues doivent impérativement connaître cette affection, car s’ils diagnostiquent à tort une simple AAG, cela peut entraîner un retard de traitement et une perte de cheveux irréversible. Contrairement à l’AAG, qui est non cicatricielle et d’évolution lente, l’alopécie fibrosante avec distribution de type lichen plan comprend une inflammation active. La reconnaissance des signes cliniques subtils, l'utilisation efficace de la trichoscopie et la confirmation du diagnostic par une biopsie, si nécessaire, sont essentielles pour mettre en place des traitements anti-inflammatoires adaptés.
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Alexander Katoulis, Grèce
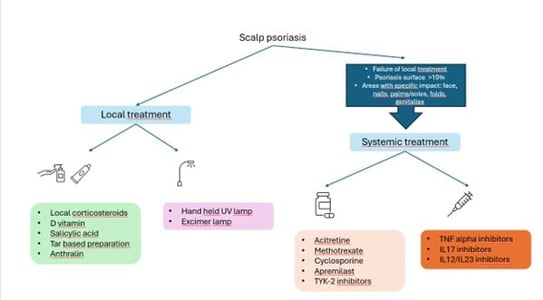
Le cuir chevelu est l’un des premiers sites anatomiques touchés par le psoriasis. Cette affection peut survenir seule ou en association avec d’autres manifestations. Le psoriasis du cuir chevelu touche les zones occipitales et temporales. Il peut rester limité à la zone des cheveux ou s'étendre au-delà, sur la peau (front, nuque). Les démangeaisons sont parfois intenses. Le psoriasis du cuir chevelu peut également être associé à P. ovale et être confondu avec ou associé à une dermatite séborrhéique. Le psoriasis du cuir chevelu en tant que tel peut avoir un impact profond sur la qualité de vie.
Les caractéristiques du psoriasis du cuir chevelu à la trichoscopie sont les suivantes :
La prise en charge est résumée ici :
Compte rendu rédigé par le Dr Lidiya Todorova (dermatologue, Bulgarie)
Intervenante : Jacek C. Szepietowski, Pologne
Les démangeaisons du cuir chevelu, ou prurit du cuir chevelu, sont un symptôme fréquent, mais souvent sous-estimé en dermatologie, qui touche un large éventail de patients avec ou sans pathologie visible au niveau du cuir chevelu. Elles peuvent découler de dermatoses inflammatoires telles que la dermatite séborrhéique, le psoriasis et la dermatite atopique, ou survenir dans le contexte de troubles entraînant une perte de cheveux, tels que le lichen plan pilaire, la pelade et même l’alopécie androgénétique. Dans d’autres cas, le prurit du cuir chevelu peut être neuropathique, psychogène ou idiopathique, ce qui pose un défi diagnostique et thérapeutique.
Par définition, le prurit est une sensation désagréable qui pousse à se gratter. Cette définition, proposée en 1660, est toujours valable. Toutefois, ce concept est très imprécis, car le terme « désagréable » est subjectif. À ce jour, de nombreuses tentatives nouvelles mais insatisfaisantes ont été faites pour élaborer une nouvelle définition. Les démangeaisons peuvent être qualifiées d’aiguës (mécanisme de défense) et de chroniques (état pathologique). D’un point de vue épidémiologique, le prurit touche 8,9 à 16,8 % de la population, et le risque d’apparition d’une démangeaison chronique augmente de 2 % chaque année. Cette affection est deux fois plus fréquente chez les retraités que chez les personnes qui ont une activité professionnelle. Dans l’ensemble, 11,5 % des patients dans les services de dermatologie sont hospitalisés en raison de démangeaisons, qui constituent le troisième motif d’hospitalisation.
En dermatologie, les démangeaisons sont souvent associées aux maladies auto-immunes du tissu conjonctif, aux maladies auto-immunes bulleuses, aux dermatoses de la grossesse, aux maladies papulo-érythémateuses, aux allergies cutanées, aux infections et infestations, à la xérose cutanée, à la mastocytose, à l’amylose cutanée primitive, aux lymphomes cutanés, aux maladies des glandes eccrines, des glandes apocrines et des glandes sébacées. Il arrive également fréquemment que le prurit du cuir chevelu ne soit associé à aucune cause évidente, ce qui en fait une situation pénible tant pour le dermatologue que pour le patient. S’il est vrai que diverses pathologies peuvent contribuer au prurit du cuir chevelu, le cuir chevelu lui-même possède une neuroanatomie et une vascularisation distinctes, des neuromédiateurs spécifiques et des récepteurs correspondants, ainsi que la présence d’un sébum et d’une microflore du cuir chevelu, autant de propriétés qui peuvent expliquer sa tendance à être atteint chez les patients qui se plaignent de démangeaisons1.
Les études suggèrent une classification du prurit du cuir chevelu en deux types : avec ou sans lésions dermatologiques, et avec ou sans chute de cheveux. Il est également important de penser d'abord aux causes les plus courantes et d’exclure ensuite d’autres étiologies moins fréquentes. L’acronyme SCALLP et les cinq étapes de l’évaluation du cuir chevelu (écouter, regarder, toucher, agrandir et prélever) sont des outils utiles à garder à l’esprit pour une approche en toute confiance chez ces patients1. Souvent, l’explication est liée à l’une de ces causes.

Figure 4. L’acronyme SCALLP permet de se rappeler facilement les causes les plus courantes des démangeaisons du cuir chevelu (dermatite séborrhéique, dermatite de contact, anxiété, lichen plan pilaire, poux et psoriasis).
Source de l'image : Vázquez-Herrera NE, Sharma D, Aleid NM, Tosti A. Scalp Itch: A Systematic Review. Skin Appendage Disord. 2018;4(3):187-199. doi:10.1159/000484354
Il est également important de se rappeler que les démangeaisons du cuir chevelu peuvent être liées à plusieurs causes et que plusieurs types de lésions peuvent être présents. Cette classification est présentée ici :
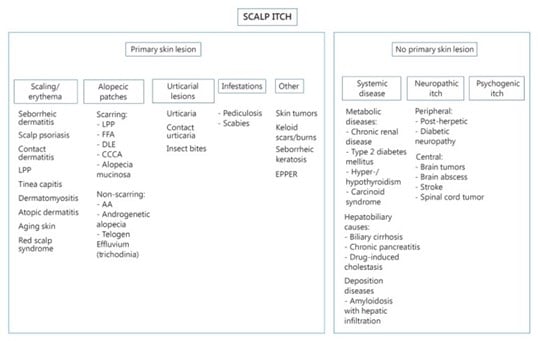
Figure 5. Algorithme face aux démangeaisons du cuir chevelu, d’après la présence ou l’absence de lésions cutanées primitives. LPP, lichen plan pilaire ; FFA, alopécie frontale fibrosante ; DLE, lupus érythémateux discoïde ; CCCA, alopécie cicatricielle centrifuge centrale ; EPPER, éruption à éosinophiles, polymorphe et prurigineuse associée à la radiothérapie ; AA, pelade.
Source de l'image : Vázquez-Herrera NE, Sharma D, Aleid NM, Tosti A. Scalp Itch: A Systematic Review. Skin Appendage Disord. 2018;4(3):187-199. doi:10.1159/000484354
Les affections les plus courantes qui s'accompagnent de démangeaisons du cuir chevelu et de lésions cutanées sont les suivantes :
D’autres lésions plus spécifiques peuvent être diagnostiquées cliniquement ou par biopsie : kératose séborrhéique, cicatrices chéloïdes, brûlures, éruptions à éosinophiles, polymorphes et prurigineuses associées à la radiothérapie (EPPER) et, rarement, tumeurs cutanées1.
Des démangeaisons du cuir chevelu (qui ne se limitent pas au cuir chevelu) associées à une maladie systémique peuvent être observées dans les cas suivants...
Maladies métaboliques :
Causes hépatobiliaires :
Paranéoplasiques :
Hématologie :
Infectieux :
Autres :
Les démangeaisons du cuir chevelu sans lésions cutanées peuvent être dues à un prurit neuropathique ou être psychogènes.
L’intervenant a ensuite proposé un traitement pour le prurit du cuir chevelu, en commençant par ces trois premières étapes :
L’intervenant a ensuite évoqué les médicaments susceptibles de soulager le prurit du cuir chevelu :
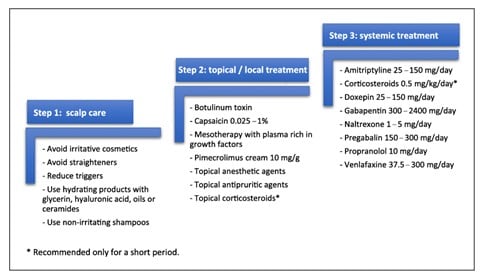
Figure 6. Traitements proposés dans la littérature face aux démangeaisons du cuir chevelu / cuirs chevelus sensibles, divisés en trois grandes catégories : soins du cuir chevelu, traitements topiques/locaux et traitements systémiques (par ordre alphabétique).
Source de l'image : Souza EN, Anzai A, Costa Fechine CO, Sakai Valente NY, Romiti R. Sensitive Scalp and Trichodynia: Epidemiology, Etiopathogenesis, Diagnosis, and Management. Skin Appendage Disord. 2023;9(6):407-415. doi:10.1159/000533795
Les dermatologues doivent impérativement connaître le prurit du cuir chevelu, car il précède ou accompagne souvent une maladie sous-jacente du cuir chevelu et peut servir d’indice clinique précoce en ce qui concerne les inflammations ou l’alopécie. En l’absence de traitement, les démangeaisons chroniques peuvent altérer considérablement la qualité de vie, perturber le sommeil et entraîner des excoriations ou une lichénification secondaires. Une compréhension approfondie de l’étiologie multifactorielle des démangeaisons du cuir chevelu, ainsi qu’une évaluation diagnostique ciblée et des stratégies de traitement personnalisées, sont essentielles pour une prise en charge efficace des patients et pour prévenir la progression de la maladie.
Littérature :
Compte rendu rédigé par le Dr Lidiya Todorova (dermatologue, Bulgarie)
Intervenante : Lidia Rudnicka, Pologne
La dermatite séborrhéique (DS) s’accompagne d’un large éventail de signes cliniques, allant d’une légère desquamation du cuir chevelu à des lésions inflammatoires avec desquamation. Alors que cette question faisait débat par le passé, tous les spécialistes présents au congrès de l’EHRS ont convenu que les pellicules font partie du spectre de la DS. Sur le plan clinique, elles constituent une forme non inflammatoire de DS associée à des signes de desquamation légère.
Selon le degré de sévérité, les caractéristiques de la DS à la trichoscopie sont les suivantes :
Un conseil précieux est de commencer par une trichoscopie à sec, seule capable de mettre en évidence la desquamation. Le liquide d’immersion permet ensuite d’observer les vaisseaux et l’inflammation du cuir chevelu, notamment :
Le psoriasis du cuir chevelu touche généralement 50 à 80 % des patients atteints de psoriasis, et chez environ 25 % d’entre eux, il s’agit de la première localisation du psoriasis. Cette localisation est souvent associée aux formes sévères de psoriasis. Les signes et caractéristiques à la trichoscopie de la maladie touchant le cuir chevelu sont les suivants :
Pour différencier la DS du psoriasis du cuir chevelu, les dermatologues doivent avoir ce tableau à l'esprit :
| Psoriasis du cuir chevelu | Dermatite séborrhéique |
| Squames blanches | Squames jaunâtres |
| Fond rose à rouge | Fond normal à rose |
| Disposition linéaire de groupes de vaisseaux en pointillés | Vaisseaux arborescents fins |
| Extravasations en pointillés |
Il n'existe actuellement aucune directive officielle pour le traitement du psoriasis du cuir chevelu, dans un contexte où le consensus européen date de 2009. Cependant, les conseils en matière de traitements sont les suivants :
L’analyse de la recherche présentée suggère que les inhibiteurs de l’interleukine 17 semblent être les plus efficaces face au psoriasis sévère du cuir chevelu.
Le professeur Rudnicka a également expliqué le phénomène de l’alopécie psoriasique, qui ne doit pas être oubliée lorsque l’on traite le psoriasis du cuir chevelu. L’alopécie psoriasique a été décrite comme un effet indésirable du traitement du psoriasis sévère par les anti-TNF (effet observé dans de rares cas après 2 à 46 mois de traitement). Ce type de perte de cheveux prend la forme d’une plaque d’alopécie associée à un psoriasis pustuleux ou en plaques sévère. Cette alopécie peut être non cicatricielle (70 %) ou cicatricielle (30 %). L’hypothèse suggérée est que les infiltrats inflammatoires périfolliculaires et l’atrophie progressive des glandes sébacées conduisent progressivement à une atteinte des follicules pileux et à une alopécie non cicatricielle, puis cicatricielle.
À la trichoscopie, l’alopécie psoriasique présente des caractéristiques variables de coexistence du psoriasis avec des signes d’effluvium anagène, d’effluvium télogène et d’alopécie cicatricielle, mais aussi des groupes de vaisseaux en disposition linéaire et des zones sans orifice folliculaire (points). Le traitement proposé est le changement de biothérapie.
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Rodrigo Pirmez, Brésil
Le lichen plan pilaire (LPP) est une affection inflammatoire chronique qui touche principalement le cuir chevelu et entraîne une alopécie cicatricielle. Le LPP étant caractérisé par une inflammation autour des follicules pileux, toutes les caractéristiques trichoscopiques se trouvent autour de ces derniers.
Les caractéristiques à la trichoscopie sont les suivantes :
Il est important de ne pas oublier la forme rare de LPP qui présente des caractéristiques d’alopécie androgénétique. L’observation d’une desquamation périfolliculaire chez un patient susceptible de présenter une AAG doit donc alerter et conduire à une biopsie du cuir chevelu afin d’exclure un LPP.

Figure 7. Prise en charge du lichen plan pilaire selon Pirmez. Bleu : traitement de première ligne ; bleu clair : traitements locaux en association avec un traitement oral - d’abord DC1, puis tacrolimus en relais ; jaune : traitement de soutien par minoxidil oral à tous les stades ; vert : traitement de deuxième ligne ; orange : traitement de troisième ligne et gris : autres traitements.
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Daniel Asz Sigall (Mexique) + à partir des affiches de Stelmaszek et al. et Soplinska et al.
L'alopécie par pression (AP) est un sous-type d’alopécie cicatricielle et non cicatricielle qui survient après une obstruction capillaire induite par la pression. L’hypoxie du bulbe capillaire entraîne une chute de cheveux dans des zones circonscrites. Deux types d’alopécies par pression ont été décrits : le type 1 (compression externe) et le type 2 (compression interne après l’injection d’un liquide dans le cadre d’un acte de médecine esthétique). Le type 1 se traduit par des plaques alopéciques sur les proéminences osseuses, tandis que le type 2 se manifeste à proximité de la zone d’injection, par exemple le cuir chevelu, la région temporale, le front ou la barbe.
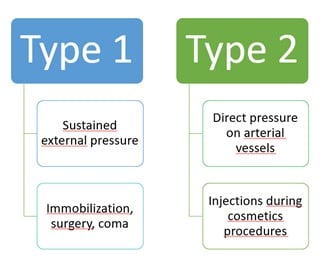
Dans le type 2, les signes et symptômes cliniques comprennent un érythème, un œdème, une douleur, une ulcération, une nécrose, puis une plaque irrégulière d’alopécie. La trichoscopie n'est pas spécifique et peut être semblable à une pelade, un lichen plan pilaire ou une trichotillomanie. Le pronostic est généralement excellent, mais dans certains cas, l’alopécie peut être définitive. Stelamaszek et al. ont rapporté le cas d’une femme de 30 ans qui présentait une plaque cicatricielle presque depuis la naissance, car elle était restée longtemps en couveuse après une naissance prématurée.
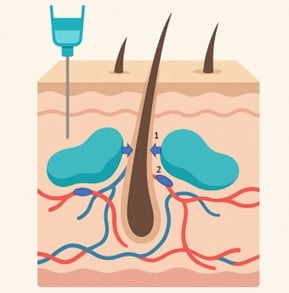
Figure 8. Physiopathologie de l’alopécie par pression de type 2 après injection cosmétique (produits de comblement...). 1. Pression mécanique 2. Thrombose vasculaire.
Compte rendu rédigé par le Dr Lidiya Todorova (dermatologue, Bulgarie)
Intervenante : Adriana Rakowska
L’alopécie du post-partum, également connue sous le nom d’effluvium télogène post-partum, est une forme de chute diffuse des cheveux qui est observée généralement 2 à 4 mois après l’accouchement et qui connaît une résolution spontanée. Cette alopécie survient quand les follicules pileux passent simultanément de la phase anagène (croissance) à la phase télogène (repos), sous l’effet des brusques changements hormonaux qui suivent l’accouchement, principalement la baisse du taux d’œstrogènes. Bien que physiologiquement normale, la perte soudaine et souvent dramatique des cheveux peut provoquer une détresse émotionnelle importante.
Le mécanisme physiopathologique de la chute des cheveux après l’accouchement réside dans l’arrêt à retardement de la phase anagène et dans les changements hormonaux pendant la grossesse. Cet arrêt à retardement de la phase anagène constitue une perturbation du cycle capillaire dans laquelle une phase anagène prolongée est suivie d’un passage synchronisé et prématuré d’un grand nombre de follicules pileux en phase télogène. Cela se traduit par une chute soudaine et diffuse des cheveux, généralement jusqu’à 2 à 4 mois après l’accouchement. Ce phénomène reflète une perturbation du cycle asynchrone normal des follicules pileux, et la chute de cheveux est généralement de résolution spontanée, les follicules revenant progressivement à la phase anagène.
Les changements hormonaux pendant la grossesse se traduisent par une quantité très élevée d’hormones : 9 fois plus de progestérone, 4 fois plus d’œstrone, 8 fois plus d’œstradiol, 9 fois plus d’œstriol et 20 fois plus de prolactine. Les véritables « méchants » responsables de la chute de cheveux sont la progestérone et la prolactine. En effet, la progestérone est responsable de l’allongement de la phase anagène, de l’augmentation du diamètre des tiges capillaires et de l’inhibition de la sécrétion d’androgènes. Résultat : au cours des deuxième et troisième trimestres, davantage de follicules du cuir chevelu sont en phase anagène. Cependant, après l’accouchement, la progestérone diminue considérablement et induit une phase catagène, tandis que les niveaux de prolactine restent élevés. La prolactine est alors responsable de l’induction de la phase catagène et de l’apoptose. D’après les estimations, le taux de prolactine revient à la normale 180 jours après l’accouchement et 7 jours après l’allaitement. Par conséquent, après ces intervalles, les follicules pileux sont très susceptibles d’entrer en phase télogène simultanément, avec un pic de chute des cheveux entre 3 et 6 mois après l’accouchement. À l’issue de cette période, la chute des cheveux tend à se normaliser et la repousse des cheveux est évidente avec une croissance quotidienne de 0,3 à 0,5 mm.
Les dermatologues sont souvent interrogés sur la possibilité de réduire la chute de cheveux en post-partum en interrompant rapidement l’allaitement chez les femmes concernées. Malheureusement, des études ont montré que le traitement hormonal substitutif n’était pas efficace face à la chute des cheveux après l’accouchement.
L’effluvium télogène post-partum (ETPP) peut-il induire une chute de cheveux par plaques chez la femme ? Malheureusement, oui. 75-84 % des patientes atteintes d’un ETPP présentent une chute de cheveux par plaques, auquel cas l’ETPP est plus sévère. Les grossesses peuvent également stimuler la chute de cheveux par plaques en cas de prédisposition génétique.
En outre, les dermatologues doivent être conscients des carences en fer après l’accouchement, carences qui peuvent entraîner une augmentation de l’effluvium télogène, mais aussi de la thyroïdite post-partum, qui survient chez 5 % des « jeunes mamans ».
L’intervenante a ensuite proposé une approche thérapeutique...
Le minoxidil oral à faible dose et la spironolactone peuvent également être envisagés, mais le finastéride, le dutastéride ou le bicalutamide ne doivent pas être proposés.
L’alopécie du post-partum est généralement bénigne et réversible, mais elle doit être différenciée d’autres formes de chutes de cheveux telles que l’alopécie androgénétique ou l’effluvium télogène dû à d’autres étiologies. Un diagnostic exact, l’information des patientes et une prise en charge de soutien (englobant notamment l’état nutritionnel, la santé du cuir chevelu et les pratiques de soins capillaires) sont essentiels pour réduire l’anxiété et éviter les actes et traitements inutiles. Dans certains cas, une chute de cheveux persistante peut révéler des troubles capillaires chroniques sous-jacents, ce qui souligne la nécessité d’un suivi attentif.
Littérature : Gizlenti S, Ekmekci TR. The changes in the hair cycle during gestation and the post-partum period. J Eur Acad Dermatol Venereol. 2014;28(7):878-881. doi:10.1111/jdv.12188
Compte rendu rédigé par le Dr Lidiya Todorova (dermatologue, Bulgarie)
Intervenante : Andy Goren, Italie
Le minoxidil, développé initialement en tant qu’antihypertenseur, est devenu une pierre angulaire dans la prise en charge de divers troubles associés à une perte de cheveux. Ainsi, le minoxidil topique est le seul médicament approuvé par la FDA pour le traitement de l’alopécie androgénétique (AAG) chez l’homme et la femme. Il favorise la croissance des cheveux en prolongeant la phase anagène, en augmentant la taille des follicules et en améliorant la circulation sanguine dans le cuir chevelu. Depuis quelques années, le minoxidil oral à faible dose est devenu une alternative prometteuse, hors AMM, en particulier chez les patients qui présentent une irritation du cuir chevelu ou une réponse sous-optimale aux traitements topiques.
Les études cliniques montrent que la réponse au minoxidil topique 5 % est généralement observée après 16 à 24 semaines de traitement. Les études démontrent également qu'après 4 semaines de traitement, il y a environ 30 à 40 % de répondeurs, c'est-à-dire de sujets dont les cheveux repoussent1.
Bien que le mécanisme d’action exact du minoxidil dans le traitement des chutes des cheveux chez la femme ne soit pas entièrement compris, la recherche a démontré que le sulfate de minoxidil est l’actif qui stimule les follicules pileux2. Le minoxidil est une prodrogue qui est transformée en sa forme active, le sulfate de minoxidil, dans la gaine radiculaire externe du follicule pileux par des enzymes sulfotransférases endogènes, principalement SULT1A12,3.
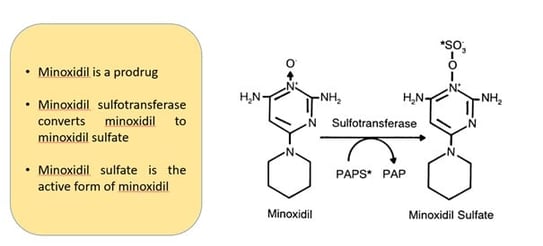
Figure 9. Mécanisme d’action du minoxidil : sulfatation du minoxidil catalysée par la sulfotransférase. PAPS* représente la [35S]-3’-phosphoadénosine5’-phosphosulfate et PAP représente la 3’-phosphoadénosine-5’-phosphate.
Source de l’image : Anderson, R. J., Kudlacek, P. E., & Clemens, D. L. (1998). Sulfation of minoxidil by multiple human cytosolic sulfotransferases. Chemico-Biological Interactions, 109(1-3), 53–67. doi:10.1016/s0009-2797(97)00120-8
Au vu de l’aspect chronophage du traitement et du faible taux de réponse, il serait intéressant de disposer d’un biomarqueur permettant de prédire la réponse en amont. L’activité des sulfotransférases dans le follicule pileux est un facteur prédictif important de la réponse au minoxidil chez les patients atteints d’une AAG. Le test d’activité enzymatique de la SULT1A1 présente une sensibilité de 95 % et une spécificité de 73 % pour prédire la réponse au traitement par minoxidil en cas d’AAG4.
Néanmoins, l’intervenant a indiqué que, d’après les études, 60 à 70 % des patients atteints d’une AAG ne répondent pas au minoxidil topique. C’est pourquoi il a posé la question de leur traitement.
La SULT1A1 est une enzyme cytosolique de métabolisme de phase II, qui est fortement exprimée dans le foie ainsi que, dans une moindre mesure, dans la peau et le cuir chevelu. La fonction première de cette enzyme est l’élimination des xénobiotiques. Elle sulfone les substances phénoliques, augmentant ainsi leur solubilité et leur élimination ultérieure au niveau des cellules. L’expression de l’enzyme SULT1A1 présente une corrélation positive avec l’expression du transporteur d’efflux de sulfate ABCC3, puisqu’une capacité de sulfonation accrue nécessite un transport d’efflux adéquat des groupements sulfonés. Le minoxidil topique est quant à lui une petite molécule qui pénètre facilement dans les kératinocytes, où elle est ensuite sulfonée, puis excrétée via le transporteur d’efflux ABCC3.
De son côté, le minoxidil oral est sulfoné par l’enzyme SULT1A1 dans le foie, si bien que la dose orale est éliminée à 80 % dans les urines dans les 30 minutes qui suivent l’ingestion. Par conséquent, une nouvelle voie inconnue est responsable de l’effet de repousse des cheveux associé au minoxidil oral. L’intervenant a ensuite présenté une étude portant sur 41 patients (26 hommes et 15 femmes), qui ont reçu respectivement 5 et 1,25 mg de minoxidil oral selon leur sexe. Après 6 mois de traitement, une amélioration clinique a été observée chez 26 patients, réponse qui était plus élevée chez les hommes (19/26) que chez les femmes (6/15). La densité visuelle des cheveux a été atteinte par 85 % des sujets.
Des études suggèrent également que le sulfate de minoxidil pénètre dans les cellules uniquement s’il est transporté activement par le transporteur d’influx SCL22A9. Or les cellules exprimant des niveaux élevés de SULT1A1 et du transporteur d’efflux de sulfate correspondant (ABCC3) ont tendance à exprimer des niveaux faibles du transporteur d’influx de sulfate SCL22A9. Ce phénomène est logique d’un point de vue biologique, car les cellules produisant de grandes quantités de groupements sulfonés doivent les éliminer plutôt que d’absorber des sulfates supplémentaires. Cependant, dans les cellules à faible activité sulfate, il est nécessaire d’améliorer le sulfate et donc d’augmenter l’expression du transporteur d’influx de sulfate SCL22A9. L’expression des transporteurs de ce médicament dans les reins varie en fonction du sexe. Cet aspect influence la pharmacocinétique du sulfate de minoxidil, car le transporteur d’influx de sulfate SCL22A9 a une expression plus élevée chez les hommes que chez les femmes. Cela pourrait expliquer que 40 % des femmes et 73 % des hommes aient répondu au minoxidil oral à faible dose en traitement de l’AAG.
Une étude portant sur l’impact des facteurs environnementaux a démontré que l’hypoxie augmente l’expression de SCL2A9 en diminuant celle des gènes ABCC3. Les changements de niveau des gènes du transporteur ABC en réponse à un environnement hypoxique peuvent contribuer à l’augmentation substantielle de l’expression de SCL2A9. À vrai dire, l’expression de SCL2A9 a été multipliée par 1,90 dans les cellules de cancer du sein exposées à une hypoxie comparativement aux cellules soumises à des conditions normoxiques. L’hépatotoxicité du paracétamol est principalement attribuée à la sulfonation. Pour contrer cette toxicité, la défériprone (déféroxamine) est fréquemment utilisée. Il a notamment été démontré que la déféroxamine, qui est un inducteur de HIF-alpha, régule à la hausse SCL22A9. La rifampicine, qui réduit SCL22A9, a été associée à une augmentation de la concentration plasmatique en sulfate de paracétamol et à un risque d’hépatotoxicité. Par conséquent, l’activité de l’enzyme SULT1A1 dans les follicules pileux arrachés sert de marqueur pour prédire la réponse au minoxidil oral à faible dose en traitement de l’AAG. Contrairement au minoxidil topique, une faible activité enzymatique de la SULT1A1 dans les follicules pileux permet de prédire la réponse à la forme orale. La voie HIF peut également être un mécanisme qui permet d’augmenter la réponse au minoxidil.
Il est de plus en plus important que les dermatologues connaissent les formes topiques et orales du minoxidil, car elles offrent des options thérapeutiques souples, bien tolérées et souvent synergiques face aux alopécies non cicatricielles. Les preuves de son efficacité et de son innocuité étant de plus en plus nombreuses, le minoxidil oral à faible dose (posologie pouvant descendre à 0,25-2,5 mg par jour) est utilisé chez davantage de patients, en particulier dans les cas difficiles à traiter et chez les patients préférant un traitement par voie orale. Il est essentiel de comprendre les indications, la posologie, les profils d’effets indésirables et les critères de sélection des patients pour les deux voies d’administration afin d’optimiser la repousse capillaire dans la pratique dermatologique.
Littérature :
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenants : Sergio Vañó-Galván (Espagne) et Yuliya S. Ovcharenko (Ukraine)
En ce qui concerne le cancer du sein, deux études récentes (une étude basée sur des données et une étude de cohorte rétrospective) ont montré que les inhibiteurs de la 5-alpha réductase administrés par voie orale n’étaient associés ni au cancer du sein ni aux tumeurs bénignes du sein. Ces résultats mettent en évidence la possibilité d’une utilisation hors AMM face aux chutes de cheveux chez la femme, avec un risque minime de cancer.
En Espagne, le consensus actuel du groupe espagnol de l’AEDV consacré à la trichologie, pour la prise en charge de l’alopécie androgénétique chez la femme est le suivant :
minoxidil oral à faible dose (0,5-1 mg/jour) ou topique à 5 %, en association avec de la spironolactone (100-200 mg/jour) ou des inhibiteurs de la 5-alpha-réductase (finastéride ou dutastéride).
En 2012, le syndrome post-finastéride (SPF) a fait son apparition. Il s’agissait alors d’une affection controversée signalée par certains patients après l’arrêt du finastéride, utilisé pour le traitement de la calvitie masculine. Les symptômes comprenaient initialement des dysfonctions sexuelles (troubles de l’érection, baisse de libido...). Lorsque ce SPF a été rendu public, les rapports de pharmacovigilance sur les problèmes de santé mentale (dépression, anxiété) et les suicides associés à la finastéride ont augmenté. Le SPF se caractérise par des dysfonctions sexuelles, des symptômes somatiques et des troubles psychologiques qui persistent après l'arrêt du traitement par finastéride.
L’hypothèse serait que l’inhibition de l’enzyme 5α-réductase par le finastéride entraîne une diminution des niveaux d’allopregnanolone, qui a des effets antidépresseurs et anxiolytiques.
L’analyse de VigiBase (base de données mondiale de l’OMS sur les effets indésirables rapportés en lien avec les médicaments et vaccins) a montré que 356 suicides et 2 926 effets indésirables psychologiques ont été rapportés chez les patients prenant du finastéride, en sachant que 70,9 % des personnes pour lesquelles des données étaient disponibles étaient âgées de 18 à 44 ans. Ces données ont montré une disproportionnalité significative entre les suicides (odds ratio 1,63 ; IC 95 %, 1,47-1,81 pour les idées suicidaires) et les effets indésirables psychologiques (odds ratio 4,33 ; IC 95 %, 4,17-4,49) rapportés sous finastéride. Il est important de souligner qu’à la fois les professionnels de santé, que ce soient les médecins, les pharmaciens et le personnel infirmier, et les patients peuvent signaler les effets indésirables présumés des médicaments dans Vigibase.
Dans les analyses de sensibilité, les patients jeunes atteints d’alopécie androgénétique (AAG) présentaient une disproportionnalité significative en ce qui concerne le risque de suicide, phénomène qui n’était pas détecté chez les patients âgés atteints d’hypertrophie bénigne de la prostate. Les analyses de sensibilité ont également montré que le signalement de ces effets indésirables a significativement augmenté après 2012, période où des cas d’hommes ayant utilisé le finastéride et ayant tenté de se suicider ou s’étant suicidés ont commencé à être rapportés.
Par ailleurs, il est important de souligner qu’aucune problématique suicidaire n’a été observée en lien avec le dutastéride, médicament dont le mécanisme d’action est similaire à celui du finastéride, mais qui n'a pas attiré autant l’attention des médias. À noter également l’absence d’association dose-réponse avec le finastéride, ce qui suggère un biais de signalement potentiel propre au finastéride.
Une revue systématique et une méta-analyse de 5 études portant sur 2 213 600 patients (228 453 patients sous inhibiteurs de la 5-alpha réductase et 1 985 147 témoins) n’a révélé aucune association significative entre l’utilisation des inhibiteurs de la 5-alpha réductase et le risque de dépression ou de suicide, y compris à la posologie de 1 mg/jour couramment prescrite face à l’alopécie.
Le comité pour l’évaluation des risques en matière de pharmacovigilance de l’EMA a malgré tout récemment déclaré que les idées suicidaires sont un effet indésirable des comprimés de finastéride chez les patients utilisant la posologie de 1 mg en traitement de l’alopécie androgénétique, bien que la fréquence ne soit pas connue.
Malgré ces mises en garde, les bénéfices du finastéride et du dutastéride continuent de dépasser les risques pour les utilisations approuvées.
Il est à noter que certains spécialistes des cheveux recommandent de vérifier les antécédents personnels ou de dépister les problèmes de santé mentale préexistants afin de sélectionner rigoureusement les patients qui sont mis sous finastéride, puisque ces critères peuvent exposer les patients à un risque accru de troubles psychologiques, tels que la dépression, et de somatisation, tels que le SPF (Trüeb RM, Gavazzoni Dias MFR, Dutra Rezende H. Suicidality and Psychological Adverse Events in Patients Treated with Finasteride. Skin Appendage Disord. 2021 Nov;7(6):524-526)

Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Rodrigo Pirmez, Brésil
Il existe actuellement peu de publications sur la prise en charge des chutes de cheveux chez les personnes transgenres. Pour rappel, un homme transgenre est une personne à qui l’on a attribué le sexe féminin à la naissance, mais qui s’identifie au genre masculin. Les hommes transgenres peuvent choisir de suivre un traitement hormonal masculinisant (THM ; testostérone) et/ou de subir des chirurgies de masculinisation. Une femme transgenre est une personne à qui l’on a attribué le sexe masculin à la naissance, mais qui s’identifie au genre féminin. Chez ces femmes, le traitement hormonal féminisant (THF) comprend des œstrogènes et des anti-androgènes. Les femmes transgenres peuvent également subir des interventions chirurgicales de féminisation.
D’après l’expérience de l’intervenant, l’alopécie androgénétique (AAG) est le 6e motif de consultation dans sa clinique au Brésil, soit 7,5 % des consultations, après l’acné (29 %), les actes cosmétiques (27,1 %), les kystes (11,2 %), la pseudofolliculite de la barbe (10,3 %) et les cicatrices d’acné (9,3 %).
L’AAG chez les hommes transgenres
L’AAG apparaît un à cinq ans après le THM (mise en place de la testostérone), même si des modifications capillaires sont parfois observées après 6 mois (diminution du diamètre des cheveux). L’AAG touche 17 % des hommes transgenres sans THM et 43 à 60 % des hommes transgenres sous THM. Les antécédents familiaux d’AAG et la durée du THM sont les principaux facteurs de risque de l’AAG.
Le traitement comprend le minoxidil 2,5 à 5 mg par jour, comme pour les hommes cisgenres. La posologie plus élevée est bien acceptée, car elle augmente également le nombre de poils sur le corps. Le finastéride 1 mg/jour peut être prescrit en association avec le minoxidil. Cependant, il est recommandé de commencer le finastéride seulement un à deux ans après le début du THM. La première raison est que l’AAG est d’apparition tardive ; deuxièmement, il existe des questions concernant l’impact d’une mise en place précoce d’un inhibiteur de la 5-alpha réductase sur la pilosité faciale et corporelle et sur l’hypertrophie clitoridienne. La place du dutastéride n’est pas connue (en cas d’échec du finastéride ?). La spironolactone est contre-indiquée chez les hommes transgenres. Enfin, les hommes transgenres qui n’ont pas subi de chirurgie doivent avoir recours à une contraception, car la testostérone ne prévient pas la grossesse.
En ce qui concerne la pousse de la barbe chez les hommes transgenres, les poils du visage commencent à apparaître après seulement 3 mois. Cependant, il existe des différences entre les individus et tous n’ont pas une barbe bien fournie. Le minoxidil topique ou oral peut être utilisé. Enfin, des greffes de poils sur le visage sont possibles.
L’AAG chez les femmes transgenres
Le THF (œstrogènes et anti-androgènes) peut stopper la progression de l’AAG chez les femmes transgenres, voire la faire régresser. La prise en charge de l’AAG chez les femmes transgenres atténue la dysphorie de genre et améliore la qualité de vie. Si nécessaire, la spironolactone 50-200 mg/j en association avec du minoxidil oral peut être utilisée. Le minoxidil oral doit être maintenu à une faible dose, de l’ordre de 0,5 mg/jour, pour éviter la dysphorie de genre (sous l’effet d’une augmentation de la pilosité corporelle). Des interventions chirurgicales telles que la greffe de cheveux ou l’avancement du cuir chevelu peuvent également être proposées.
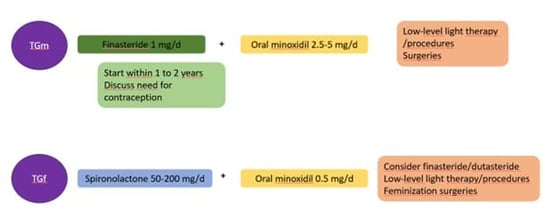
Figure 10. Résumé de la prise en charge de l’AAG chez les personnes transgenres selon Pirmez (TGf : femmes transgenres ; TGm : hommes transgenres).
Compte rendu rédigé par le Dr Nicolas Kluger (dermatologue, Finlande)
Intervenante : Arash Mostaghimi, États-Unis
Le Prof. Mostaghimi a présenté une étude publiée dans JAMA Dermatology 2021, qui évaluait la prévalence et l’ampleur de la stigmatisation, par le grand public, des personnes atteintes d’alopécie à divers degrés. Cette étude cherchait par ailleurs à savoir si cette stigmatisation augmentait avec la gravité de l’alopécie (Creadore A, Manjaly P, Li SJ, Tkachenko E, Zhou G, Joyce C, Huang KP, Mostaghimi A. Evaluation of Stigma Toward Individuals with Alopecia. JAMA Dermatol. 2021 Apr 1;157(4):392-398, consultable gratuitement https://pmc.ncbi.nlm.nih.gov/articles/PMC7948115/)
Les auteurs ont généré des images par IA à partir de portraits libres de droits de 6 personnes sans perte de cheveux. Chaque portrait était modifié de manière à créer deux versions supplémentaires : l’une avec une calvitie et l’autre avec une perte complète des cheveux et de la pilosité, pour un total de 18 images. Une enquête a ensuite été réalisée sur Internet auprès de 2 015 personnes. L’enquête comprenait une série de questions relatives à la stigmatisation dans trois domaines : les stéréotypes, la distance sociale et les mythes liés à la maladie (afin de savoir si les personnes interrogées pensaient que la personne photographiée souffrait d’une maladie).
Plus la sévérité de l’alopécie augmentait, plus les personnes interrogées étaient nombreuses à approuver chaque stéréotype et chaque élément de distance sociale. Les augmentations les plus importantes autour des stéréotypes concernaient les qualificatifs de « malade » (augmentation de 27,6 %) et « peu attirant » (augmentation de 16,5 %) dans le cas d’une perte totale des cheveux et de la pilosité. En ce qui concerne la distance sociale, les changements les plus importants étaient une augmentation de 18,3 % du désaccord avec l’affirmation « Je trouverais la personne sur cette photo attirante » et une augmentation de 6,9 % du désaccord avec l’affirmation « Cela ne me dérangerait pas d’avoir un contact physique avec la personne sur cette photo ».
Le degré d’augmentation de la stigmatisation entre la version originale et la version présentant une perte totale des cheveux et de la pilosité dépendait de la couleur de peau et du sexe de la personne représentée. Dans toutes les catégories de portraits, une alopécie plus sévère était associée à une plus grande conviction que la personne photographiée souffrait d’un problème de santé. Ces résultats suggèrent que le grand public peut stigmatiser les personnes atteintes d’alopécie, que cette stigmatisation augmente avec la gravité de l’alopécie et qu'elle peut être influencée par les origines ethniques et le sexe.

Figure 11. Échantillon de portraits générés par ordinateur et 2 versions présentant différents degrés d’alopécie.
Source des images : Creadore A, Manjaly P, Li SJ, Tkachenko E, Zhou G, Joyce C, Huang KP, Mostaghimi A. Evaluation of Stigma Toward Individuals With Alopecia. JAMA Dermatol. 2021 Apr 1;157(4):392-398)
Créez en toute simplicité votre compte professionnel
Je crée mon compteAméliorez vos connaissances professionnelles en profitant de nombreux services exclusifs dans le domaine de la dermatologie : plus de 500 visuels de pathologies, des cas cliniques, des vidéos d’experts…
Bénéficiez d’options uniques telles que l’offre de contenus audio et de supports à proposer à vos patients.
Restez informé(e) des événements et des webinaires à venir, des dernières publications scientifiques et des innovations produit.