2 professionals
Bioderma Congress Reports JNPD 2026
Bioderma Congress Reports JNPD 2026
Comptes rendus rédigés par Joséfina MARCO-BONNET (Dermatologue à Montrouge) et Camille LOISEAU (Interne en Dermatologie à Lille)
Sujets liés
Rédigé par Dr Camille LOISEAU (Interne en Dermatologie à Lille)
Par Pr Marie Beylot-Barry
Classification pratique et démarche diagnostique
La classification des lymphomes cutanés est complexe et régulièrement actualisée, mais des approches simplifiées permettent une utilisation pratique en clinique. Le mycosis fongoïde représente la forme la plus fréquente et se manifeste classiquement par des plaques bien limitées, avec des variantes cliniques incluant les formes folliculotropes, tumorales ou érythrodermiques. Le syndrome de Sézary correspond à une forme plus avancée avec atteinte sanguine.
La démarche diagnostique est standardisée, mais le bilan d’extension doit être adapté au stade cutané. Dans les formes limitées, une évaluation clinique seule est suffisante et il est important de savoir ne pas prescrire d’examens complémentaires inutiles. À l’inverse, les formes plus avancées nécessitent un bilan complet incluant imagerie, biologie et exploration sanguine spécialisée. L’immunophénotypage sanguin doit être réalisé dans des structures adaptées et comparé à la clonalité cutanée. Une biopsie ganglionnaire peut être discutée, tandis que la biopsie ostéomédullaire n’est pas recommandée.
Les autres lymphomes cutanés comprennent des formes indolentes, comme les lymphoproliférations CD30 ou les lymphomes B de bas grade, et des formes plus agressives, comme certains lymphomes T cytotoxiques ou les lymphomes B à grandes cellules.
Focus sur les lymphoproliférations T CD4+ à petites et moyennes cellules
Les lymphoproliférations T CD4+ à petites et moyennes cellules constituent une entité de plus en plus reconnue en pratique clinique. Elles se présentent le plus souvent sous la forme d’un nodule solitaire, fréquemment localisé au visage, pouvant évoquer un carcinome ou une autre tumeur cutanée. Après biopsie, une régression spontanée est souvent observée.
L’examen histologique montre un infiltrat mixte riche en lymphocytes T et B, avec expression de marqueurs de type T helper folliculaire. Une clonalité T est fréquemment détectée en biologie moléculaire. Le pronostic est excellent et la prise en charge repose sur un bilan d’extension minimal et des traitements locaux simples, comme les dermocorticoïdes, l’exérèse ou une radiothérapie à faible dose(1,2). Une surveillance clinique est généralement suffisante, et il est essentiel de rassurer les patients. Cette entité est aujourd’hui considérée comme proche d’un pseudolymphome, bien que des formes multiples nécessitent une attention particulière.
Lymphomes cutanés de l’enfant
Les lymphomes cutanés peuvent débuter dans l’enfance, notamment sous forme de mycosis fongoïde, bien que cela reste rare. Les présentations cliniques sont souvent particulières, avec des formes hypopigmentées, folliculotropes et des stades précoces prédominants.
La prise en charge repose sur un bilan simple comprenant un examen clinique, une biopsie cutanée et un bilan biologique. En cas de nécessité, une échographie ganglionnaire est préférée aux examens irradiants. Le traitement est adapté à l’âge et au caractère indolent de la maladie, reposant principalement sur les dermocorticoïdes et la photothérapie UVB. Le pronostic est globalement excellent, même si des récidives peuvent survenir. Les données de cohortes montrent une survie prolongée avec très peu de décès (3,4).
Les papuloses lymphomatoïdes sont également fréquentes chez l’enfant et ont une évolution similaire à celle observée chez l’adulte (5,6).
Actualités thérapeutiques
Dans les formes précoces, les lymphomes cutanés doivent être considérés comme des maladies chroniques. L’objectif thérapeutique est de contrôler les lésions et d’améliorer la qualité de vie tout en limitant la toxicité des traitements. Une rémission complète est possible, mais la persistance de lésions minimes est acceptable et ne doit pas conduire à une escalade thérapeutique injustifiée.
Dans les formes avancées, l’allogreffe de cellules souches hématopoïétiques représente actuellement le seul traitement potentiellement curatif. Les données récentes confirment son efficacité en termes de survie prolongée, malgré des risques non négligeables liés à la procédure (7). Cette option est réservée à des patients sélectionnés, en fonction de leur âge, de leurs comorbidités et de la disponibilité d’un donneur.
Le mogamulizumab constitue une avancée thérapeutique importante, notamment dans le syndrome de Sézary. Ce traitement agit à la fois sur les cellules tumorales et les lymphocytes T régulateurs, permettant des réponses rapides et prolongées, en particulier sur l’atteinte sanguine. Des rémissions complètes durables ont été observées, parfois même après l’arrêt du traitement (8). Toutefois, ce traitement expose à des effets indésirables auto-immuns qui nécessitent une surveillance attentive.
Lymphomes « masqués » et biothérapies
Certains lymphomes cutanés peuvent mimer des dermatoses inflammatoires fréquentes telles que le psoriasis, l’eczéma du sujet âgé, le vitiligo ou certaines dermatoses pigmentées. Cette proximité clinique complique parfois le diagnostic.
Des cas de lymphomes cutanés ont été rapportés chez des patients traités par dupilumab, principalement des mycosis fongoïdes ou des syndromes de Sézary (9). Dans la majorité des situations, il s’agit d’une aggravation de lésions préexistantes ou de formes initialement méconnues. Le dupilumab semble ainsi jouer un rôle de révélation plutôt que d’induction.
Une vigilance particulière est recommandée chez les patients présentant une dermatite atopique d’apparition tardive, sans antécédents atopiques ou avec des localisations atypiques. Dans ces cas, une biopsie cutanée doit être discutée. En cas de doute diagnostique, certaines thérapeutiques comme les inhibiteurs de JAK ou la ciclosporine doivent être évitées, tandis que le méthotrexate peut être envisagé.
Conclusion
Les lymphomes cutanés constituent un ensemble hétérogène de pathologies nécessitant une approche diagnostique et thérapeutique adaptée à chaque situation. Les avancées récentes permettent une meilleure caractérisation de certaines entités indolentes et une amélioration des options thérapeutiques dans les formes avancées. La prise en charge repose sur une collaboration multidisciplinaire, une information claire des patients et une attention particulière aux diagnostics différentiels. L’objectif reste d’assurer un équilibre optimal entre efficacité thérapeutique et qualité de vie.
Références
1. Willemze R, Assaf C, Bagot M, Beylot-Barry M, Berti E, Busschots AM, et al. European Organisation for Research and Treatment of Cancer, United States Cutaneous Lymphoma Consortium and International Society for Cutaneous Lymphomas consensus recommendations for management and treatment of cutaneous lymphoproliferative disorders. Br J Dermatol. 18 nov 2025;193(6):1090‑100. doi:10.1093/bjd/ljaf312 PubMed PMID: 40795052.
2. Bashall SEL, Thomas BR, Sim V, Wain M, Child F, Whittaker S, et al. Primary cutaneous CD4+ small/medium T-cell lymphoproliferative disorder: 20 years of experience from a specialist centre. Br J Dermatol. 18 nov 2025;193(6):1214‑20. doi:10.1093/bjd/ljaf338 PubMed PMID: 40920577.
3. Welfringer-Morin A, Barroil M, Fraitag S, Szablewski V, Boccara O, Lacour JP, et al. Clinical Features, Histological Characteristics, and Disease Outcomes of Mycosis Fungoides in Children and Adolescents: A Nationwide Multicentre Cohort of 46 Patients. Dermatology. 2023;239(1):132‑9. doi:10.1159/000526788 PubMed PMID: 36349768.
4. Lohray R, Purnak S, Huen A, Duvic M, Dai J. Long-term outcomes in juvenile-onset mycosis fungoides. J Am Acad Dermatol. 2 mars 2026;S0190-9622(26)00320-8. doi:10.1016/j.jaad.2026.02.095 PubMed PMID: 41780598.
5. Alberti-Violetti S, Avallone G, Colonna C, Tavoletti G, Venegoni L, Merlo V, et al. Paediatric cutaneous lymphomas including rare subtypes: A 40-year experience at a tertiary referral centre. J Eur Acad Dermatol Venereol. janv 2025;39(1):161‑70. doi:10.1111/jdv.20028 PubMed PMID: 38650545; PubMed Central PMCID: PMC11664474.
6. Blanchard M, Morren MA, Busschots AM, Hauben E, Alberti-Violetti S, Berti E, et al. Paediatric-onset lymphomatoid papulosis: results of a multicentre retrospective cohort study on behalf of the EORTC Cutaneous Lymphoma Tumours Group (CLTG). Br J Dermatol. 16 juill 2024;191(2):233‑42. doi:10.1093/bjd/ljae150 PubMed PMID: 38595050.
7. de Masson A, Beylot-Barry M, Ram-Wolff C, Mear JB, Dalle S, d’Incan M, et al. Allogeneic transplantation in advanced cutaneous T-cell lymphomas (CUTALLO): a propensity score matched controlled prospective study. Lancet. 10 juin 2023;401(10392):1941‑50. doi:10.1016/S0140-6736(23)00329-X PubMed PMID: 37105210.
8. Kim YH, Bagot M, Pinter-Brown L, Rook AH, Porcu P, Horwitz SM, et al. Mogamulizumab versus vorinostat in previously treated cutaneous T-cell lymphoma (MAVORIC): an international, open-label, randomised, controlled phase 3 trial. Lancet Oncol. sept 2018;19(9):1192‑204. doi:10.1016/S1470-2045(18)30379-6 PubMed PMID: 30100375.
9. Amatore F, Neildez M, de Masson A, Battistella M, Tauber M, Ingen-Housz-Oro S, et al. Cutaneous T-cell lymphomas and dupilumab for atopic dermatitis: A systematic review and expert consensus. J Eur Acad Dermatol Venereol. 12 mars 2026. doi:10.1111/jdv.70407 PubMed PMID: 41821352.
Rédigé par Dr Camille LOISEAU (Interne en Dermatologie à Lille)
Par Pr Mahtab Samimi
Épidémiologie et registres
Le carcinome de Merkel est une tumeur cutanée rare dont la compréhension repose largement sur des bases de données dédiées. La base nationale CARADERM, qui recense les cancers cutanés rares, constitue un outil essentiel pour améliorer les connaissances sur cette pathologie. En 2025, plus de 2000 patients atteints de carcinome de Merkel y sont inclus, ce qui en fait l’une des plus grandes cohortes décrites dans la littérature et permet une meilleure caractérisation des aspects cliniques et évolutifs de la maladie.
Caractéristiques cliniques et physiopathologie
Le carcinome de Merkel est classiquement décrit comme une tumeur survenant sur des zones photo-exposées chez des sujets âgés, notamment au niveau de la tête et du cou. Toutefois, les données récentes montrent que cette présentation ne concerne qu’une minorité des cas et qu’environ 80 % des carcinomes de Merkel sont liés au polyomavirus de Merkel plutôt qu’à l’exposition solaire. Ainsi, des localisations non photo-exposées sont fréquemment observées, notamment au niveau des membres, du tronc, des fesses ou encore des organes génitaux externes. Par ailleurs, environ 10 % des cas correspondent à des formes à primitif cutané occulte, se révélant par une atteinte ganglionnaire isolée sans lésion cutanée identifiée.
Dermoscopie
Les données issues d’une étude internationale menée par Korecka et al. (1) et s’intéressant à la dermoscopie ont permis de mieux décrire les caractéristiques de cette tumeur, bien que celles-ci restent peu spécifiques. Les lésions de carcinome de Merkel présentent le plus souvent une coloration rose ou rouge laiteuse, associée à des structures blanches brillantes et à des vaisseaux linéaires irréguliers. Des squames ou des ulcérations peuvent également être observées mais de façon moins fréquente. Aucun de ces critères n’étant discriminant, le diagnostic dermoscopique reste difficile et nécessite une confirmation histologique.
Prise en charge des formes localisées
Le traitement des carcinomes de Merkel localisés repose sur une approche combinée associant chirurgie et radiothérapie. La chirurgie consiste en une exérèse avec des marges latérales d’un centimètre, les marges plus larges n’étant plus recommandées. Cette stratégie est rendue possible par l’utilisation systématique d’une radiothérapie adjuvante, en raison de la forte radiosensibilité de la tumeur. La radiothérapie doit être initiée rapidement après la chirurgie, idéalement dans un délai de huit semaines, afin d’optimiser le contrôle local. Des approches de désescalade thérapeutique, notamment avec des schémas de radiothérapie en une seule séance, sont actuellement à l’étude chez des patients sélectionnés.
La réalisation d’un ganglion sentinelle est recommandée chez les patients éligibles, bien que cette procédure soit encore insuffisamment réalisée en pratique. En cas de micrométastase ganglionnaire, une radiothérapie est généralement proposée, même en l’absence de preuve formelle de bénéfice sur le pronostic. En présence de métastases ganglionnaires macroscopiques, un curage ganglionnaire est indiqué, éventuellement complété par une radiothérapie en fonction des facteurs de risque.
Immunothérapie adjuvante
L’intérêt de l’immunothérapie (nivolumab/pembrolizumab) en situation adjuvante a été évalué dans deux essais randomisés récents (2,3). Ces études montrent une amélioration de la survie sans récidive chez les patients traités par immunothérapie, bien que les résultats ne soient pas statistiquement significatifs, probablement en raison d’effectifs limités. Une amélioration significative de la survie sans métastase à distance a toutefois été observée dans l’étude de Mehnert el al., ce qui constitue un élément cliniquement pertinent. En l’absence de données robustes et de démonstration d’un bénéfice sur la survie globale, cette stratégie n’est pas encore intégrée dans les recommandations, mais peut être discutée au cas par cas chez des patients à haut risque de récidive.
Approche néoadjuvante
L’immunothérapie administrée avant la chirurgie a été évaluée dans de petites études de phase II (4,5), montrant qu’environ la moitié des patients obtiennent une réponse complète pathologique. Ce type de réponse est associé à un excellent contrôle de la maladie à long terme. Bien que cette approche soit mentionnée dans les recommandations américaines, elle n’est pas encore validée en Europe en raison du faible niveau de preuve et de l’absence d’études comparatives.
Formes avancées et métastatiques
Dans les formes avancées non opérables, l’immunothérapie par anti-PD-1 ou anti-PD-L1 (avelumab) constitue le traitement de référence. Environ la moitié des patients répondent à ce traitement, avec des réponses souvent durables. La durée optimale du traitement reste toutefois incertaine, car l’arrêt de l’immunothérapie expose à un risque de progression d’environ 40 %, en particulier chez les patients n’ayant pas obtenu de réponse complète (6,7). En revanche, chez les patients en réponse complète prolongée, le risque de rechute est nettement plus faible (8,9), ce qui permet d’envisager un arrêt du traitement dans certaines situations.
En cas d’échec de la monothérapie, la combinaison d’ipilimumab et de nivolumab peut être proposée, avec un taux de réponse d’environ 30 %, au prix d’une toxicité plus importante (10,11). Cette stratégie est actuellement réservée aux situations de résistance, et son utilisation en première ligne n’est pas recommandée en l’absence de données solides et en raison du risque accru d’effets indésirables.
Métastases cérébrales
Les métastases cérébrales sont rares au diagnostic initial du carcinome de Merkel et ne justifient pas la réalisation systématique d’une imagerie cérébrale à ce stade. En revanche, chez les patients atteints de maladie métastatique, elles surviennent dans environ 7 % des cas, le plus souvent de manière secondaire et asymptomatique (12). Elles peuvent apparaître malgré une réponse systémique complète, ce qui justifie un suivi régulier par IRM cérébrale chez les patients de stade IV.
Le traitement repose principalement sur l’association d’une immunothérapie et d’une radiothérapie stéréotaxique, qui semble offrir les meilleurs résultats. En cas de progression, une intensification thérapeutique par double immunothérapie peut être envisagée.
Conclusion
Le carcinome de Merkel est une tumeur rare mais agressive dont la prise en charge a considérablement évolué ces dernières années. Les données issues de registres nationaux et les avancées en immunothérapie ont permis d’améliorer la compréhension et le traitement de cette maladie. Si la chirurgie et la radiothérapie restent les piliers des formes localisées, l’immunothérapie occupe désormais une place centrale dans les formes avancées. Les stratégies adjuvantes et néoadjuvantes apparaissent prometteuses, mais nécessitent encore des validations complémentaires. La gestion des résistances thérapeutiques et des localisations cérébrales constitue un enjeu majeur pour les années à venir.
Références
1. Korecka K, Badiu IM, Tschandl P, Akay BN, Apalla Z, Hofmann-Wellenhof R, et al. Dermoscopy in Merkel Cell Carcinoma—A Multicenter Retrospective Study of the International Dermoscopy Society. International Journal of Dermatology. n/a(n/a). doi:10.1111/ijd.70213
2. Becker JC, Ugurel S, Leiter U, Meier F, Gutzmer R, Haferkamp S, et al. Adjuvant immunotherapy with nivolumab versus observation in completely resected Merkel cell carcinoma (ADMEC-O): disease-free survival results from a randomised, open-label, phase 2 trial. Lancet. 2 sept 2023;402(10404):798‑808. doi:10.1016/S0140-6736(23)00769-9 PubMed PMID: 37451295.
3. Mehnert JM, Lee SJ, Gastman B, Hsu C, Cohen G, Eicher DM, et al. LBA56 ECOG-ACRIN EA6174: STAMP: Surgically treated adjuvant merkel cell carcinoma with pembrolizumab, a phase III trial. Annals of Oncology. sept 2025;36:S1600. doi:10.1016/j.annonc.2025.09.068
4. Topalian SL, Bhatia S, Amin A, Kudchadkar RR, Sharfman WH, Lebbé C, et al. Neoadjuvant Nivolumab for Patients With Resectable Merkel Cell Carcinoma in the CheckMate 358 Trial. J Clin Oncol. août 2020;38(22):2476‑87. doi:10.1200/JCO.20.00201
5. Brohl AS, Sondak VK, Wuthrick EJ, Kim Y, Eroglu Z, Markowitz J, et al. Neoadjuvant lenvatinib plus pembrolizumab in Merkel cell carcinoma: an investigator-initiated, open-label phase II trial. J Immunother Cancer. 14 janv 2026;14(1):e013939. doi:10.1136/jitc-2025-013939 PubMed PMID: 41534900; PubMed Central PMCID: PMC12815050.
6. Weppler AM, Da Meda L, Pires da Silva I, Xu W, Grignani G, Menzies AM, et al. Durability of response to immune checkpoint inhibitors in metastatic Merkel cell carcinoma after treatment cessation. Eur J Cancer. avr 2023;183:109‑18. doi:10.1016/j.ejca.2023.01.016 PubMed PMID: 36842413.
7. Ramadoss T, Nichols M, Palacios C, Eroglu Z, Markowitz J, Karapetyan L, et al. Durability of response to immune checkpoint blockade following treatment discontinuation and efficacy of rechallenge in advanced Merkel cell carcinoma. J Immunother Cancer. 5 sept 2024;12(9):e009816. doi:10.1136/jitc-2024-009816 PubMed PMID: 39242118; PubMed Central PMCID: PMC11381633.
8. Zijlker LP, Levy S, Wolters W, van Thienen JV, van Akkooi ACJ, Tesselaar MET. Avelumab treatment for patients with metastatic Merkel cell carcinoma can be safely stopped after 1 year and a PET/CT-confirmed complete response. Cancer. 1 févr 2024;130(3):433‑8. doi:10.1002/cncr.35050 PubMed PMID: 37788133.
9. Tachiki L, Moshiri Y, Hippe DS, Gong E, Zawacki L, Pulliam T, et al. Risk of disease progression after discontinuing immunotherapy in 105 patients with Merkel cell carcinoma who responded to PD-1 pathway blockade. J Immunother Cancer. 11 août 2025;13(8):e012123. doi:10.1136/jitc-2025-012123 PubMed PMID: 40789739; PubMed Central PMCID: PMC12352153.
10. Akaike T, Jabbour AJ, Goff PH, Park SY, Bhatia S, Nghiem P. Merkel cell carcinoma refractory to anti-PD(L)1: utility of adding ipilimumab for salvage therapy. J Immunother Cancer. 24 juill 2024;12(7):e009396. doi:10.1136/jitc-2024-009396 PubMed PMID: 39053946; PubMed Central PMCID: PMC11284820.
11. Kim S, Wuthrick E, Blakaj D, Eroglu Z, Verschraegen C, Thapa R, et al. Combined nivolumab and ipilimumab with or without stereotactic body radiation therapy for advanced Merkel cell carcinoma: a randomised, open label, phase 2 trial. The Lancet. 24 sept 2022;400(10357):1008‑19. doi:10.1016/S0140-6736(22)01659-2 PubMed PMID: 36108657.
12. Caillot R, Blom A, Lebbé C, Da Meda L, Boileau M, Dutriaux C, et al. Brain metastases from Merkel cell carcinoma: A nationwide retrospective study. Eur J Cancer. 9 sept 2025;227:115637. doi:10.1016/j.ejca.2025.115637 PubMed PMID: 40712254.
Rédigé par Dr Camille LOISEAU (Interne en Dermatologie à Lille)
Par Dr Caroline Dutriaux
Les recommandations européennes EADO/EORTC 2024 (1) constituent une base essentielle pour la prise en charge du mélanome. Elles permettent d’orienter la réflexion clinique et d’harmoniser les pratiques, en particulier dans les stades précoces, qui sont les plus fréquemment rencontrés.
Mélanome de stade précoce (stade I)
La prise en charge des mélanomes de stade IA repose sur une reprise chirurgicale avec des marges de 1 cm. Une échographie ganglionnaire est recommandée et le dossier peut être discuté en réunion de concertation pluridisciplinaire.
La question du ganglion sentinelle se pose principalement pour les formes pT1B. Les recommandations européennes et françaises autorisent sa réalisation en option, mais cette décision doit être réfléchie. En effet, la réalisation d’un ganglion sentinelle implique d’envisager un traitement adjuvant en cas de positivité. Cette décision doit donc intégrer les comorbidités du patient, son mode de vie et ses préférences.
Des outils prédictifs permettent d’estimer le risque de positivité du ganglion sentinelle et peuvent aider à la décision, notamment le site melanomarisk.org, bien qu’ils ne soient pas encore utilisés en routine.En cas de ganglion sentinelle négatif, une simple surveillance est indiquée. En cas de positivité, le patient est reclassé en stade IIIA, ce qui pose la question d’un traitement adjuvant.
Stade IIIA : vers une approche individualisée
Les données récentes remettent en question le caractère systématique du traitement adjuvant dans les stades IIIA. Il a été montré que la quantité de tumeur dans le ganglion sentinelle est un facteur pronostique majeur. Par ailleurs, certaines analyses montrent que les courbes de survie sont similaires entre les patients traités et ceux simplement surveillés, ce qui suggère un risque de surtraitement (2,3).
Concernant les thérapies ciblées, seuls les patients mutés BRAFV600E auraient un bénéfice, tous stades confondus. Ainsi, la stratégie adjuvante par thérapie ciblée dans les stades IIIA semble bénéfique mais il dépend du type de mutation, avec notamment un moindre effet observé pour certaines mutations comme BRAF V600K (4).
Ainsi, la prise en charge des stades IIIA doit être discutée au cas par cas et ne doit pas être systématique.
Stades IIB–IIC : bénéfices et limites du traitement adjuvant
La prise en charge des stades IIB et IIC repose sur une chirurgie avec des marges de 2 cm et la discussion du ganglion sentinelle. Les immunothérapies disposent désormais d’autorisations dans ces stades et ont montré un bénéfice en survie sans récidive dans des essais de phase III.
Cependant, une proportion importante de patients ne récidivera pas, même en l’absence de traitement. Cela expose à un risque de surtraitement, d’autant plus que les immunothérapies peuvent entraîner des effets indésirables sévères et parfois irréversibles.
La décision d’un traitement adjuvant doit donc reposer sur une évaluation rigoureuse du rapport bénéfice-risque, qui doit être expliquée au patient.
Des modèles intégrant des données cliniques, histologiques et génétiques permettent d’identifier des patients à haut ou bas risque de récidive (5). Ces approches, bien que prometteuses, ne sont pas encore utilisées en pratique courante.
Stades III macroscopiques : développement du néoadjuvant
Dans les formes avec atteinte ganglionnaire macroscopique, la stratégie thérapeutique évolue vers une approche néoadjuvante. Le traitement médical est désormais initié avant la chirurgie.
Cette stratégie repose sur le fait que la présence de la tumeur permet une meilleure stimulation du système immunitaire grâce à l’exposition aux antigènes tumoraux.
La réponse pathologique obtenue après traitement devient un marqueur pronostique essentiel et permet d’adapter la suite de la prise en charge (6).Des essais récents ont montré qu’une immunothérapie néoadjuvante, notamment en bithérapie (7,8), améliore significativement le pronostic par rapport à une stratégie classique avec chirurgie d’emblée suivie d’un traitement adjuvant.
Cette approche permet également, chez certains patients, de réduire l’intensité du traitement et donc de limiter les toxicités.
Mélanome avancé (stade IV)
Dans les formes métastatiques, l’association d’immunothérapie anti-PD1 et anti-CTLA4 reste le traitement de référence en première ligne. Cette stratégie permet d’obtenir des réponses durables chez certains patients, avec des survies prolongées.
De nouvelles combinaisons thérapeutiques sont en cours de développement. Certaines visent à améliorer la tolérance, comme l’association avec des anti-LAG3 (opdualag (9)). D’autres stratégies incluent des inhibiteurs multikinase (lenvatinib associé au pembrolizumab (10)), des anticorps bispécifiques (tebentafusp (11)) ou encore des virus oncolytiques administrés en intratumoral en association au pembrolizumab (12).
Ces approches ouvrent des perspectives thérapeutiques prometteuses.
Conclusion
La prise en charge du mélanome évolue vers une médecine de plus en plus personnalisée. Les données récentes soulignent la nécessité d’éviter les traitements systématiques, en particulier dans les stades précoces.
Le développement de stratégies néoadjuvantes et d’outils de stratification du risque permet d’adapter plus finement les traitements.
La décision thérapeutique doit être individualisée, en tenant compte des caractéristiques tumorales, du profil du patient et de ses préférences.
Références
1. Garbe C, Amaral T, Peris K, Hauschild A, Arenberger P, Basset-Seguin N, et al. European consensus-based interdisciplinary guideline for melanoma. Part 2: Treatment - Update 2024. Eur J Cancer. 17 janv 2025;215:115153. doi:10.1016/j.ejca.2024.115153 PubMed PMID: 39709737.
2. Hagopian G, Jiang X, Grant C, Brazel D, Kumar P, Yamamoto M, et al. Survival impact of post-operative immunotherapy in resected stage III cutaneous melanomas in the checkpoint era. ESMO Open. févr 2024;9(2):102193. doi:10.1016/j.esmoop.2023.102193 PubMed PMID: 38271786; PubMed Central PMCID: PMC10937207.
3. Helgadottir H, Ny L, Ullenhag GJ, Falkenius J, Mikiver R, Olofsson Bagge R, et al. Survival after introduction of adjuvant treatment in stage III melanoma: a nationwide registry-based study. J Natl Cancer Inst. 7 sept 2023;115(9):1077‑84. doi:10.1093/jnci/djad081 PubMed PMID: 37227040; PubMed Central PMCID: PMC10483326.
4. Long GV, Hauschild A, Santinami M, Kirkwood JM, Atkinson V, Mandala M, et al. Final Results for Adjuvant Dabrafenib plus Trametinib in Stage III Melanoma. N Engl J Med. 7 nov 2024;391(18):1709‑20. doi:10.1056/NEJMoa2404139 PubMed PMID: 38899716.
5. Amaral T, Chatziioannou E, Nuebling A, Nanz L, Sinnberg T, Niessner H, et al. Risk stratification using the Merlin Assay (CP-GEP) in an independent cohort of 930 patients with clinical stage I/II melanoma who did not undergo sentinel lymph node biopsy. Eur J Cancer. 2 mai 2025;220:115372. doi:10.1016/j.ejca.2025.115372 PubMed PMID: 40274320.
6. Tetzlaff MT, Messina JL, Stein JE, Xu X, Amaria RN, Blank CU, et al. Pathological assessment of resection specimens after neoadjuvant therapy for metastatic melanoma. Ann Oncol. 1 août 2018;29(8):1861‑8. doi:10.1093/annonc/mdy226 PubMed PMID: 29945191; PubMed Central PMCID: PMC6096739.
7. Blank CU, Lucas MW, Scolyer RA, van de Wiel BA, Menzies AM, Lopez-Yurda M, et al. Neoadjuvant Nivolumab and Ipilimumab in Resectable Stage III Melanoma. N Engl J Med. 7 nov 2024;391(18):1696‑708. doi:10.1056/NEJMoa2402604 PubMed PMID: 38828984.
8. Patel SP, Othus M, Chen Y, Wright GP, Yost KJ, Hyngstrom JR, et al. Neoadjuvant-Adjuvant or Adjuvant-Only Pembrolizumab in Advanced Melanoma. N Engl J Med. 2 mars 2023;388(9):813‑23. doi:10.1056/NEJMoa2211437 PubMed PMID: 36856617; PubMed Central PMCID: PMC10410527.
9. Tawbi HA, Schadendorf D, Lipson EJ, Ascierto PA, Matamala L, Castillo Gutiérrez E, et al. Relatlimab and Nivolumab versus Nivolumab in Untreated Advanced Melanoma. N Engl J Med. 6 janv 2022;386(1):24‑34. doi:10.1056/NEJMoa2109970 PubMed PMID: 34986285; PubMed Central PMCID: PMC9844513.
10. Arance A, de la Cruz-Merino L, Petrella TM, Jamal R, Ny L, Carneiro A, et al. Phase II LEAP-004 Study of Lenvatinib Plus Pembrolizumab for Melanoma With Confirmed Progression on a Programmed Cell Death Protein-1 or Programmed Death Ligand 1 Inhibitor Given as Monotherapy or in Combination. J Clin Oncol. 1 janv 2023;41(1):75‑85. doi:10.1200/JCO.22.00221 PubMed PMID: 35867951.
11. Middleton MR, McAlpine C, Woodcock VK, Corrie P, Infante JR, Steven NM, et al. Tebentafusp, A TCR/Anti-CD3 Bispecific Fusion Protein Targeting gp100, Potently Activated Antitumor Immune Responses in Patients with Metastatic Melanoma. Clin Cancer Res. 15 nov 2020;26(22):5869‑78. doi:10.1158/1078-0432.CCR-20-1247 PubMed PMID: 32816891; PubMed Central PMCID: PMC9210997.
12. Wong MK, Milhem MM, Sacco JJ, Michels J, In GK, Muñoz Couselo E, et al. RP1 Combined With Nivolumab in Advanced Anti-PD-1-Failed Melanoma (IGNYTE). J Clin Oncol. 20 nov 2025;43(33):3589‑99. doi:10.1200/JCO-25-01346 PubMed PMID: 40627813; PubMed Central PMCID: PMC12622257.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Pr Marie-Sylvie DOUTRE
Obésité et maladies auto-immunes
En 2024, près de 50 % de la population française est en situation de surpoids ou d’obésité, et cette proportion continue de progresser. Les projections de l’Organisation mondiale de la santé indiquent que la prévalence de l’obésité en France pourrait atteindre entre 25 et 29 % d’ici 2030. Cette évolution s’inscrit dans une tendance mondiale, également observée aux États-Unis, notamment chez les enfants et les adolescents.
L’obésité constitue un enjeu majeur de santé publique en raison de son impact important sur la qualité de vie et de son association avec de nombreuses comorbidités telles que le diabète, les maladies cardiovasculaires, certains cancers et une réduction de l’espérance de vie. Au-delà de ces complications bien connues, des liens entre obésité et maladies auto-immunes sont désormais évoqués, tant sur le plan physiopathologique que clinique.
Sur le plan mécanistique, la leptine, hormone produite par le tissu adipeux et augmentée en cas d’obésité, joue un rôle central en modulant les réponses immunitaires. Elle agit à la fois sur l’immunité innée et adaptative en influençant les monocytes, les macrophages ainsi que différentes populations de lymphocytes T, notamment les cellules Th1, Th17 et les lymphocytes T régulateurs. Ces interactions contribuent à un état inflammatoire chronique susceptible de favoriser ou d’aggraver certaines maladies auto-immunes.
Cliniquement, plusieurs études ont montré une association entre l’obésité et certaines maladies auto-immunes, notamment la polyarthrite rhumatoïde, la sclérose en plaques et le lupus érythémateux systémique. Dans le lupus, il existe un véritable cercle vicieux dans lequel l’inflammation chronique, les traitements par corticoïdes et la diminution de l’activité physique favorisent la prise de poids, tandis que l’obésité aggrave l’inflammation. L’augmentation de l’indice de masse corporelle est ainsi corrélée à l’activité de la maladie, mesurée par le score SLEDAI, ainsi qu’à certaines manifestations cliniques comme les thromboses ou l’atteinte rénale, dont le pronostic est moins favorable chez les patients obèses.
Ces observations soulèvent la question d’implications thérapeutiques potentielles. Les analogues du GLP-1, tels que le sémaglutide, initialement développés pour le diabète et l’obésité, font actuellement l’objet de nombreuses études dans les maladies inflammatoires et auto-immunes (1–3). Les résultats disponibles restent toutefois hétérogènes et parfois contradictoires, et il demeure difficile de déterminer si les effets observés sont directement liés au médicament ou secondaires à la perte de poids induite. Par ailleurs, des effets paradoxaux ont été décrits, notamment l’apparition de lupus cutanés ou systémiques sous traitement.
Ces molécules suscitent un intérêt croissant en raison de leurs effets potentiels dans d’autres domaines tels que la fibromyalgie, les addictions ou certaines maladies neurodégénératives. Néanmoins, leur utilisation s’accompagne d’effets indésirables, parmi lesquels le phénomène dit de « visage Ozempic », caractérisé par un relâchement cutané et un vieillissement facial accéléré lié à une perte de poids rapide, avec des implications en dermatologie esthétique (4,5).
Sarcoïdose : actualités thérapeutiques
La sarcoïdose est une maladie systémique pouvant toucher différents organes, notamment les poumons, la peau et les articulations. Les recommandations européennes publiées en 2021 (6) soulignent l’absence de traitement disposant d’une AMM spécifique ainsi que le manque d’études contrôlées de grande qualité. Elles précisent également que le traitement n’est pas systématique et qu’il doit être réservé aux formes sévères menaçant un organe, la survie ou la qualité de vie. Il n’existe pas de traitement curatif de la sarcoïdose, et les traitements actuels sont uniquement suspensifs, exposant à un risque de rechute.
Les manifestations dermatologiques sont observées dans environ 20 à 30 % des cas et peuvent être isolées ou associées à des atteintes systémiques, en particulier pulmonaires et ganglionnaires.
La prise en charge thérapeutique repose sur une stratégie progressive débutant par les corticoïdes locaux, puis les corticoïdes systémiques en cas d’échec ou de formes plus sévères. D’autres traitements peuvent être utilisés en association, tels que l’hydroxychloroquine, le méthotrexate ou les anti-TNF, bien que le niveau de preuve de ces options reste globalement faible. Une étude française récente menée par Cohen et al. (7) a montré qu’une rémission complète était obtenue chez environ un tiers des patients à un an, avec des résultats comparables entre les corticoïdes systémiques et l’association d’hydroxychloroquine et de corticoïdes locaux. Cette dernière stratégie pourrait être privilégiée en raison d’un meilleur profil de tolérance.
Les avancées dans la compréhension de la physiopathologie de la sarcoïdose ont permis l’émergence de nouvelles options thérapeutiques, notamment les biothérapies telles que les anti-TNF comme l’infliximab ou l’adalimumab, ainsi que des inhibiteurs de JAK comme le tofacitinib et des inhibiteurs de mTOR comme le sirolimus. Ces traitements ne sont pas utilisés en première intention mais représentent des alternatives intéressantes dans les formes résistantes ou corticodépendantes (8–11).
Autres flashs
L’ostéopathie induite par le méthotrexate est une complication désormais décrite dans les maladies inflammatoires chroniques, notamment la polyarthrite rhumatoïde et le psoriasis (12,13). Elle se manifeste par des fissures ou des fractures des os des membres inférieurs, en particulier du tibia ou du pied, responsables de douleurs et de troubles de la marche. Le diagnostic est souvent difficile en raison de radiographies peu contributives, ce qui peut conduire à méconnaître ces lésions. L’IRM ou la scintigraphie osseuse permettent de mettre en évidence des fractures transversales caractéristiques. Lorsque cela est possible, l’arrêt du méthotrexate entraîne une régression des symptômes sans récidive.
Concernant la dermatomyosite, une étude récente portant sur 320 patients n’a pas mis en évidence de différence significative dans la fréquence des auto-anticorps entre les formes classiques avec atteinte musculaire et les formes amyopathiques (14). La présence d’auto-anticorps constitue un argument diagnostique, mais leur absence ne permet pas d’exclure le diagnostic. Ces résultats peuvent varier selon les techniques de laboratoire utilisées et suggèrent l’existence d’auto-anticorps encore non identifiés.
Enfin, la capillaroscopie apparaît comme un outil d’intérêt croissant dans la dermatomyosite. Des anomalies capillaires sont observées dans 80 à 90 % des cas, et certains profils spécifiques pourraient être associés à un risque accru d’atteinte pulmonaire ou de cancer, notamment chez les patients porteurs d’anticorps anti-TIF1γ (15,16). La capillaroscopie pourrait également constituer un marqueur d’évolutivité dans la dermatomyosite juvénile (17).
Références
1. Kyriazi N, Vassilakis KD, Bakiri A, Iliopoulos A, Fragoulis GE. Antiobesity medications in rheumatology. Quo vadis? Ann Rheum Dis. mars 2026;85(3):412‑6. doi:10.1016/j.ard.2025.08.013 PubMed PMID: 40946026.
2. Burke OM, Sa B, Cespedes DA, Tosti A. Dermatologic Implications of Glucagon-Like Peptide-1 Receptor Agonist Medications. Skin Appendage Disord. oct 2025;11(5):416‑23. doi:10.1159/000544023 PubMed PMID: 41058954; PubMed Central PMCID: PMC12500303.
3. Persson C, Eaton A, Mayrovitz HN. A Closer Look at the Dermatological Profile of GLP-1 Agonists. Diseases. 22 avr 2025;13(5):127. doi:10.3390/diseases13050127 PubMed PMID: 40422559; PubMed Central PMCID: PMC12110338.
4. Jodat Z, Shahzad K, Younas M, Afridi H, Mahato RK. Emergence of « ozempic face »: addressing unintended consequences of rapid weight loss. Ann Med Surg (Lond). févr 2026;88(2):2087‑8. doi:10.1097/MS9.0000000000004254 PubMed PMID: 41675819; PubMed Central PMCID: PMC12889234.
5. Daneshgaran G, Shauly O, Gould DJ. « Ozempic Face » in Plastic Surgery: A Systematic Review of the Literature on GLP-1 Receptor Agonist Mediated Weight Loss and Analysis of Public Perceptions. Aesthet Surg J Open Forum. 2025;7:ojaf056. doi:10.1093/asjof/ojaf056 PubMed PMID: 40626110; PubMed Central PMCID: PMC12232544.
6. Baughman RP, Valeyre D, Korsten P, Mathioudakis AG, Wuyts WA, Wells A, et al. ERS clinical practice guidelines on treatment of sarcoidosis. Eur Respir J. déc 2021;58(6):2004079. doi:10.1183/13993003.04079-2020 PubMed PMID: 34140301.
7. Cohen E, Lheure C, Ingen-Housz-Oro S, Hotz C, Bettuzzi T, Chasset F, et al. Which first-line treatment for cutaneous sarcoidosis? A retrospective study of 120 patients. Eur J Dermatol. 1 déc 2023;33(6):680‑5. doi:10.1684/ejd.2023.4584 PubMed PMID: 38465550.
8. Bechman K, Biddle K, Miracle A, He K, Gibson M, Russell MD, et al. Systematic review and meta-analysis of the efficacy of biologic and targeted synthetic therapies in sarcoidosis. Thorax. 15 sept 2025;80(10):702‑10. doi:10.1136/thorax-2025-223014 PubMed PMID: 40393718; PubMed Central PMCID: PMC12505053.
9. Bouadi N, Rijal H, Sood S, Bagit A, Maliyar K, Georgakopoulos JR, et al. Use of Biologics for Cutaneous Sarcoidosis: A Systematic Review. J Cutan Med Surg. 2024;28(3):294‑5. doi:10.1177/12034754241235964 PubMed PMID: 38404164.
10. Quaggetto M, Ben Salem T, Haroche J, Campagne J, Moyon Q, Lhote R, et al. Janus kinase inhibitors in pulmonary and extra-pulmonary sarcoidosis: A case series and a systematic review of the literature. Sarcoidosis Vasc Diffuse Lung Dis. 15 déc 2025;42(4):17246. doi:10.36141/svdld.v42i4.17246 PubMed PMID: 41396108; PubMed Central PMCID: PMC12815289.
11. Redl A, Doberer K, Unterluggauer L, Kleissl L, Krall C, Mayerhofer C, et al. Efficacy and safety of mTOR inhibition in cutaneous sarcoidosis: a single-centre trial. Lancet Rheumatol. févr 2024;6(2):e81‑91. doi:10.1016/S2665-9913(23)00302-8 PubMed PMID: 38267106.
12. Robin F, Leloix A, Guggenbuhl P, Gandemer V, Bonneau-Lagacherie J. Methotrexate osteopathy: Old description, but still important to know. ACR Open Rheumatol. avr 2025;7(4):e70039. doi:10.1002/acr2.70039 PubMed PMID: 40210601; PubMed Central PMCID: PMC11985256.
13. Robin F, Ghossan R, Mehsen-Cetre N, Triquet L, Larid G, Coiffier G, et al. METHOFRACT, a methotrexate osteopathy multicentre cohort study. RMD Open. 25 sept 2025;11(3):e005941. doi:10.1136/rmdopen-2025-005941 PubMed PMID: 40998522; PubMed Central PMCID: PMC12481393.
14. Yang X, Chambers S, On A, Ali H, Khosravi-Hafshejani T, Lopes Almeida Gomes L, et al. Autoantibody Positivity Rates in Classic and Clinically Amyopathic Dermatomyositis. JAMA Dermatol. 1 nov 2025;161(11):1184‑6. doi:10.1001/jamadermatol.2025.3143 PubMed PMID: 40928802; PubMed Central PMCID: PMC12423947.
15. Xu H, Qian J. The role of nailfold video-capillaroscopy in the assessment of dermatomyositis. Rheumatology (Oxford). 1 mai 2025;64(5):2987‑94. doi:10.1093/rheumatology/keae677 PubMed PMID: 39689020.
16. Mumtaz S, Phillipps J, Sullivan MM, Diaz-Menindez M, Wang B, Majithia V, et al. Microvascular abnormalities between anti-TIF1-γ-associated dermatomyositis with and without malignancy. BMC Rheumatol. 6 mai 2025;9(1):50. doi:10.1186/s41927-025-00504-z PubMed PMID: 40329336; PubMed Central PMCID: PMC12057095.
17. Kassani PH, Ehwerhemuepha L, Martin-King C, Kassab R, Gibbs E, Morgan G, et al. Artificial intelligence for nailfold capillaroscopy analyses - a proof of concept application in juvenile dermatomyositis. Pediatr Res. mars 2024;95(4):981‑7. doi:10.1038/s41390-023-02894-7 PubMed PMID: 37993641.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Pr François CHASSET
Trois maladies auto-immunes systémiques à expression dermatologique sont au cœur des avancées récentes : le lupus systémique, la dermatomyosite et la maladie de Sjögren. Les progrès récents concernent à la fois la compréhension des mécanismes physiopathologiques et le développement de nouvelles stratégies thérapeutiques ciblées, en particulier autour des voies de l’interféron et des lymphocytes B.
Lupus systémique : avancées physiopathologiques et thérapeutiques
Rôle central de la peau et des kératinocytes
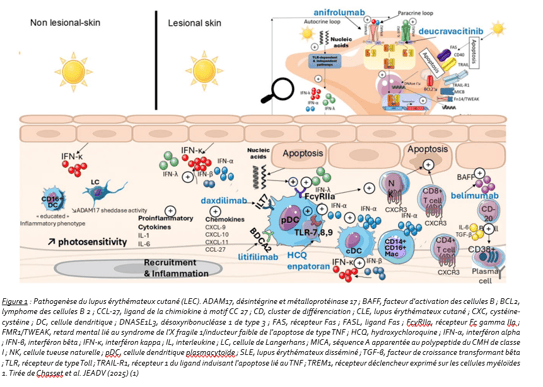
Des progrès majeurs ont permis de démontrer que la peau constitue un organe initiateur du lupus et non plus seulement une cible. Les kératinocytes apparaissent désormais comme des cellules centrales dans la physiopathologie de la maladie. Ils sont capables de produire précocement des interférons de type I, notamment les interférons kappa, alpha et bêta, et ce avant même l’apparition des manifestations cliniques.
La production d’interférons implique plusieurs types cellulaires au sein de la peau, ce qui suggère qu’une inhibition globale de cette voie pourrait être plus efficace qu’un ciblage cellulaire isolé. Les cellules dendritiques plasmacytoïdes conservent un rôle clé, tout comme les lymphocytes B, qui participent à la production d’auto-anticorps.
Figure 1 : Pathogenèse du lupus érythémateux cutané (LEC). ADAM17, désintégrine et métalloprotéinase 17 ; BAFF, facteur d'activation des cellules B ; BCL2, lymphome des cellules B 2 ; CCL-27, ligand de la chimiokine à motif CC 27 ; CD, cluster de différenciation ; CLE, lupus érythémateux cutané ; CXC, cystéine-cystéine ; DC, cellule dendritique ; DNASE1L3, désoxyribonucléase 1 de type 3 ; FAS, récepteur Fas ; FASL, ligand Fas ; FcγRIIa, récepteur Fc gamma IIa ; FMR1/TWEAK, retard mental lié au syndrome de l'X fragile 1/inducteur faible de l'apoptose de type TNF ; HCQ, hydroxychloroquine ; IFN-α, interféron alpha ; IFN-β, interféron bêta ; IFN-κ, interféron kappa ; IL, interleukine ; LC, cellule de Langerhans ; MICA, séquence A apparentée au polypeptide du CMH de classe I ; NK, cellule tueuse naturelle ; pDC, cellule dendritique plasmacytoïde ; SLE, lupus érythémateux disséminé ; TGF-β, facteur de croissance transformant bêta ; TLR, récepteur de type Toll ; TRAIL-R1, récepteur 1 du ligand induisant l'apoptose lié au TNF ; TREM1, récepteur déclencheur exprimé sur les cellules myéloïdes 1. Tirée de Chasset et al. JEADV (2025) (1)
Stratégie thérapeutique actuelle
La prise en charge du lupus cutané associé au lupus systémique repose sur des recommandations actualisées en 2024 (2). Les traitements de première ligne reposent sur les thérapeutiques topiques et l’hydroxychloroquine. En cas d’échec, des traitements de deuxième ligne peuvent être proposés, incluant le thalidomide, le méthotrexate et certaines biothérapies.
L’objectif thérapeutique actuel est d’atteindre une rémission clinique, définie par l’absence de symptômes, une faible activité globale de la maladie, une corticothérapie minimale inférieure à 5 mg par jour et une stabilité du traitement de fond.
Biothérapies ciblant les lymphocytes B
Le belimumab dispose aujourd’hui d’un niveau de preuve élevé avec plusieurs essais de phase III ayant inclus au total plus de 2000 patients. Les analyses combinées post-hoc montrent une amélioration significative par rapport au placebo, avec une réponse prolongée dans le temps (3). Cette efficacité semble particulièrement marquée chez les patients présentant une activité immunologique élevée, ce qui ouvre la voie à une médecine plus personnalisée.
L’obinutuzumab, anticorps anti-CD20, a également démontré son efficacité dans les atteintes systémiques du lupus, avec des taux de rémission supérieurs au placebo, bien que les données spécifiques sur l’atteinte cutanée restent encore limitées (4,5).
Inhibition des interférons
L’anifrolumab, qui bloque le récepteur des interférons de type I, constitue une avancée majeure dans la prise en charge du lupus systémique. Les études montrent une réponse rapide et importante sur l’atteinte cutanée, avec une amélioration significative des scores d’activité dès les premiers mois (6).
À long terme, ce traitement permet d’obtenir des taux de rémission supérieurs à ceux du traitement standard. Des données récentes issues de la vie réelle confirment ces résultats, avec une proportion importante de patients atteignant une faible activité de la maladie (7).
Une nouvelle formulation sous-cutanée, administrée de manière hebdomadaire, a récemment démontré une efficacité comparable, voire supérieure, à la forme intraveineuse, ce qui pourrait améliorer l’accessibilité et l’acceptabilité du traitement dans les années à venir.
Nouvelles molécules en développement
Le deucravacitinib, inhibiteur de TYK2 déjà utilisé dans le psoriasis, montre des résultats très prometteurs dans le lupus systémique, notamment sur les atteintes cutanées et articulaires (8). Il agit en réduisant efficacement la signature interféron et pourrait constituer une option thérapeutique orale innovante.
D’autres molécules, telles que l’enpatoran (9) et l’afimetoran (10), ciblant les récepteurs TLR7 et TLR8, présentent également des résultats encourageants avec un profil de tolérance favorable. Ces traitements confirment l’intérêt croissant pour le ciblage des voies de l’immunité innée dans le lupus.
Dermatomyosite : nouvelles perspectives thérapeutiques
Limites des traitements conventionnels
Dans la dermatomyosite, les antipaludéens de synthèse présentent une efficacité limitée, avec des taux de réponse faibles et une fréquence élevée d’effets indésirables conduisant souvent à l’arrêt du traitement. Ces données remettent en question leur utilisation systématique dans cette pathologie.
Ciblage des interférons
Les interférons de type I apparaissent comme une cible thérapeutique particulièrement pertinente dans la dermatomyosite. Des observations initiales (11) ont suggéré une efficacité de l’anifrolumab sur les atteintes cutanées et musculaires, résultats désormais confirmés par des études prospectives.
Une cohorte espagnole a notamment montré une amélioration rapide et durable de l’atteinte cutanée, mesurée par le score CDASI (12). Des travaux similaires sont en cours en France et devraient confirmer ces résultats.
Innovations thérapeutiques
De nouvelles stratégies thérapeutiques sont en cours de développement, notamment avec le dazukibart (13), qui cible spécifiquement l’interféron bêta, et le brepocitinib (14), inhibiteur des voies JAK. Ce dernier a récemment montré des résultats positifs dans un essai de phase III, constituant une avancée majeure dans la prise en charge de la dermatomyosite.
Maladie de Sjögren : vers une nouvelle ère thérapeutique
Évolution des concepts
Un consensus international récent recommande l’utilisation du terme « maladie de Sjögren », remplaçant les anciennes appellations de syndrome (15). Cette évolution terminologique reflète une meilleure reconnaissance de la maladie et de son impact sur les patients.
Associations et diagnostic
La maladie de Sjögren est fréquemment associée à d’autres maladies auto-immunes, notamment le lupus systémique, la dermatomyosite, la polyarthrite rhumatoïde et les spondyloarthrites. Elle reste cependant probablement sous-diagnostiquée, ce qui justifie une vigilance accrue chez les patients présentant ces pathologies.
Nouvelles biothérapies
Des avancées thérapeutiques majeures sont en cours avec le développement de l’ianalumab, un anticorps ciblant le BAFF et entraînant une déplétion des lymphocytes B. Les essais de phase III ont montré des résultats positifs, avec une amélioration significative de l’activité de la maladie et du flux salivaire (16).
Cette molécule pourrait représenter la première biothérapie efficace dans la maladie de Sjögren, ouvrant des perspectives thérapeutiques inédites pour cette pathologie longtemps dépourvue de traitements spécifiques.
Conclusion
Les avancées récentes dans le lupus systémique, la dermatomyosite et la maladie de Sjögren mettent en évidence le rôle central des interférons de type I et des lymphocytes B dans la physiopathologie de ces maladies. Le développement de thérapies ciblées permet d’envisager une amélioration significative de la prise en charge, avec des stratégies de plus en plus personnalisées. La dermatologie occupe une place essentielle dans cette évolution, notamment dans l’identification et le suivi des atteintes cutanées.
Références
1. Chasset F, Teboul A. Update on cutaneous lupus erythematosus pathogenesis, diagnosis and management. Journal of the European Academy of Dermatology and Venereology. n/a(n/a). doi:10.1111/jdv.70186
2. Amoura Z, Bader-Meunier B, Antignac M, Bardin N, Belizna C, Belot A, et al. French protocol for the diagnosis and management of systemic lupus erythematosus. La Revue de Médecine Interne. sept 2024;45(9):559‑99. doi:10.1016/j.revmed.2024.07.006
3. Grosso G, Giannopoulou N, Tsoi A, Cetrez N, Nikolopoulos D, Lindblom J, et al. Belimumab efficacy in mucocutaneous manifestations of systemic lupus erythematosus: a large post hoc analysis of five phase III clinical trials. Rheumatology (Oxford). 1 juill 2025;64(7):4257‑66. doi:10.1093/rheumatology/keaf145 PubMed PMID: 40085009; PubMed Central PMCID: PMC12212913.
4. Furie RA, Rovin BH, Garg JP, Santiago MB, Aroca-Martínez G, Zuta Santillán AE, et al. Efficacy and Safety of Obinutuzumab in Active Lupus Nephritis. N Engl J Med. 17 avr 2025;392(15):1471‑83. doi:10.1056/NEJMoa2410965 PubMed PMID: 39927615.
5. Furie RA, Dall’Era M, Vital EM, Garg JP, Irazoque Palazuelos F, Zuta Santillán AE, et al. Efficacy and Safety of Obinutuzumab in Active Systemic Lupus Erythematosus. N Engl J Med. 6 mars 2026. doi:10.1056/NEJMoa2516150 PubMed PMID: 41789864.
6. de La Rochefoucauld J, Teboul A, Ait Abdallah N, Sonigo G, Papo M, Charre C, et al. Predictors of response to anifrolumab in cutaneous lupus erythematosus: A prospective cohort study of 57 patients. J Am Acad Dermatol. janv 2026;94(1):235‑8. doi:10.1016/j.jaad.2025.08.092 PubMed PMID: 40914462.
7. Tani C, Cardelli C, Moroni L, Zen M, Bottazzi F, Fredi M, et al. Patient profiles and early response in patients with systemic lupus erythematosus initiating anifrolumab: interim analysis from the ongoing multicentre observational REVEAL study. Lancet Rheumatol. mars 2026;8(3):e181‑91. doi:10.1016/S2665-9913(25)00316-9 PubMed PMID: 41655581.
8. Morand E, Pike M, Merrill JT, van Vollenhoven R, Werth VP, Hobar C, et al. Deucravacitinib, a Tyrosine Kinase 2 Inhibitor, in Systemic Lupus Erythematosus: A Phase II, Randomized, Double-Blind, Placebo-Controlled Trial. Arthritis Rheumatol. févr 2023;75(2):242‑52. doi:10.1002/art.42391 PubMed PMID: 36369798; PubMed Central PMCID: PMC10100399.
9. Witte T, Fernandez-Ruiz R, Abramova N, Weinelt D, Moreau F, Klopp-Schulze L, et al. Enpatoran, a first-in-class, selective, orally administered toll-like receptor 7/8 inhibitor, in systemic and cutaneous lupus erythematosus: results from a randomised, placebo-controlled phase Ib study. Lupus Sci Med. 23 oct 2025;12(2):e001705. doi:10.1136/lupus-2025-001705 PubMed PMID: 41136221; PubMed Central PMCID: PMC12557744.
10. Hosein F, Ignatenko S, Chadwick KD, Zhu L, Baribaud F, Saini J, et al. Safety, Tolerability, Efficacy, Pharmacokinetics, and Pharmacodynamics of Afimetoran, a Toll-Like Receptor 7 and 8 Inhibitor, in Patients With Cutaneous Lupus Erythematosus: A Phase 1b Randomized, Double-Blind, Placebo-Controlled Study. ACR Open Rheumatol. juill 2025;7(7):e70059. doi:10.1002/acr2.70059 PubMed PMID: 40568766; PubMed Central PMCID: PMC12198911.
11. Srivatsa A, Rehman W, Rehman R, Moossavi M, Daveluy S, Potts G. A novel treatment for refractory dermatomyositis: A systematic review of anifrolumab and dermatomyositis. J Am Acad Dermatol. août 2025;93(2):543‑6. doi:10.1016/j.jaad.2025.04.025 PubMed PMID: 40228662.
12. Retuerto-Guerrero M, Moriano Morales C, Pareja-Martínez A, Molina-Esteban N, Puig-Buendia J, Postigo Llorente C, et al. Real-world experience of anifrolumab in 30 patients with refractory DM: a multicentre-multidisciplinary retrospective study. Rheumatology (Oxford). 4 févr 2026;65(2):keaf662. doi:10.1093/rheumatology/keaf662 PubMed PMID: 41400930.
13. Fiorentino D, Mangold AR, Werth VP, Christopher-Stine L, Femia A, Chu M, et al. Efficacy, safety, and target engagement of dazukibart, an IFNβ specific monoclonal antibody, in adults with dermatomyositis: a multicentre, double-blind, randomised, placebo-controlled, phase 2 trial. Lancet. 11 janv 2025;405(10473):137‑46. doi:10.1016/S0140-6736(24)02071-3 PubMed PMID: 39798982.
14. Paik JJ, Vencovský J, Charles-Schoeman C, Wright GC, Vleugels RA, Goriounova AS, et al. Brepocitinib, a potent and selective TYK2/JAK1 inhibitor: scientific and clinical rationale for dermatomyositis. Clin Exp Rheumatol. févr 2025;43(2):354‑63. doi:10.55563/clinexprheumatol/eeglsa PubMed PMID: 39008325.
15. Ramos-Casals M, Baer AN, Brito-Zerón MDP, Hammitt KM, Bouillot C, Retamozo S, et al. 2023 International Rome consensus for the nomenclature of Sjögren disease. Nat Rev Rheumatol. juill 2025;21(7):426‑37. doi:10.1038/s41584-025-01268-z PubMed PMID: 40494962.
16. Dörner T, Bowman SJ, Fox R, Mariette X, Papas A, Grader-Beck T, et al. Safety and Efficacy of Ianalumab in Patients With Sjögren’s Disease: 52-Week Results From a Randomized, Placebo-Controlled, Phase 2b Dose-Ranging Study. Arthritis Rheumatol. mai 2025;77(5):560‑70. doi:10.1002/art.43059 PubMed PMID: 39557617.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Dr Cédric LENORMAND
Syndrome VEXAS
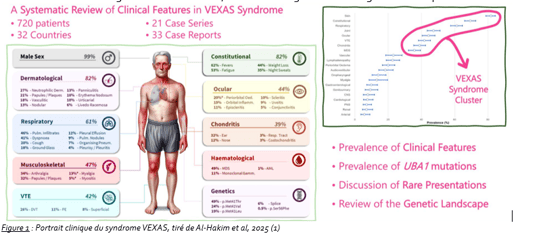
Le syndrome VEXAS est une maladie auto-inflammatoire acquise liée à des mutations somatiques du gène UBA1 situé sur le chromosome X. Cette pathologie touche presque exclusivement les hommes de plus de 50 ans et reste exceptionnelle chez les femmes. La mutation survient dans un progéniteur myéloïde, ce qui explique l’association d’anomalies hématologiques et de manifestations inflammatoires systémiques pouvant atteindre de nombreux organes. Le syndrome VEXAS se distingue ainsi par son caractère très systémique, en faisant une des maladies les plus internistes. Un signe d’alerte fréquent est la macrocytose, qui constitue souvent un premier indice d’atteinte médullaire. L’évolution se fait fréquemment vers un syndrome myélodysplasique avec apparition d’une anémie, parfois d’une thrombopénie et souvent d’une gammapathie monoclonale. Les données épidémiologiques récentes suggèrent que cette maladie est plus fréquente qu’initialement estimé, avec une prévalence d’environ un homme sur 4000 après 50 ans.
Manifestations cliniques systémiques
Les manifestations générales telles que la fièvre et l’altération de l’état général ne sont pas constantes. Les patients peuvent présenter des atteintes oculaires, des chondrites, des arthralgies, des myosites, des atteintes respiratoires ainsi que des atteintes digestives, notamment des colites neutrophiliques. De nouvelles manifestations sont régulièrement décrites, traduisant la grande hétérogénéité clinique de la maladie.
Manifestations dermatologiques
Les atteintes cutanées sont très fréquentes, étant présentes chez plus de 80 % des patients, et constituent le premier signe de la maladie dans environ deux tiers des cas. Les lésions typiques se présentent sous la forme de plaques érythémato-œdémateuses, arciformes, non fugaces, avec une collerette desquamative centrale qui persistent plusieurs semaines avant de disparaître. Ces lésions, bien que non spécifiques, sont fortement évocatrices du syndrome VEXAS dans un contexte clinique adapté.
D’autres présentations cutanées sont possibles, notamment des papules érythémateuses ou des lésions maculeuses peu infiltrées d’aspect urticarien qui peuvent évoquer un granulome annulaire interstitiel. Il est important de savoir évoquer ce diagnostic chez un homme de plus de 50 ans présentant ce type de lésions. Des manifestations vasculaires peuvent également être observées, comme un livedo racemosa témoignant d’un état de thrombophilie, des purpuras palpables traduisant une vasculite des petits vaisseaux, ainsi que des nodules de type érythème noueux ou thrombophlébites nodulaires. Des réactions au site d’injection de certains traitements, notamment l’anakinra, sont également décrites.
Sur le plan histologique, les lésions cutanées correspondent le plus souvent à un syndrome de Sweet histiocytoïde. Les cellules présentes dans la peau portent la mutation UBA1, ce qui correspond à un véritable tableau de leukemia cutis.
Diagnostic
Le diagnostic repose sur la mise en évidence de la mutation du gène UBA1 sur un prélèvement sanguin. La présence de lésions cutanées évocatrices chez un homme de plus de 50 ans doit conduire à rechercher cette mutation afin de confirmer le diagnostic.
Prise en charge thérapeutique du syndrome VEXAS
Les traitements dermatologiques classiques, tels que la dapsone, la colchicine, les antipaludéens de synthèse, le méthotrexate ou l’azathioprine, sont globalement peu efficaces. La corticothérapie permet un contrôle des symptômes mais expose à une corticodépendance importante, avec des rechutes fréquentes en dessous de 15 mg par jour, rendant cette stratégie difficile à maintenir à long terme.
Les thérapies ciblées, notamment les anti-interleukine 6 comme le tocilizumab et les inhibiteurs de JAK tels que le ruxolitinib, montrent une efficacité modérée, avec une réponse observée chez environ un tiers des patients (2,3). Les anti-interleukine 1 et les anti-TNF apparaissent globalement peu efficaces.
L’azacitidine, agent hypométhylant utilisé dans les syndromes myélodysplasiques, constitue une option thérapeutique prometteuse. Elle permet d’obtenir une réponse inflammatoire chez environ 60 % des patients et une réponse hématologique chez près de 75 % d’entre eux (4). Ce traitement présente également un effet prolongé avec un maintien de la rémission chez la majorité des patients à 1 an et à 5 ans. Son mécanisme repose sur le ciblage du clone pathologique, illustrant l’intérêt d’une approche dirigée contre la cause de la maladie plutôt que contre ses seules conséquences.
Les patients atteints de VEXAS présentent par ailleurs un risque infectieux accru, notamment d’infections opportunistes à germes intracellulaires, ce qui impose une surveillance et des mesures préventives adaptées.
Vasculites
Exploration des vasculites des petits vaisseaux
Les recommandations récentes soulignent l’importance de ne pas se limiter à une biopsie cutanée standard et de réaliser systématiquement une IFD afin de rechercher des dépôts d’immunoglobulines, en particulier les IgA. Le bilan biologique initial doit comporter une numération formule sanguine, une CRP, une créatinine ainsi qu’un examen urinaire à la recherche d’une hématurie, d’une protéinurie et de cylindres hématiques. Un bilan immunologique complet est également nécessaire, incluant notamment les ANCA, les ANA, le complément, le facteur rhumatoïde, la recherche de cryoglobulinémie ainsi qu’une électrophorèse des protéines avec immunofixation. Il est enfin essentiel de rechercher une cause infectieuse, en particulier des agents à tropisme endothélial ou des infections systémiques.
Vasculites à IgA de l’adulte : nouvelles données
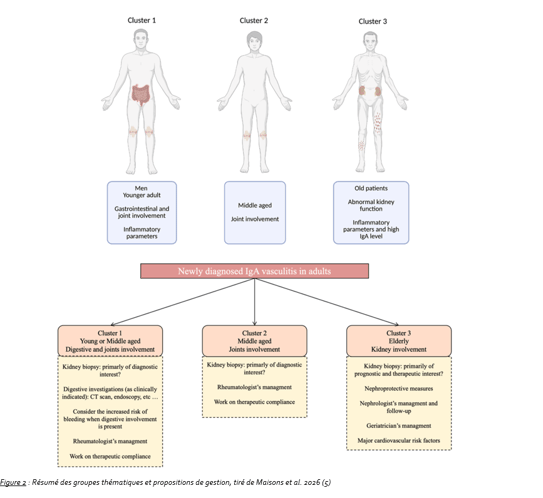
Des travaux récents utilisant l’intelligence artificielle ont permis d’identifier trois profils cliniques distincts chez les patients atteints de vasculite à IgA (5). Le groupe 1 avec des patients plutôt jeunes présentent fréquemment des signes généraux marqués avec une atteinte digestive parfois sévère. Le groupe 2 avec des patients d’âge intermédiaire présentent plutôt une atteinte articulaire et cutanée sans atteinte digestive significative. Enfin, le groupe 3 avec des patients plus âgés présentent des lésions cutanées plus sévères, souvent nécrotiques ou bulleuses, associées à une atteinte rénale plus importante et à un risque accru d’évolution vers une insuffisance rénale chronique. Le groupe 1 a tendance à rechuter plus fréquemment, tandis que le groupe 3 avec des patients âgés est plus sévère sur le plan rénal.
Facteurs de rechute
Les facteurs associés au risque de rechute des vasculites à IgA incluent la présence initiale de fièvre, une atteinte articulaire et la présence de lésions purpuriques abdominales. À l’inverse, un contexte infectieux initial et l’utilisation de corticoïdes semblent associés à un moindre risque de récidive (6).
Atteinte rénale et innovations thérapeutiques
L’atteinte rénale des vasculites à IgA repose sur la formation de complexes immuns impliquant des immunoglobulines A1 mal glycosylées, qui se déposent dans le rein et induisent une inflammation avec altération de la fonction rénale. La prise en charge repose initialement sur un traitement néphroprotecteur, suivi en cas d’échec d’une corticothérapie, voire d’immunosuppresseurs dans les formes sévères.
De nouvelles options thérapeutiques ont émergé récemment, notamment les corticoïdes à action digestive comme le budésonide (7), ainsi que plusieurs traitements ciblant différentes voies physiopathologiques, notamment les antagonistes des récepteurs de l’endothéline l’atrasentan (8), les inhibiteurs du complément et les inhibiteurs de BAFF/APRIL (9). Ces traitements permettent une réduction significative de la protéinurie et représentent des alternatives prometteuses à la corticothérapie.
Traitement des formes cutanées récidivantes
Dans les formes cutanées récidivantes de vasculite à IgA, la dapsone apparaît comme une option thérapeutique efficace, avec une efficacité comparable à celle des corticoïdes associés aux immunosuppresseurs (10). Toutefois, un arrêt trop rapide du traitement expose à un risque de rechute.
Des avancées récentes en médecine préventive doivent également être soulignées. Une dose unique de vaccin contre l’HPV semble aussi efficace que deux doses chez les adolescentes, ce qui pourrait améliorer l’adhésion vaccinale (11). La vaccination contre le VRS chez les sujets âgés permet de réduire significativement le risque d’hospitalisation (12). Enfin, l’utilisation d’un spray nasal d’azélastine pourrait réduire le risque d’infections virales respiratoires, notamment le COVID-19, ainsi que la durée des symptômes et la contagiosité (13).
Références
1. Al-Hakim A, Goldberg S, Gaillard S, Heiblig M, Beck DB, Savic S. Clinical features in VEXAS syndrome: a systematic review. Rheumatology (Oxford). 16 juin 2025;64(10):5217‑29. doi:10.1093/rheumatology/keaf293 PubMed PMID: 40570089; PubMed Central PMCID: PMC12494223.
2. Hadjadj J, Nguyen Y, Mouloudj D, Bourguiba R, Heiblig M, Aloui H, et al. Efficacy and safety of targeted therapies in VEXAS syndrome: retrospective study from the FRENVEX. Ann Rheum Dis. 30 sept 2024;83(10):1358‑67. doi:10.1136/ard-2024-225640 PubMed PMID: 38777378.
3. Al-Hakim A, Trikha R, Phyu Htut EE, Chowdhury O, MacLennan CA, Chee A, et al. Treatment outcomes in patients with VEXAS syndrome: a retrospective cohort study. Lancet Rheumatol. juill 2025;7(7):e472‑84. doi:10.1016/S2665-9913(25)00034-7 PubMed PMID: 40412417.
4. Jachiet V, Kosmider O, Beydon M, Hadjadj J, Zhao LP, Grobost V, et al. Efficacy and safety of azacitidine for VEXAS syndrome: a large-scale retrospective study from FRENVEX. Blood. 18 sept 2025;146(12):1450‑61. doi:10.1182/blood.2024028133 PubMed PMID: 40373272.
5. Maisons V, Hankard A, Hočevar A, Pillebout E, Halimi JM, Sautenet B, et al. Identifying distinct clinical phenotypes and outcomes in adult-onset IgA vasculitis using unsupervised clustering analysis. Eur J Intern Med. 4 févr 2026;106742. doi:10.1016/j.ejim.2026.106742 PubMed PMID: 41644397.
6. Lutz W, Hua C, Mariotti EB, Terrier B, Dupin N, Aractingi S, et al. Risk factors for recurrence or relapse after a first episode of adult IgA vasculitis: A multicenter retrospective study. J Am Acad Dermatol. févr 2026;94(2):495‑502. doi:10.1016/j.jaad.2025.10.009 PubMed PMID: 41061973.
7. Lafayette R, Kristensen J, Stone A, Floege J, Tesař V, Trimarchi H, et al. Efficacy and safety of a targeted-release formulation of budesonide in patients with primary IgA nephropathy (NefIgArd): 2-year results from a randomised phase 3 trial. Lancet. 9 sept 2023;402(10405):859‑70. doi:10.1016/S0140-6736(23)01554-4 PubMed PMID: 37591292.
8. Heerspink HJL, Jardine M, Kohan DE, Lafayette RA, Levin A, Liew A, et al. Atrasentan in Patients with IgA Nephropathy. N Engl J Med. 6 févr 2025;392(6):544‑54. doi:10.1056/NEJMoa2409415 PubMed PMID: 39460694.
9. Lafayette R, Barbour SJ, Brenner RM, Campbell KN, Doan T, Eren N, et al. A Phase 3 Trial of Atacicept in Patients with IgA Nephropathy. N Engl J Med. 12 févr 2026;394(7):647‑57. doi:10.1056/NEJMoa2510198 PubMed PMID: 41196369.
10. Glatre A, Mahévas T, Jaccard C, Moulis G, Chasset F, Senet P, et al. Treatment strategies and outcomes in adult relapsing or refractory cutaneous IgA Vasculitis: A multicenter retrospective cohort study. Semin Arthritis Rheum. déc 2025;75:152870. doi:10.1016/j.semarthrit.2025.152870 PubMed PMID: 41270569.
11. Kreimer AR, Porras C, Liu D, Hildesheim A, Carvajal LJ, Ocampo R, et al. Noninferiority of One HPV Vaccine Dose to Two Doses. N Engl J Med. 18 déc 2025;393(24):2421‑33. doi:10.1056/NEJMoa2506765 PubMed PMID: 41337735.
12. Lassen MCH, Johansen ND, Christensen SH, Aliabadi N, Skaarup KG, Modin D, et al. RSV Prefusion F Vaccine for Prevention of Hospitalization in Older Adults. N Engl J Med. 8 janv 2026;394(2):138‑51. doi:10.1056/NEJMoa2509810 PubMed PMID: 40888695.
13. Lehr T, Meiser P, Selzer D, Rixecker T, Holzer F, Mösges R, et al. Azelastine Nasal Spray for Prevention of SARS-CoV-2 Infections: A Phase 2 Randomized Clinical Trial. JAMA Intern Med. 1 nov 2025;185(11):1309‑17. doi:10.1001/jamainternmed.2025.4283 PubMed PMID: 40892398; PubMed Central PMCID: PMC12406145.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Pr Julien Seneschal
Le vitiligo est une dermatose chronique acquise caractérisée par une dépigmentation cutanée, dont la présentation clinique est particulièrement hétérogène. En effet, les lésions peuvent varier en termes de localisation, d’étendue et de dynamique évolutive, ce qui rend indispensable une approche individualisée pour chaque patient.
Les recommandations internationales récentes insistent sur la nécessité de définir des objectifs thérapeutiques clairs. Dans un premier temps, il est essentiel de stopper la progression de la maladie, car l’activité du vitiligo est un facteur clé de mauvais pronostic. Dans un second temps, l’objectif est d’induire une repigmentation des lésions. Enfin, il est nécessaire de maintenir cette repigmentation dans le temps, ce qui constitue souvent un défi thérapeutique.
Évaluation de l’activité de la maladie
L’identification d’un vitiligo actif est une étape fondamentale dans la prise en charge, car elle conditionne les décisions thérapeutiques.
Il est indispensable de rechercher des signes cliniques objectifs d’activité. Parmi ceux-ci, on retrouve la présence de bordures floues traduisant une extension en cours, ainsi que des lésions en « confettis », correspondant à de petites macules dépigmentées disséminées. L’aspect trichrome, associant une zone centrale blanche, une zone intermédiaire hypopigmentée et une périphérie hyperpigmentée, est également évocateur d’activité. Enfin, le phénomène de Koebner de type 2B, correspondant à l’apparition de lésions sur des zones de traumatisme sous forme linéaire, constitue un signe supplémentaire de maladie évolutive.
Stratégies thérapeutiques de stabilisation
Chez les patients présentant un vitiligo actif, la priorité est la stabilisation de la maladie, qui repose sur des traitements immunomodulateurs.
Les traitements locaux comprennent principalement les dermocorticoïdes et les inhibiteurs de la calcineurine, tels que le tacrolimus. Ce dernier bénéficie actuellement d’un accès compassionnel avec une autorisation d’utilisation à partir de l’âge de 2 ans, ce qui élargit les possibilités thérapeutiques chez l’enfant.
Dans les formes plus actives ou extensives, un traitement systémique peut être nécessaire. La corticothérapie générale en mini-bolus est alors utilisée, généralement sous forme de méthylprednisolone administrée deux jours par semaine. La posologie est adaptée au poids du patient. Cette stratégie permet de contrôler rapidement l’activité de la maladie et peut être utilisée également chez l’enfant, notamment sous forme de comprimés orodispersibles facilitant l’observance.
Il existe d’autres traitements systémiques utilisés hors AMM, notamment le méthotrexate. Dans tous les cas, l’association avec une photothérapie permet une repigmentation plus efficace.
Ruxolitinib topique : une innovation majeure
Le ruxolitinib topique représente une avancée thérapeutique importante dans la prise en charge du vitiligo.
Son utilisation repose sur une application biquotidienne, sur des surfaces limitées à moins de 10 % de la surface corporelle. Il est important d’informer le patient que l’efficacité du traitement ne peut être évaluée qu’après une durée prolongée, généralement comprise entre 6 mois et un an, ce qui nécessite une bonne observance.
Les données cliniques montrent une efficacité notable, en particulier au niveau du visage, où plus de la moitié des patients obtiennent une repigmentation supérieure à 75 %. Au niveau du corps, environ la moitié des patients obtiennent une repigmentation supérieure à 50 % (1). Par ailleurs, les études montrent qu’il n’existe pas de plateau d’efficacité, et que la poursuite du traitement peut permettre d’améliorer encore les résultats même après deux ans.
Individualisation des objectifs thérapeutiques
Dans les formes étendues de vitiligo, il est souvent nécessaire d’adapter les objectifs thérapeutiques en fonction des attentes du patient. Il peut être pertinent de cibler en priorité certaines zones visibles, comme le visage ou le décolleté, qui ont un impact psychologique majeur.
La réponse thérapeutique varie selon les localisations. Les zones du visage et du cou répondent généralement très bien au traitement, avec des repigmentations rapides et importantes. À l’inverse, les extrémités, notamment les mains et les pieds, sont beaucoup plus résistantes au traitement, voire réfractaires dans certains cas (2). Cette variabilité doit être expliquée au patient afin d’adapter ses attentes.
Maintien de la repigmentation
Une fois la repigmentation obtenue, la question du maintien du résultat se pose. Les données montrent qu’en cas d’arrêt du traitement, une rechute survient dans environ 60% des cas, souvent au niveau des mêmes zones, ce qui suggère l’existence d’une mémoire cutanée.
Le traitement de maintien est bien établi avec le tacrolimus, dont l’application deux fois par semaine permet de maintenir la repigmentation dans la grande majorité des cas. En revanche, pour le ruxolitinib, les données concernant les stratégies de maintien sont encore limitées, et des études sont en cours pour évaluer l’intérêt d’une réduction de la fréquence d’application.
Inhibiteurs de JAK systémiques
Les inhibiteurs de JAK administrés par voie orale représentent une option prometteuse pour les formes sévères, actives et étendues de vitiligo.
Les résultats des études de phase 3, notamment avec l’upadacitinib, montrent qu’environ un quart des patients obtiennent une amélioration significative du vitiligo, avec une repigmentation importante du visage et du corps après un an de traitement. Ces résultats doivent être interprétés en tenant compte du profil des patients inclus, souvent porteurs de formes sévères.
Ces traitements systémiques sont amenés à être utilisés en association avec d’autres modalités, notamment la photothérapie.
Photothérapie : un pilier du traitement
La photothérapie par UVB à spectre étroit reste un élément central de la prise en charge du vitiligo.
Elle est débutée à faible dose (0,2 J/cm2) avec un rythme de 2 à 3 séances par semaine et une augmentation progressive au fil des séances, jusqu’à l’obtention d’un érythème léger. Elle peut être utilisée chez l’enfant, à condition que celui-ci soit capable de rester immobile dans la cabine. L’exposition solaire naturelle peut également être proposée, de manière encadrée, avec des durées d’exposition progressives. Le traitement topique doit être appliqué au moins 2 heures avant une exposition solaire ou après celle-ci.
Intérêt des associations thérapeutiques
L’association de la photothérapie avec les traitements immunomodulateurs, qu’ils soient topiques ou systémiques, permet d’améliorer significativement les résultats.
Les études montrent que cette combinaison augmente la rapidité de repigmentation et le taux de réponse (3,4). Par exemple, l’association du ruxolitinib avec la photothérapie permet d’obtenir des taux de repigmentation faciale supérieurs à 80 %, contre environ 50 % en monothérapie. De même, l’association du baricitinib avec la photothérapie montre des résultats nettement supérieurs à la photothérapie seule.
Ces données confirment que les stratégies combinées représentent aujourd’hui une approche thérapeutique de référence.
Perspectives thérapeutiques
De nombreuses innovations sont en cours de développement dans le domaine du vitiligo. Parmi celles-ci, on retrouve d’autres inhibiteurs de JAK comme le ritlecitinib, le deucravacitinib qui agit également sur TYK2, ainsi que des biothérapies ciblant des cytokines spécifiques, notamment l’interleukine 15.
D’autres approches sont également à l’étude, comme l’utilisation de l’anifrolumab en association avec la photothérapie. Des essais cliniques concernent également des populations spécifiques, notamment les enfants, ainsi que des stratégies combinées associant plusieurs traitements.
Conclusion
La prise en charge du vitiligo connaît actuellement des avancées majeures, avec l’émergence de nouvelles thérapies ciblées et de stratégies combinées. L’évaluation précise de l’activité de la maladie et la définition d’objectifs thérapeutiques personnalisés sont essentielles pour optimiser les résultats.
L’association des traitements immunomodulateurs avec la photothérapie apparaît aujourd’hui comme une stratégie particulièrement efficace, permettant d’améliorer significativement la repigmentation et la qualité de vie des patients.
Références
1.Rosmarin D, Passeron T, Pandya AG, Grimes P, Harris JE, Desai SR, et al. Two Phase 3, Randomized, Controlled Trials of Ruxolitinib Cream for Vitiligo. N Engl J Med. 20 oct 2022;387(16):1445‑55. doi:10.1056/NEJMoa2118828 PubMed PMID: 36260792.
2.Passeron T, Harris JE, Pandya AG, Seneschal J, Grimes P, Kornacki D, et al. Repigmentation by body region in patients with vitiligo treated with ruxolitinib cream over 52 weeks. J Eur Acad Dermatol Venereol. mars 2025;39(3):e251‑4. doi:10.1111/jdv.20236 PubMed PMID: 39011655; PubMed Central PMCID: PMC11851260.
3.Dang YP, Li Q, Shi F, Yuan XY, Liu W. Effect of topical calcineurin inhibitors as monotherapy or combined with phototherapy for vitiligo treatment: a meta-analysis. Dermatol Ther. 2016;29(2):126‑33. doi:10.1111/dth.12295 PubMed PMID: 26460804.
4.Lee JH, Kwon HS, Jung HM, Lee H, Kim GM, Yim HW, et al. Treatment Outcomes of Topical Calcineurin Inhibitor Therapy for Patients With Vitiligo: A Systematic Review and Meta-analysis. JAMA Dermatol. 1 août 2019;155(8):929‑38. doi:10.1001/jamadermatol.2019.0696 PubMed PMID: 31141108; PubMed Central PMCID: PMC6547091.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Dr Olivier COGREL
La maladie de Verneuil, également appelée hidradénite suppurée, est une dermatose inflammatoire chronique particulièrement invalidante. Elle se caractérise par des lésions douloureuses à type de nodules inflammatoires, d’abcès récidivants et de fistules, responsables à terme de cicatrices irréversibles.
Contrairement à d’autres dermatoses inflammatoires, cette pathologie évolue volontiers vers des formes destructrices si elle n’est pas prise en charge précocement. Ainsi, l’un des objectifs majeurs est d’éviter la progression vers les stades fistulisants, qui marquent un tournant évolutif sévère.Il existe donc une véritable fenêtre d’opportunité thérapeutique, (1–3) durant laquelle une intervention adaptée permettrait de modifier l’histoire naturelle de la maladie et de prévenir les séquelles cicatricielles.
Retard diagnostique et enjeux de prise en charge
Malgré une meilleure connaissance de la maladie au cours des dernières années, le délai de diagnostic et de prise en charge reste particulièrement long. Les données récentes confirment un retard moyen supérieur à six ans, comparable à celui observé il y a plus d’une décennie (4).
Ce retard s’explique notamment par une méconnaissance de la maladie, une banalisation des symptômes initiaux et un parcours de soins souvent inadapté. En conséquence, de nombreux patients sont encore pris en charge à des stades avancés, avec des lésions déjà fistulisées et cicatricielles.
Cette situation souligne l’importance d’une sensibilisation accrue des cliniciens et d’un repérage précoce des formes débutantes.
Physiopathologie
La maladie de Verneuil est une affection inflammatoire complexe, multifactorielle, impliquant des interactions entre facteurs génétiques, immunologiques et environnementaux.
Elle débute par une occlusion du follicule pileux, qui constitue l’événement initial. Cette obstruction entraîne une dilatation folliculaire, suivie d’une rupture et d’une réaction inflammatoire locale. Une colonisation bactérienne secondaire peut aggraver le processus inflammatoire sans en être la cause principale.
L’immunité innée joue un rôle central, notamment via l’activation de l’inflammasome et la production de cytokines pro-inflammatoires telles que l’IL-1. Par ailleurs, certaines anomalies génétiques, en particulier au niveau de la voie de signalisation Notch ou des complexes de la gamma-sécrétase, ont été identifiées chez certains patients.
Aux stades évolués, l’inflammation chronique conduit à la formation d’abcès, de trajets fistuleux et de remaniements cicatriciels importants.
Hétérogénéité clinique et phénotypique
La maladie de Verneuil se caractérise par une grande variabilité interindividuelle, que ce soit concerant la réponse aux traitements, la sévérité, la topographie des lésions, les comorbidités (tabac, obésité, facteurs hormonaux…). Certains patients présentent des formes peu sévères, limitées et peu évolutives, tandis que d’autres développent des formes rapidement progressives et particulièrement délabrantes.
La détermination de sous-tyopes est importante afin d’identifier les formes agressives, adapter le traitement et éventuellement prédire par la suite l’évolution de l’hidradénite suppurée.
Différents phénotypes cliniques ont été décrits par Canoui‑Poitrine et al. (5) en 2013 :
• LC1 (48%) : forme classique, axillaire et mammaire, prédominant chez la femme, cicatrices hypertrophiques fréquentes
• LC2 (26%) : forme folliculaire, atteinte rétro-auriculaire, prédominance de lésions folliculaires (kystes épidermiques, comédons, kyste pilonidal), souvent associée à un antécédent d’acné sévère, prédominance masculine et chez les fumeurs
• LC3 (26%) : forme glutéale, atteint périnéo-fessière, surtout des papules folliculaires et folliculites, majoritairement chez les fumeurs et IMC plus faibles
D’autres classifications existent, notamment celle de Van der Zee and Jemec (6) décrivant 6 formes : classique, folliculaire, furonculaire, conglobata, syndromique ou bien ectopique.
Par ailleurs, certaines formes s’intègrent dans des syndromes auto-inflammatoires, tels que les syndromes PAPA, PASH ou SAPHO, suggérant un terrain génétique particulier (7).
Cette hétérogénéité souligne la nécessité d’une approche individualisée de la prise en charge.
Nouveaux concepts physiopathologiques
Des travaux récents ont permis d’identifier des lésions histologiques précurseurs des fistules, décrites comme des structures « pseudopod-like » ou « tentacle-like » (8). Ces lésions pourraient représenter un stade intermédiaire entre l’inflammation initiale et la formation des trajets fistuleux.
Leur identification pourrait constituer un marqueur précoce de gravité et ouvrir la voie à de nouvelles stratégies thérapeutiques ciblées.
De plus, la notion d’endotypes émerge, avec des profils immunologiques distincts selon les patients. Par exemple, certaines formes, notamment avec atteinte faciale, seraient associées à une surexpression d’IL-17A et IL-17F, ce qui pourrait orienter les choix thérapeutiques à l’avenir.
Évaluation de la sévérité
L’évaluation de la sévérité repose sur plusieurs scores cliniques.
Le score de Hurley, historiquement utilisé, distingue trois stades selon notamment la présence et l’étendue de fistule. Toutefois, il reste peu sensible aux variations évolutives.
Le score IHS4 est dorénavant l’outil de référence. Il prend en compte le nombre de nodules inflammatoires, d’abcès et de fistules. Il permet de classer la maladie en :
• Forme légère (score < 3)
• Forme modérée (score ≥ 4)
• Forme sévère (score ≥ 11)
Ce score facilite la décision thérapeutique, notamment l’introduction précoce des biothérapies. Par ailleurs, l’évaluation de la qualité de vie est essentielle, compte tenu de l’impact majeur de la maladie sur le plan physique, psychologique et social.
Nouvelles recommandations européennes – Stratégies thérapeutiques
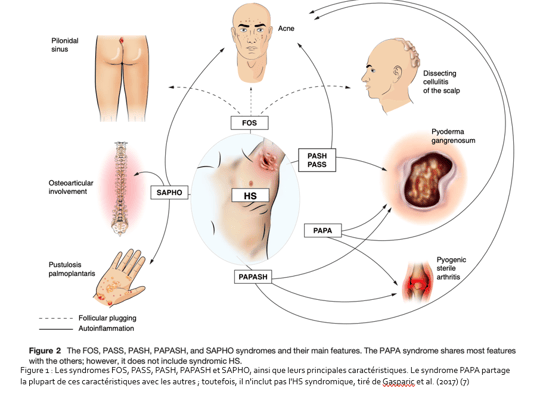
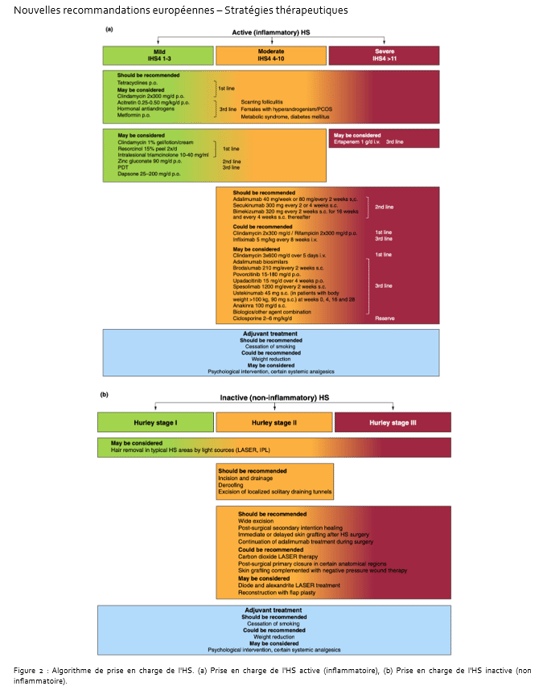
Les nouvelles recommandations européennes utilisent le score IHS4 pour le choix thérapeutique des formes actives et le score de Hurley pour les formes inactives d’hidradénite suppurée.
Formes légères
Les formes mineures peuvent être traitées par : Antibiotiques (tétracyclines, clindamycine), Traitements hormonaux ou métaboliques (spironolactone, metformine), Rétinoïdes (acitrétine).Ces traitements visent à contrôler l’inflammation et à prévenir les poussées.
Formes modérées à sévères
Dans les formes plus avancées, les biothérapies occupent une place centrale : Adalimumab (anti-TNFa), Secukinumab (anti-IL-17A), Bimekizumab (anti-IL-17A/F) De nombreuses molécules sont actuellement en développement, notamment des inhibiteurs de JAK, des anti-IL-1 et des inhibiteurs de la tyrosine kinase de Bruton, témoignant du dynamisme de la recherche dans ce domaine.
Prise en charge des poussées
La gestion des poussées inflammatoires repose sur une approche multimodale, en particulier antibiothérapie, drainage des abcès ou bien injections intra-lésionnelles de corticoïdes. Ces dernières apparaissent particulièrement efficaces pour réduire rapidement l’inflammation et la douleur. Elles peuvent être répétées et associées à d’autres traitements (9).Certaines équipes américaines proposent même des stratégies plus agressives, incluant corticothérapie générale ou biothérapies en phase aiguë.
Place de la chirurgie
La chirurgie est indiquée principalement dans les formes chroniques avec fistules non inflammatoires. Elle permet l’exérèse des lésions séquellaires et peut être réalisée selon différentes techniques, plus ou moins conservatrices.Elle s’intègre souvent dans une stratégie globale associant traitement médical et contrôle de l’inflammation.
Vers des stratégies combinées
L’évolution des connaissances suggère que les approches thérapeutiques doivent être plus précoces, plus ciblées et souvent combinées.L’association de plusieurs modalités thérapeutiques (antibiotiques, biothérapies, injections locales, chirurgie) pourrait permettre un meilleur contrôle de la maladie et limiter sa progression.
Ces stratégies combinées représentent probablement l’avenir de la prise en charge.
Conclusion
La maladie de Verneuil est une pathologie inflammatoire chronique complexe, marquée par une grande hétérogénéité clinique et un retard diagnostique encore trop important.
Une prise en charge précoce, adaptée au profil du patient, est essentielle pour prévenir les formes sévères et améliorer le pronostic.Les avancées récentes en physiopathologie et en thérapeutique permettent d’envisager une médecine plus personnalisée et plus efficace, reposant notamment sur l’identification de phénotypes et d’endotypes spécifiques.
Références
1. Caposiena Caro RD, Chiricozzi A, Sechi A, Molinelli E, Venturini M, Candi E, et al. Flares as dynamic predictive factor of response to adalimumab in hidradenitis suppurativa: real-life data. Ital J Dermatol Venerol. juin 2022;157(3):240‑6. doi:10.23736/S2784-8671.21.07049-3 PubMed PMID: 34159775.
2. Martorell A, Caballero A, González Lama Y, Jiménez-Gallo D, Lázaro Serrano M, Miranda J, et al. Management of patients with hidradenitis suppurativa. Actas Dermosifiliogr. sept 2016;107 Suppl 2:32‑42. doi:10.1016/S0001-7310(17)30007-8 PubMed PMID: 28081768.
3. Marzano AV, Genovese G, Casazza G, Moltrasio C, Dapavo P, Micali G, et al. Evidence for a « window of opportunity » in hidradenitis suppurativa treated with adalimumab: a retrospective, real-life multicentre cohort study. Br J Dermatol. janv 2021;184(1):133‑40. doi:10.1111/bjd.18983 PubMed PMID: 32119111.
4. Samela T, Abeni D, Colonna L, Ciccone D, Di Guardo A, Pupa MB, et al. Diagnostic delay for hidradenitis suppurativa: No change in the 2015–2024 decade. Journal of the European Academy of Dermatology and Venereology. n/a(n/a). doi:10.1111/jdv.70404
5. Canoui-Poitrine F, Thuaut AL, Revuz JE, Viallette C, Gabison G, Poli F, et al. Identification of Three Hidradenitis Suppurativa Phenotypes: Latent Class Analysis of a Cross-Sectional Study. J Invest Dermatol. 1 juin 2013;133(6):1506‑11. doi:10.1038/jid.2012.472 PubMed PMID: 23235532.
6. Van Der Zee HH, Jemec GBE. New insights into the diagnosis of hidradenitis suppurativa: Clinical presentations and phenotypes. Journal of the American Academy of Dermatology. nov 2015;73(5):S23‑6. doi:10.1016/j.jaad.2015.07.047
7. Gasparic J, Theut Riis P, Jemec G b. Recognizing syndromic hidradenitis suppurativa: a review of the literature. Journal of the European Academy of Dermatology and Venereology. 2017;31(11):1809‑16. doi:10.1111/jdv.14464
8. Dunstan RW, Salte KM, Todorović V, Lowe M, Wetter JB, Harms PW, et al. Histologic progression of acne inversa/hidradenitis suppurativa: Implications for future investigations and therapeutic intervention. Exp Dermatol. juin 2021;30(6):820‑30. doi:10.1111/exd.14273 PubMed PMID: 33377546; PubMed Central PMCID: PMC8247901.
9. Cuenca-Barrales C, Montero-Vílchez T, Sánchez-Díaz M, Martínez-López A, Rodríguez-Pozo JÁ, Díaz-Calvillo P, et al. Intralesional Treatments in Hidradenitis Suppurativa: A Systematic Review. Dermatology. 2022;238(6):1084‑91. doi:10.1159/000524121 PubMed PMID: 35477143.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Pr Delphine Staumont-Salle
La dermatite atopique connaît aujourd’hui une véritable révolution thérapeutique, marquée par l’émergence de nombreuses molécules innovantes et une meilleure compréhension des mécanismes physiopathologiques. Dans ce contexte, la prise en charge ne peut plus se limiter à des algorithmes rigides, mais doit s’inscrire dans une démarche individualisée. Trois messages majeurs se dégagent des dernières recommandations françaises (1) : la nécessité de préserver la liberté de prescription, l’évolution des stratégies systémiques et l’intégration de nouvelles cibles thérapeutiques dans une logique de médecine de précision.
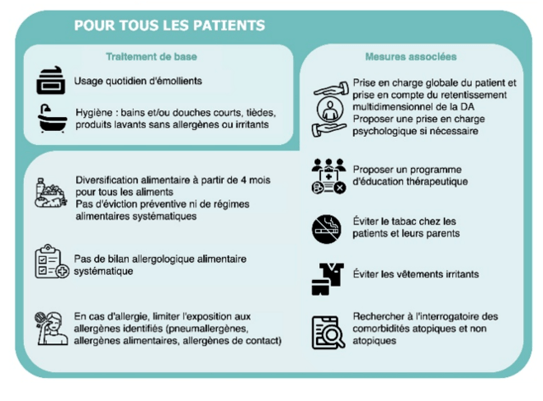
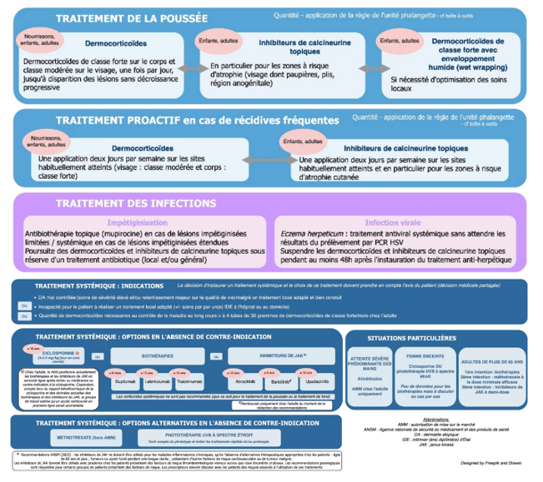
Préserver la liberté de prescription
Les recommandations récentes ont fait le choix délibéré de ne pas imposer de scores stricts ni de seuils précis pour déterminer l’éligibilité aux traitements systémiques. Cette décision repose sur la volonté de maintenir une certaine souplesse dans la pratique clinique. En effet, bien que des scores objectifs et des indicateurs rapportés par les patients (qualité de vie, fardeau du traitement topique) soient pris en compte, ils ne doivent pas enfermer le clinicien dans une approche trop normative.
Cette liberté est essentielle pour permettre une véritable décision médicale partagée avec le patient. Elle évite également les dérives observées dans certains systèmes de santé où l’accès aux traitements innovants dépend de contraintes administratives lourdes et standardisées. Enfin, elle constitue un rempart face à une possible automatisation des décisions thérapeutiques par des outils d’intelligence artificielle, en réaffirmant la place centrale du jugement clinique.
Une redéfinition des stratégies systémiques
Les recommandations actuelles proposent un changement majeur en positionnant au même niveau plusieurs options thérapeutiques systémiques, notamment la ciclosporine, les biothérapies et les inhibiteurs de JAK. Cette approche reflète les données de la littérature, qui ne montrent pas de supériorité nette d’une classe sur une autre en termes d’efficacité globale.
La ciclosporine conserve néanmoins une place importante. Elle reste un traitement particulièrement efficace, notamment en raison de sa rapidité d’action, et doit être utilisée en cures courtes à posologies adaptées d’emblée. Son utilisation est aujourd’hui encadrée par des contraintes de remboursement qui imposent souvent de la considérer systématiquement en première ligne systémique avant d’accéder à d’autres traitements. Les alternatives ne sont généralement envisagées qu’en cas d’échec, d’intolérance ou de contre-indication.L’objectif des recommandations est d’accompagner une évolution vers un accès plus direct aux nouvelles molécules, notamment les inhibiteurs de JAK, sans passer systématiquement par une étape préalable imposée. Cette évolution est actuellement en cours d’évaluation par les autorités de santé.
Maintenir la place des traitements classiques
Malgré l’arrivée de nouvelles options thérapeutiques, les traitements plus anciens conservent toute leur pertinence. La photothérapie, par exemple, reste une option utile pour franchir un cap dans la prise en charge. De même, le méthotrexate peut constituer une alternative intéressante dans certaines situations cliniques.Chez l’adulte, une attention particulière doit être portée au diagnostic différentiel, notamment à la possibilité d’un lymphome cutané T, dont le risque semble légèrement augmenté dans les formes sévères de dermatite atopique. Dans ce contexte, la réalisation de biopsies répétées peut être nécessaire en cas de doute persistant.
Le méthotrexate peut alors représenter une option thérapeutique adaptée, contrairement à certaines biothérapies comme le dupilumab, pour lesquelles des cas de lymphome ont été rapportés, bien que cela reste rare (2,3).
Nouvelles perspectives thérapeutiques
Le nemolizumab et la cible IL-31
Le nemolizumab constitue une avancée majeure en ciblant le récepteur de l’interleukine 31, cytokine clé impliquée dans le prurit. Les études cliniques ont montré une amélioration rapide et significative du prurit, parfois dès les premiers jours de traitement. Par ailleurs, une proportion importante de patients atteint des objectifs cliniques ambitieux, incluant une amélioration des lésions cutanées (4).L’efficacité du traitement se maintient dans le temps, en particulier chez les patients présentant un prurit intense. Le profil de tolérance est globalement favorable, avec peu d’effets indésirables notables. Une attention particulière doit toutefois être portée aux patients asthmatiques, nécessitant une évaluation préalable du contrôle de la maladie.
La voie OX40/OX40L : une stratégie en amont
Une autre voie prometteuse repose sur le ciblage de l’axe OX40/OX40L, qui intervient en amont dans l’activation des lymphocytes T (5). Cette approche pourrait permettre un contrôle plus global de la réponse immunitaire.
Parmi les molécules étudiées, l’amlitelimab présente des résultats encourageants, avec une amélioration progressive des scores cliniques et un profil de tolérance satisfaisant. Un aspect particulièrement innovant réside dans le maintien de l’efficacité après l’arrêt du traitement, suggérant un effet durable sur l’évolution de la maladie (6).
Cette approche s’inscrit dans un changement de paradigme, passant d’une logique de contrôle symptomatique à une stratégie de modification de la maladie, avec l’objectif ultime d’obtenir une rémission sans traitement.
Les innovations en traitements topiques
Les traitements topiques continuent également d’évoluer. Le ruxolitinib en crème, déjà disponible dans certaines indications, montre une efficacité notable dans la dermatite atopique modérée, avec un excellent profil de tolérance. Son arrivée prochaine en Europe est attendue.Par ailleurs, le delgocitinib, inhibiteur de JAK topique, constitue une avancée importante dans le traitement de l’eczéma chronique des mains. Il présente une efficacité comparable, voire supérieure, à celle de traitements systémiques comme l’alitrétinoïne, tout en offrant les avantages d’une administration locale (7).
Vers une médecine personnalisée et combinatoire
Le choix thérapeutique devient aujourd’hui de plus en plus complexe et ne peut plus se résumer à une stratégie unique. Il repose sur une analyse fine du profil du patient, incluant les caractéristiques cliniques, l’impact sur la qualité de vie, et potentiellement des éléments biologiques ou immunologiques.Il est désormais envisageable d’adapter le traitement non seulement au patient, mais aussi aux différentes lésions qu’il présente, en combinant plusieurs approches thérapeutiques. Cette évolution reflète l’entrée dans une véritable médecine personnalisée.Malgré les progrès technologiques, cette complexité décisionnelle souligne l’importance du rôle du clinicien. La prise en charge de la dermatite atopique reste un exercice d’équilibre, nécessitant une expertise médicale et une relation étroite avec le patient, qui ne peut être entièrement remplacée par des outils d’intelligence artificielle.
Conclusion
La dermatite atopique est entrée dans une nouvelle ère thérapeutique, marquée par une diversification des options et une ambition accrue en termes de contrôle de la maladie. L’objectif n’est plus seulement d’obtenir une amélioration clinique, mais de viser une rémission durable, voire une absence de traitement à long terme (8). Dans ce contexte, la liberté de prescription, la personnalisation des stratégies et la décision médicale partagée apparaissent comme des éléments essentiels pour optimiser la prise en charge des patients.
Références
1. Sigg N, Leducq S, Barbarot S, Sallé-Staumont D, Ertus C, Hurson C, et al. French guidelines for the management of atopic dermatitis. J Eur Acad Dermatol Venereol. janv 2026;40(1):e52‑6. doi:10.1111/jdv.20782 PubMed PMID: 40539572; PubMed Central PMCID: PMC12723561.
2. Thyssen JP, Halling AS, Schmid-Grendelmeier P, Guttman-Yassky E, Silverberg JI. Comorbidities of atopic dermatitis-what does the evidence say? J Allergy Clin Immunol. mai 2023;151(5):1155‑62. doi:10.1016/j.jaci.2022.12.002 PubMed PMID: 36621338.
3. Amatore F, Neildez M, de Masson A, Battistella M, Tauber M, Ingen-Housz-Oro S, et al. Cutaneous T-cell lymphomas and dupilumab for atopic dermatitis: A systematic review and expert consensus. J Eur Acad Dermatol Venereol. 12 mars 2026. doi:10.1111/jdv.70407 PubMed PMID: 41821352.
4. Nemolizumab with concomitant topical therapy in adolescents and adults with moderate-to-severe atopic dermatitis (ARCADIA 1 and ARCADIA 2): results from two replicate, double-blind, randomised controlled phase 3 trials. The Lancet. 3 août 2024;404(10451):445‑60. doi:10.1016/S0140-6736(24)01203-0
5. Guttman-Yassky E, Croft M, Geng B, Rynkiewicz N, Lucchesi D, Peakman M, et al. The role of OX40 ligand/OX40 axis signalling in atopic dermatitis. Br J Dermatol. 18 sept 2024;191(4):488‑96. doi:10.1093/bjd/ljae230 PubMed PMID: 38836560.
6. Weidinger S, Blauvelt A, Papp KA, Reich A, Lee CH, Worm M, et al. Phase 2b randomized clinical trial of amlitelimab, an anti-OX40 ligand antibody, in patients with moderate-to-severe atopic dermatitis. J Allergy Clin Immunol. avr 2025;155(4):1264‑75. doi:10.1016/j.jaci.2024.10.031 PubMed PMID: 39522654.
7. Giménez-Arnau AM, Pinter A, Sondermann W, Reguiai Z, Woolf R, Lynde C, et al. Efficacy and safety of topical delgocitinib cream versus oral alitretinoin capsules in adults with severe chronic hand eczema (DELTA FORCE): a 24-week, randomised, head-to-head, phase 3 trial. Lancet. 10 mai 2025;405(10490):1676‑88. doi:10.1016/S0140-6736(25)00001-7 PubMed PMID: 40252681.
8. Lommatzsch M, Blumchen K, Beck LA, Bousquet J, Brusselle GG, Fokkens WJ, et al. Roads to remission: evolving treatment concepts in type 2 inflammatory diseases. EClinicalMedicine. févr 2025;80:103050. doi:10.1016/j.eclinm.2024.103050 PubMed PMID: 39867971; PubMed Central PMCID: PMC11764424.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Dr Bruno MATARD
Données physiopathologiques émergentes
Des données récentes suggèrent que la testostérone pourrait jouer un rôle dans l’obstruction folliculaire, ce qui laisse envisager une augmentation de la fréquence de certaines folliculites inflammatoires du cuir chevelu dans les années à venir. Par ailleurs, des avancées importantes en immunopathologie permettent de mieux comprendre les mécanismes sous-jacents de la folliculite décalvante, qui apparaît désormais comme une maladie à profil immunitaire de type Th17. Une étude en immunomarquage a notamment mis en évidence une surexpression significative de l’interleukine 17 dans la peau lésionnelle, associée à une augmentation du nombre de mastocytes, suggérant un rôle actif de ces cellules dans l’inflammation locale (1).
Diagnostic différentiel entre lichen plan pilaire et folliculite décalvante
Le diagnostic différentiel entre le lichen plan pilaire et la folliculite décalvante demeure particulièrement difficile en pratique clinique, en raison de similitudes histologiques importantes. Une controverse récente propose l’existence d’un spectre phénotypique entre ces deux entités, fondée sur leur possible coexistence chez certains patients. Toutefois, cette hypothèse est contestée, étant donné les études d’immunomarquage qui ont montré des profils immunitaires distincts entre ces deux pathologies. De plus, les aspects cliniques dits « lichénoïdes » observés après traitement d’une folliculite décalvante correspondent en réalité à des formes peu évolutives avec persistance d’un érythème et d’une hyperkératose, et ne justifient pas l’individualisation d’un spectre commun (2). Cette distinction est essentielle, car elle conditionne directement la stratégie thérapeutique.
Controverses thérapeutiques et place de l’isotrétinoïne
Certaines publications récentes ont proposé des recommandations thérapeutiques incluant l’isotrétinoïne comme traitement de première intention dans les formes modérées ou résistantes de folliculite décalvante. Néanmoins, ces propositions reposent sur des études de faible niveau de preuve, souvent rétrospectives, avec des effectifs réduits et des biais méthodologiques importants. Certaines données rapportées, telles qu’un taux élevé de repousse capillaire dans une alopécie cicatricielle, apparaissent difficilement plausibles. L’expérience clinique, notamment sur de larges cohortes suivies dans des centres spécialisés, ne montre pas d’efficacité significative de l’isotrétinoïne dans cette indication, ce qui conduit à ne pas recommander son utilisation en l’absence de données plus robustes (3).
Facteurs iatrogènes et interactions immunologiques
Des cas de folliculite décalvante induite par le dupilumab ont été décrits, suggérant une interaction complexe entre les différentes voies immunitaires (4). Il est probable que l’inhibition de la voie Th2 par ce traitement puisse moduler indirectement la voie Th17, favorisant ainsi l’émergence de dermatoses inflammatoires telles que la folliculite décalvante. Ce phénomène s’inscrit dans un contexte plus large d’apparition de maladies inflammatoires cutanées sous biothérapies ciblées.
Risque carcinologique dans les folliculites chroniques
La survenue d’un carcinome épidermoïde sur une folliculite décalvante constitue une complication rare mais potentiellement grave, avec un nombre limité de cas rapportés dans la littérature. Dans les contextes d’inflammation chronique, ces tumeurs présentent un risque métastatique particulièrement élevé. Le diagnostic est souvent difficile en raison de l’aspect cicatriciel du cuir chevelu, ce qui impose une vigilance clinique accrue et un recours facilité à la biopsie devant toute lésion proliférante suspecte.
Approches chirurgicales dans les formes stabilisées
Les greffes folliculaires, longtemps considérées comme risquées dans ce contexte inflammatoire, semblent aujourd’hui pouvoir être envisagées chez des patients sélectionnés présentant une maladie peu active et stable depuis plusieurs mois. Les résultats rapportés montrent une bonne survie des greffons et une satisfaction des patients, bien que le risque de récidive à long terme doive être clairement expliqué (5). Par ailleurs, des techniques chirurgicales innovantes associant exérèse complète des zones atteintes et suture sous tension avec répartition des contraintes ont permis d’obtenir des résultats prometteurs sans récidive à moyen terme, chez des patients soigneusement sélectionnés (6).
Place des biothérapies
Les biothérapies représentent une option thérapeutique en cours d’évaluation dans les folliculites inflammatoires sévères du cuir chevelu. Les anti-TNF sont actuellement les traitements les mieux documentés, avec des résultats montrant une efficacité chez environ la moitié des patients à six mois. Les autres biothérapies ont été utilisées de manière plus ponctuelle, sans données suffisantes pour conclure à leur efficacité. Ces observations soulignent la nécessité de conduire des études contrôlées afin de mieux définir leur place dans la stratégie thérapeutique.
Références
1. Franciozi AB, Sotto MN, Rivitti-Machado MCM, Pagliari C, Doche I. Evidence of interleukin-17-secreting mast cells in scalp lesions of folliculitis decalvans points to new therapeutic targets in recalcitrant lesions. Clin Exp Dermatol. 24 févr 2025;50(3):629‑31. doi:10.1093/ced/llae421 PubMed PMID: 39388582.
2. Matard B, Cavelier Balloy B, Assouly P, Reygagne P. It has the Erythema of a Lichen Planopilaris, it has the Hyperkeratosis of a Lichen Planopilaris, but it is Not a Lichen Planopilaris: About the “Lichen Planopilaris-Like” Form of Folliculitis Decalvans. The American Journal of Dermatopathology. mars 2021;43(3):235. doi:10.1097/DAD.0000000000001758
3. Waśkiel-Burnat A, Starace M, Iorizzo M, Katoulis A, Apalla Z, Asfour L, et al. Management of folliculitis decalvans: The EADV task force on hair diseases position statement. J Eur Acad Dermatol Venereol. août 2025;39(8):1385‑94. doi:10.1111/jdv.20687 PubMed PMID: 40230058.
4. Sorrentino P, Malaspina M, Tancredi V, Argenziano G, Di Brizzi EV. Dissecting Cellulitis of the Scalp Associated With Dupilumab: A Paradoxical Neutrophilic Reaction. Int J Dermatol. 12 janv 2026. doi:10.1111/ijd.70277 PubMed PMID: 41524532.
5. Cova-Martín R, Perez-Bootello J, Hermosa-Gelbard A, Gomez Zubiaur A, Pigem Gasos R, Vaño-Galvan S, et al. Hair transplantation in folliculitis decalvans: Outcome description in a multicentre series of 11 patients. J Eur Acad Dermatol Venereol. oct 2025;39(10):e845‑9. doi:10.1111/jdv.20558 PubMed PMID: 39927701.
6. Umar S, Waterman A, Ton D, Shitabata P. Refractory Folliculitis Decalvans Treatment Success with a Novel Surgical Excision Approach Using Guarded High-Tension Sutures. Clin Cosmet Investig Dermatol. 2023;16:2381‑90. doi:10.2147/CCID.S422077 PubMed PMID: 37675182; PubMed Central PMCID: PMC10478779.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Dr Philippe ASSOULY
PELADE
Évaluation de la sévérité et facteurs pronostiques
La sévérité de la pelade est évaluée à l’aide du score SALT. Une pelade est considérée comme sévère lorsque le SALT est supérieur à 50 et très sévère au-delà de 95. En pratique, il existe un décalage entre cette théorie et la réalité clinique où l’impact sur la qualité de vie peut être important même pour des atteintes moins étendues, c’est pour cela que les critères des études se basent plutôt sur un SALT 10.
La repousse dépend principalement de deux facteurs : l’étendue de l’atteinte et son ancienneté. Certaines pelades très étendues peuvent néanmoins repousser rapidement (formes ADTA), tandis que des formes anciennes dites biphasiques présentent une raréfaction folliculaire importante, limitant fortement les possibilités de repousse.
Dans les formes anciennes (plus de 6 ans), une évaluation complémentaire peut être réalisée par biopsies pour estimer la densité folliculaire et l’inflammation, éventuellement associées à une échographie du cuir chevelu et à un test thérapeutique par corticoïdes retard.
Inhibiteurs de JAK : traitements de référence récents
Deux inhibiteurs de JAK disposent actuellement d’une AMM : le baricitinib et le ritlecitinib (1,2). Ils sont indiqués pour des atteintes supérieures à 50 % (SALT 50).
À 52 semaines, environ 30 à 40 % des patients atteignent un SALT 10 dans les formes sévères sous inhibiteur de JAK, contre environ 20 % dans les formes universelles. À 24 mois, les données sont plus limitées pour le baricitinib, mais le ritlecitinib montre environ 40 % de réponses dans les formes sévères et 30 % dans les formes très étendues. Une amélioration des sourcils est observée dans plus de 30 % des cas.
Les réponses sont variables (3,4) : certains patients présentent une repousse rapide et durable, tandis que d’autres ne répondent pas. L’arrêt du traitement expose à une rechute rapide, souvent en moins de 8 semaines. Sous traitement continu, environ 10 % des patients rechutent dans l’année.
La réduction de dose (baricitinib 4 mg à 2 mg) peut entraîner une perte d’efficacité, et la reprise ne garantit pas une réponse identique. L’augmentation de dose de 2 à 4 mg améliore généralement les résultats.
Comment choisir entre les deux molécules ? Elles ont une efficacité comparable. Le ritlecitinib est prescrit dès 12 ans avec une ordonnance simple, tandis que le baricitinib nécessite une prescription hospitalière initiale mais bénéficie d’un meilleur remboursement.
Autres inhibiteurs de JAK et perspectives
D’autres molécules sont en développement : le deuruxolitinib (disponible aux États-Unis), l’upadacitinib (en attente d’AMM), ou encore l’ivarmacitinib. Les formes topiques n’ont pas montré d’efficacité à ce jour.
Le switch entre inhibiteurs de JAK est fréquent en pratique mais repose sur peu de données solides, les études étant souvent associées à d’autres traitements (minoxidil oral, corticothérapie).
Place des autres traitements
La corticothérapie systémique reste le traitement le plus rapidement efficace, souvent utilisée en association pour initier une repousse. Sur le plan local, les dermocorticoïdes de classe IV permettent une repousse dans environ 20 % des pelades sévères.
Les injections de triamcinolone (8 à 10 mg) constituent un traitement de référence, notamment pour les sourcils dans les formes universelles (5).
La photothérapie (PUVA) n’a pas démontré de bénéfice clair. L’immunothérapie de contact montre environ 20 % de repousse complète dans les formes très sévères, malgré l’absence d’études en double aveugle (6).
Le méthotrexate seul est peu efficace, mais son association à la corticothérapie améliore les résultats (jusqu’à 31 % de SALT 10 à un an), restant néanmoins inférieur aux inhibiteurs de JAK (7).
Le minoxidil est recommandé en association, notamment par voie orale, mais agit principalement en épaississant les cheveux existants.
Les traitements comme le PRP ou le microneedling restent très discutables. Le dupilumab peut être envisagé en cas d’atopie associée.
Aspects pratiques et prise en charge globale
Les effets indésirables des inhibiteurs de JAK restent rassurants à ce jour. Les prothèses capillaires bénéficient désormais d’un meilleur remboursement, y compris pour les pelades, avec une prise en charge partielle pour les modèles en cheveux naturels. Elles sont être prescrites sur ordonnance simple.
LICHEN PLAN PILAIRE
Formes cliniques et principes généraux
Le lichen plan pilaire comprend deux formes principales : la forme classique et l’alopécie frontale fibrosante (AFF). Il s’agit d’une alopécie cicatricielle, sans possibilité de repousse une fois la destruction folliculaire installée, ce qui nécessite une prise en charge précoce et un fort engagement du patient.
Traitements de la forme classique
Il n’existe pas de consensus thérapeutique clair. Les traitements de première ligne reposent sur les dermocorticoïdes et les injections locales de corticoïdes, associés éventuellement aux cyclines.
La corticothérapie systémique à forte dose reste le traitement de référence en phase active. Le méthotrexate est utilisé en cas de résistance ou de contre-indication.
Certains traitements doivent être relativisés, notamment l’hydroxychloroquine, faute de données probantes. Les anti-IL17 et les inhibiteurs de JAK n’ont pas démontré d’efficacité convaincante à ce jour. Des molécules comme le deucravacitinib ou le brepocitinib suscitent un intérêt, mais les données restent limitées.
Les traitements de troisième ligne comme le cyclophosphamide ou le mycophénolate mofétil ne sont plus recommandés. Les greffes capillaires (FUE) peuvent être envisagées lorsque la maladie est stabilisée, sous couvert d’un traitement d’entretien.
Le suivi repose sur une documentation photographique régulière, essentielle pour évaluer l’évolution.
Alopécie frontale fibrosante (AFF)
La prise en charge de l’AFF est similaire à celle de la forme classique. Les inhibiteurs de la 5-alpha réductase sont largement discutés, sans preuve formelle d’efficacité.
Les inhibiteurs de JAK ne sont pas convaincants actuellement, mais restent à l’étude. Les greffes capillaires peuvent également être proposées dans les formes stabilisées.
Références
1. King B, Zhang X, Harcha WG, Szepietowski JC, Shapiro J, Lynde C, et al. Efficacy and safety of ritlecitinib in adults and adolescents with alopecia areata: a randomised, double-blind, multicentre, phase 2b-3 trial. Lancet. 6 mai 2023;401(10387):1518‑29. doi:10.1016/S0140-6736(23)00222-2 PubMed PMID: 37062298.
2. Piliang M, Soung J, King B, Shapiro J, Rudnicka L, Farrant P, et al. Efficacy and safety of the oral Janus kinase 3/tyrosine kinase expressed in hepatocellular carcinoma family kinase inhibitor ritlecitinib over 24 months: integrated analysis of the ALLEGRO phase IIb/III and long-term phase III clinical studies in alopecia areata. Br J Dermatol. 24 janv 2025;192(2):215‑27. doi:10.1093/bjd/ljae365 PubMed PMID: 39432738.
3. Senna M, Mostaghimi A, Ohyama M, Sinclair R, Dutronc Y, Wu WS, et al. Long-term efficacy and safety of baricitinib in patients with severe alopecia areata: 104-week results from BRAVE-AA1 and BRAVE-AA2. J Eur Acad Dermatol Venereol. mars 2024;38(3):583‑93. doi:10.1111/jdv.19665 PubMed PMID: 38391212.
4. Ko JM, Mayo TT, Bergfeld WF, Dutronc Y, Yu G, Ball SG, et al. Clinical Outcomes for Uptitration of Baricitinib Therapy in Patients With Severe Alopecia Areata: A Pooled Analysis of the BRAVE-AA1 and BRAVE-AA2 Trials. JAMA Dermatol. 1 sept 2023;159(9):970‑6. doi:10.1001/jamadermatol.2023.2581 PubMed PMID: 37556146; PubMed Central PMCID: PMC10413213.
5. Gregoire S, McIntosh B, Sanchez K, Biba U, Mostaghimi A. Local Corticosteroids for Alopecia Areata: A Narrative Review. Dermatol Ther (Heidelb). juill 2025;15(7):1607‑31. doi:10.1007/s13555-025-01421-2 PubMed PMID: 40323545; PubMed Central PMCID: PMC12126370.
6. Mateos-Haro M, Novoa-Candia M, Sánchez Vanegas G, Correa-Pérez A, Gaetano Gil A, Fernández-García S, et al. Treatments for alopecia areata: a network meta-analysis. Cochrane Database Syst Rev. 23 oct 2023;10(10):CD013719. doi:10.1002/14651858.CD013719.pub2 PubMed PMID: 37870096; PubMed Central PMCID: PMC10591288.
7. Joly P, Lafon A, Houivet E, Donnadieu N, Richard MA, Dupuy A, et al. Efficacy of Methotrexate Alone vs Methotrexate Plus Low-Dose Prednisone in Patients With Alopecia Areata Totalis or Universalis: A 2-Step Double-Blind Randomized Clinical Trial. JAMA Dermatol. 1 avr 2023;159(4):403‑10. doi:10.1001/jamadermatol.2022.6687 PubMed PMID: 36884234; PubMed Central PMCID: PMC9996454.
Rédigé par Camille LOISEAU (Interne en Dermatologie à Lille)
Par Dr Pascal REYGAGNE
Finastéride
Contexte réglementaire et alerte récente sur le finastéride
Une alerte récente de l’ANSM et d’associations de patients a concerné les effets secondaires potentiels du finastéride, en particulier les troubles psychiatriques. Quelques cas d’idées suicidaires ont été rapportés dans les bases de pharmacovigilance. Ces événements restent rares et leur fréquence est difficile à déterminer avec précision. Sur environ 270 millions d’années-patient, 313 cas d’idées suicidaires ont été identifiés. Un seul suicide a été rapporté dans ce contexte. Ces chiffres sont très inférieurs à ceux attendus dans la population générale et permet de relativiser.
Cette situation a conduit à une réévaluation du rapport bénéfice-risque par le PRAC.
Les conclusions indiquent que le rapport bénéfice-risque reste positif dans toutes les indications, y compris dans l’alopécie androgénétique masculine à la dose de 1 mg par jour.
Les autorités ont mis en place des mesures pour renforcer l’information des patients et des professionnels de santé. Des avertissements ont été ajoutés sur les boîtes de finastéride, des cartes d’information destinées aux patients ont également été introduites.
Une attestation d’information partagée, concernant uniquement le finastéride dosé à 1 mg, doit désormais être signée par le médecin et le patient. Cette attestation est obligatoire pour les primo-prescriptions à partir du 16 avril et devient obligatoire pour les renouvellements à partir du 7 juin. Elle est valable pour une durée d’un an et doit être renouvelée chaque année. À noter que les effets secondaires surviennent le plus souvent au cours du premier mois de traitement.
Données récentes de sécurité du finastéride
Les études récentes apportent des éléments rassurants concernant la sécurité du finastéride. Une analyse issue de la base TriNetX (1) a inclus 25 000 patients traités et 86 000 patients contrôles. Le risque de syndrome dépressif n’était pas augmenté chez les patients traités. L’ORR était de 0,9, ce qui ne suggère pas de sur-risque de dépression.
Les données de pharmacovigilance de la FDA montrent une meilleure tolérance de la forme topique (2). Par ailleurs, aucun suicide n’a été rapporté avec la forme topique et très peu de cas d’idées suicidaires ont été observés avec cette forme.
Finastéride topique : une alternative récente
Le finastéride topique est une forme récemment commercialisée. Il s’applique une fois par jour sur le cuir chevelu. Le dispositif d’application permet de limiter la diffusion du produit en dehors de la zone traitée.
Les études montrent une augmentation du nombre de cheveux comparable entre les formes orale et topique (3). La forme orale entraîne une augmentation d’environ 18 cheveux. La forme topique entraîne une augmentation d’environ 16 cheveux. L’efficacité de la forme topique est donc proche de celle de la forme orale.
Les effets indésirables sexuels sont comparables au placebo avec la forme topique. Ils sont légèrement plus fréquents avec la forme orale. La concentration plasmatique avec la forme topique est inférieure à 1 % de celle observée avec la forme orale. L’efficacité apparaît après 3 à 6 mois de traitement mais les bénéfices disparaissent en 6 à 12 mois après l’arrêt.
Finastéride et cancer du sein
Les données disponibles ne montrent pas d’augmentation du risque de cancer du sein sous finastéride. Les études chez l’homme sont rassurantes. Une étude épidémiologique récente chez la femme montre un odds ratio proche de 1 (4). Ces résultats suggèrent l’absence de lien significatif entre finastéride et cancer du sein.
Minoxidil
Minoxidil oral à faible dose : une nouvelle tendance
Le minoxidil oral à faible dose est utilisé de plus en plus fréquemment depuis 2020.
Plusieurs études ont confirmé son intérêt dans l’alopécie androgénétique (5–8).
Une étude récente a comparé des doses de 2,5 mg et de 5 mg chez l’homme.
Une amélioration clinique a été observée chez environ 60 % des patients.
Cette efficacité est comparable à celle du finastéride oral et du minoxidil topique.
Les données montrent l’absence d’impact significatif sur la pression artérielle et le pouls.
Avantages et effets secondaires du minoxidil oral
Le minoxidil oral présente plusieurs avantages pratiques. Il n’entraîne pas d’irritation cutanée, est plus simple d’utilisation et favorise une meilleure observance. Il permet également la réalisation de colorations capillaires sans contrainte et constitue une alternative en cas d’allergie au minoxidil topique.
Les effets secondaires incluent une hypertrichose, principalement chez la femme, ainsi que des hypotensions orthostatiques, des œdèmes. Des symptômes cardiovasculaires rares comme des palpitations ou une tachycardie peuvent aussi apparaître.
Posologie et surveillance du minoxidil oral
Chez la femme, la dose initiale recommandée est de 0,5 mg par jour et peut être augmentée jusqu’à 1,25 mg dans certains cas. Chez l’homme, la dose initiale est de 2,5 mg par jour et peut être augmentée jusqu’à 5 mg par jour (9).
La surveillance repose uniquement sur l’examen clinique. Il est recommandé de surveiller le poids, la tension artérielle et le pouls, rechercher des signes de palpitations, de céphalées ou d’œdèmes. Aucune surveillance biologique n’est nécessaire.
Chez les patients de plus de 65 ans, le profil de sécurité reste globalement favorable.
Une prudence est recommandée en cas d’antécédents d’arythmie.
Thérapies combinées
Une étude italienne (10) a évalué l’association de finastéride topique et de minoxidil.
Cette association a montré une efficacité supérieure au minoxidil seul. La qualité méthodologique de cette étude reste limitée et ces résultats doivent être interprétés avec prudence.
Références
1. Neubauer Z, Ong MM, Lipner SR. No increased risk of mood disorders in male androgenetic alopecia patients treated with dutasteride and finasteride: A retrospective cohort database study. J Am Acad Dermatol. juill 2025;93(1):197‑9. doi:10.1016/j.jaad.2025.03.068 PubMed PMID: 40158535.
2. Gupta AK, Talukder M, Keene SA, Bamimore MA. Is the Safety of Finasteride Correlated With Its Route of Administration: Topical Versus Oral? A Pharmacovigilance Study With Data From the United States Food and Drug Administration Adverse Event Reporting System. Int J Dermatol. janv 2026;65(1):108‑18. doi:10.1111/ijd.17957 PubMed PMID: 40662444; PubMed Central PMCID: PMC12712763.
3. Piraccini BM, Blume-Peytavi U, Scarci F, Jansat JM, Falqués M, Otero R, et al. Efficacy and safety of topical finasteride spray solution for male androgenetic alopecia: a phase III, randomized, controlled clinical trial. J Eur Acad Dermatol Venereol. févr 2022;36(2):286‑94. doi:10.1111/jdv.17738 PubMed PMID: 34634163; PubMed Central PMCID: PMC9297965.
4. Chen LC, Hsieh TYJ, Senna MM. 5α-reductase inhibitor exposure for dermatologic conditions does not increase the risk of female breast or gynecologic cancers: A population-based propensity score-matched cohort study. J Am Acad Dermatol. févr 2025;92(2):343‑5. doi:10.1016/j.jaad.2024.10.023 PubMed PMID: 39442887.
5. Jimenez-Cauhe J, Saceda-Corralo D, Rodrigues-Barata R, Hermosa-Gelbard A, Moreno-Arrones OM, Fernandez-Nieto D, et al. Effectiveness and safety of low-dose oral minoxidil in male androgenetic alopecia. J Am Acad Dermatol. août 2019;81(2):648‑9. doi:10.1016/j.jaad.2019.04.054 PubMed PMID: 31054970.
6. Randolph M, Tosti A. Oral minoxidil treatment for hair loss: A review of efficacy and safety. J Am Acad Dermatol. mars 2021;84(3):737‑46. doi:10.1016/j.jaad.2020.06.1009 PubMed PMID: 32622136.
7. Villani A, Fabbrocini G, Ocampo-Candiani J, Ruggiero A, Ocampo-Garza SS. Review of oral minoxidil as treatment of hair disorders: in search of the perfect dose. J Eur Acad Dermatol Venereol. juill 2021;35(7):1485‑92. doi:10.1111/jdv.17216 PubMed PMID: 33660357.
8. Vañó-Galván S, Pirmez R, Hermosa-Gelbard A, Moreno-Arrones ÓM, Saceda-Corralo D, Rodrigues-Barata R, et al. Safety of low-dose oral minoxidil for hair loss: A multicenter study of 1404 patients. J Am Acad Dermatol. juin 2021;84(6):1644‑51. doi:10.1016/j.jaad.2021.02.054 PubMed PMID: 33639244.
9. Carvalho Fonseca LP, Miot HA, Prescendo Chaves CR, Müller Ramos P. Oral minoxidil 2.5 mg versus 5 mg for male androgenetic alopecia: A double-blind randomized clinical trial. J Am Acad Dermatol. janv 2026;94(1):316‑8. doi:10.1016/j.jaad.2025.09.031 PubMed PMID: 40962189.
10. Rossi A, Magri F, D’Arino A, Pigliacelli F, Muscianese M, Leoncini P, et al. Efficacy of Topical Finasteride 0.5% vs 17α-Estradiol 0.05% in the Treatment of Postmenopausal Female Pattern Hair Loss: A Retrospective, Single-Blind Study of 119 Patients. Dermatol Pract Concept. 2020;10(2):e2020039. doi:10.5826/dpc.1002a39 PubMed PMID: 32363101; PubMed Central PMCID: PMC7190559.
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
N’OUBLIEZ PAS LES REVALORISATIONS
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
Par Dr Nicole Jouan & Dr Florence Corgibet
Prise en charge de la dermatite atopique (DA).
Les nouvelles recommandations mettent au même plan la ciclosporine, les biothérapies (dupilmab, lebrikizumab,tralokinumab et nevolizumab) et les JAK inhibiteurs (abrocitinib, baricitinib, upadacinitib).
En cas de rémission complète ou quai complète sous traitement systématique :
Le MTX est une alternative hors AMM en seconde intention après les biothérapies chez les adultes de plus de 65 ans à dose minimale efficace
Lymphomes en cas de DA sous dupilumab.
Une revue de la littérature montre que les caractéristiques des lymphomes cutanés diagnostiqués sous dupilumab sont :
Pour un patient avec Da chez qui on envisage une mise sous dupilumab il faut se méfier si le début de la DA est tardif (>40 ans), s’il n’y a pas d’ATCD personnel d’atopie et si les caractéristiques cliniques sont atypiques. Ne pas hésiter à faire une biopsie et éviter de prescrire du dupilumab, la ciclosprine et les JAKi. Les alternatives sont le MTX et la photothérapie. Il n’y a pas assez de données concernant les autres biothérapies anti-Th2.
L’eczéma chronique des mains.
Le delgocitinib (Anzupgo crème 2 fois par jour) est indiqué dans tous les eczémas chroniques des mains allergique ou atopiques, en seconde ligne après échec des dermocorticoïdes. Il est remboursé depuis février 2026, Dans les essais, le delgocitinib est plus efficace que l’alitrétinoïne.
Les médicaments en accès direct, ordonnance avec mention « prescription au titre de l’accès direct »
Le prurigo nodulaire de l’adulte nécessite un TTT systémique en cas d’inefficacité des TTT locaux car le prurit chronique (> 6 semaines) est une maladie chronique qui est responsable d’une hyperexcitabilité neuronale ce qui donne un fonctionnement cérébral envahi. Les 2 médicaments ayant eu l’AMM sont le dupilumab (Dupixent à la même dose que la DA) et le nemolizumab (Nemluvio à 60 mg à l’induction puis 30 mg toutes les 4 semaines pendant 16 semaines puis toutes les 8 semaines en entretien).
Le prurit des dialysés a un nouveau médicament le Difelikefaline IV à faire lors des dialyses (agoniste des récepteurs opioïdes kappa). La prescription ne peut être faite que par les dermatologues et les néphrologues.
Le prurit cholestatique. Sa prise en charge est transformée par :
Le vitiligo.
Le ruxolitinib associé aux UVBTL01 est efficace et la tolérance est bonne. La photothérapie UVB à domicile est possible avec des des lampes type dermafix 1000 ou 2000 (www.dermafix.fr).
Pelade sévére adulte.
Deux AMM pour les antiJAK sont :
FINASTERIDE ORALE
A partir du 16 avril 2026 il faudra faire signer une attestation d’information partagée. Elle sera à renouveler tous les ans.
Finasteride topique dans l’alopécie androgénogénétique légère à modérée. Son efficacité est proche de celle du finastéride oral (1 à 4 pulvérisations par jour sur cuir chevelu sec). Sa concentration plasmatique est au moins 100 fois inférieure à la forme per os 1 mg/j et ses effets indésirables (prurit 2% et érythème 2%) sont inférieures à ceux du minoxidil.
Minoxidil orale et AAG.
Le lonoten existe en comprimés à 5 et 10 mg. Il est Hors AMM.
Chez la femme, les posologies sont de 0,5 à 2 mg et chez l’homme de 2,5 à 5 mg/j. Il faut faire des préparations magistrales). Les contre-indications sont les péricardites, l’insuffisance cardiaque, les troubles du rythme et les ATCD d’IDM….
Les effets indésirables sont un effet antabuse, un effet shedding, hypotension orthostatique, l’œdème des paupières. Il faut donc surveiller la TA, l’apparition d’une dyspnée, la prise de poids et l’apparition d’une tachycardie.
Il faut baisser la dose si mauvaise tolérance ou apparition d’une hypertrichose.
Les biologiques de l’hidradénite suppurée :
A venir : remibrutimib (voie lympho B), isokibep (IL17), povorcitinib, upadacitinib, lutikizumab anti IL1 alpha et beta, ruxolitinib topique.
Les biothérapies permettent uniquement la prise en charge de l’inflammation. Il faut donc les commencer tôt et traiter fort. Pour la prise en charge des tunnels et fistules, il faut associer un TTT chirurgical.
Psoriasis et ses comorbidités et AR GLP1 (agonistes du glucagon like peptide).
Une étude rétrospective à partir de données de la cohorte TriNetX montre que les AR GLP1 étaient associés chez les patients psoriasiques à une chute très significative de la mortalite2 globale (-78%), MACE (-44%) et des addictions (-49%) sans augmentation d’effet secondaire attribué aux TTT. Des études prospectives sont en cours notamment en association à des biothérapies du psoriasis modéré à sévère.
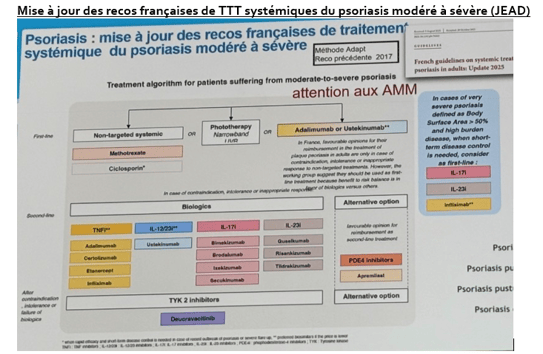
Si votre patient a un risque cardiovasculaire important le méthotrexate est possible. S’il a un haut risque les anti-TNF (sauf insuffisance cardiaque) ou anti IL 17.
Il faut éviter les antis IL 23.
Vous pouvez calculer les scores sur le site : medicalcul.free.fr
Réductions des doses dans le psoriasis.
L’Etude BeNeBio montre qu’une réduction de dose jusqu’à 50% des anti IL 17et 23 pour des patients psoriasiques avec une activité de maladie faible et stable est non-inférieure aux doses habituelles.
A faire après au moins un an de TTT.
Nouveaux TTT du psoriasis.
Les molécules orales.
Methotrexate chez l’homme et conception : mise à jour en janvier 2025. Le ttt par MTX peut être poursuivi chez un patient qui désire concevoir. Il n’y a pas de suivi particulier à faire chez la femme enceinte d’un patient traité par MTX.
Urticaire chronique spontanée.
Le dupilumab est en cours de demande d’AMM.
Le Remibrutinib est en cours d’essai phase 3, c’est un inhibiteur de la kinase de bruton.
Lupus cutané : l’avenir des biothérapies.
LEC pur (LEC + AAN négatif ou< 10 points) : dermocorticoïdes, tacrolimus topique (hors AMM), hydroxychloroquine (HCQ), RTU thalidomide, ou essais cliniques (chronique, aigu ou subaigu).
LEC+LES biologiques (LEC > 10 points dont la seule manifestation clinique est l’atteinte cutanée) : accès biothérapies à venir car 30% évolue vers des LES à 10 ans.
LES > 10 points avec ou sans LEC.
Si échec des TTT habituels il y a des essais anifrolumab/pbo, litifilimab/pbo, lenalidomide/MTX
Atteinte cutanée d’un lupus systémique PNDS 2024. En première ligne : photoprotection, topique (DC, tacrolimus), HCQ. En seconde ligne : thalidomide, MTX faible dose hors AMM, anifrolumab (Saphnelo) +/- belimumab (Benlysta).
Infections émergentes :
Toxicité cutanée des anticancéreux :
Trois outils pour votre pratique
Apremilast.
Fragilité osseuse liée au méthotrexate : étude methofract.
Il s’agit d’une ostéopathie qui donne des douleurs articulaires mécaniques, principalement aux membres inférieurs. Les radios ne suffisent pas, il faut faire une IRM ou une scinti osseuse. Cela atteint surtout des femmes post ménopausiques qui ont eu des TTT prolongés (10 ans en moyenne). Le TTT est l’arrêt du MTX et les fractures se consolident.
Teignes à Trichophyton tonsurans.
Émergence de ce type de teigne chez des jeunes adultes hommes ayant eu une coupe chez un coiffeur ou barbier. Importance des mesures d’hygiène chez le professionnel car des prélèvements ont montré que ce sont les tondeuses électriques et les brosses qui étaient contaminées.
Teignes de l’enfant microsporiques de l’enfant de moins de 20kg.
Arrêt de la fabrication de l’itraconazole buvable ce qui est problématique car la terbinafine à une efficacité sous optimale et que les PMR à l’itraconazole ont une biodisponibilité faible avec un risque d’inefficacité et des sous-dosage. Le centre de preuve a une action en cours auprès de l’ANSM.
Le trichophyton indotineae est responsable de teignes extensives cutanées résistante à la terbinafine touchant essentiellement les HSH et les travailleurs du sexe. Il s’agit d’une mycose à transmission anthropophile.
Folliculite de la barbe à Klebsiella aerogenes touchant des HSH. Ces lésions sont persistantes avec de fréquentes rechutes malgré des TTT par TMP-SMX. Il est important de dépister les partenaires, de décontaminer le matériel de rasage et de décoloniser les fosses nasales. Il existe également des balanoposthites à Klebsiella aérogènes.
Les leishmanioses sont endémiques dans le bassin méditerranéen du fait du réchauffement climatique. Il y a un cas autochtone en Normandie. Elles donnent des aspects trompeurs dactylite, chéilites, perlèches, plaques psoriasiformes.
Ne pas hésiter à contacter le centre référent : cnr-leishmania@chu-montpellier.fr qui envoie des ordonnances type pour la préparation à la paromomycine crème.
Traitement de l’hyperhidrose primitive de l’adulte généralisée en première intention ou localisée en seconde intention par oxybutine à la dose progressive de 2,5 à 10 mg/j. Il faut respecter les contre-indications (prostate, myasthe2nie, transit, glaucome). Les effets indésirables sont connus et dose-dépendants.
La LC-OCT assistée par IA pour la chirurgie des carcinomes basocellulaires permet une meilleure détermination des marges préopératoires pour une prise en charge chirurgicale optimisée.
Allergie de contact à l’urushiol qui est une laque (urushi en japonais) pour recoller des morceaux d’objets et recouvrir des fissures d’or. Cela donne des lésions flexurales. L’urushiol est contenu dans les racines des plantes Rhus non comestibles (poison sumac, poison Ivy, poison oak), l’arbre à laque japonaise, comestible (mangue, noix de cajou, pistache).
Vaginoses.
C’est une dysbiose du microbiome vaginal, Il ne faut traiter que les causes symptomatiques par du métronidazole 2g en prise unique et/ou ovules ou 500 mg 1 fois par jour pendant 7 jours.
Dans les formes récidivantes il faut traiter le partenaire par métronidazole 2g/j 7jours +clindamycine cre1me. Dans ces formes récidivantes, on se demande s’il ne s’agit pas d’IST.
Érythème polymorphe à la cocaïne. Le rôle de la consommation de cocaïne est probable devant la récidive des lésions cutanées à chaque prise de la drogue. Il existe un effet dose connu pour les hypersensibilités de type IV.
Des fiches pratiques d’aide à la prescription des systémiques chez les adultes en âge de procréer, la femme enceinte et allaitante dans les principales maladies dermatologiques grâce à la thèse de Capucine Defrance. Elles sont disponibles sur le site du centre de preuves.
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
Par Dr Christine Léauté Labrèze
Quels sont les HI à risque ?
Il existe un score le IH Referral Score (IHReS) qui permet de savoir quels enfants sont à adresser à un centre expert. Il est en 2 parties. La partie A comprend 6 questions, si l’une d’entre elle est positive il faut adresser le patient. Si elles sont toutes négatives on passe à la partie B. http://www.ihscoring.com
Les bétabloquqnts en pratique.
Le propanolol est le seul TTT qui a l’AMM (3mg/kg/j pendant 6mois). Il permet une régression dans 60% des cas et même 80% si le TTT est commencé avant 3 mois.
On obtient 76% de régression complète avec 3mg/kg/j si le ttt est poursuivi jusqu’à 12 mois avec également moins de récidives à l’arrêt du TTT.
Il y a 10 à 15% de récidives à l’arrêt du TTT sur les HI segmentaires et/ou profonds. Un ttt trop court expose à une récidive.
L’atenolol est proposé comme alternative (hors AMM).
La chirurgie est rarement possible sauf dans les formes localisées. Le laser vasculaire a une efficacité très limitée à la phase précoce (voire délétère) mais est intéressant à la phase tardive sur les télangiectasies résiduelles.
Les bétabloquants sous forme topique ne marchent pas.
Le propanolol normalise le réseau vasculaire ce qui a ouvert une voie thérapeutique dans l’angiogenèse.
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
Par Dr Stéphanie Mallet
C’est comme chez les adultes ou presque.
La DA
Le dupilumab est le seul à voir l’AMM à partir de 6 mois et dans l’asthme. Les autres sont après 12 ans.
Il ne faut pas faire de bilan pré thérapeutique.
Il n’y a pas de contre-indication s’il y a une conjonctivite.
Il faut préférer les seringues au stylos injectables car il permet une injection lente car c’est douloureux. Il faut conseiller de sortir le produit du frigo une heure avant.
La tolérance est bonne.
Les 12-17 ans : DA modérée à sévère (seringue ou stylos)
- < 60 kg : 400 puis 200 mg/2 semaines
- > 60 kg posologie adulte
Les 6-11 ans : DA sévère (seringue)
Les 6 mois- 5 ans : DA sévère (seringue)
Il existe des pousses seringues (aiguille tampon) qui permettent des injections très lente avec un système de pompe.
Le tralokinumab marche plus lentement que le dupilumab mais est moins cher.
Le Lebrikizumab a la même efficacite2 que le dupilumab mais il y a moins d’injections à faire
Le nemoluzimab à L’AMM dans la DA et le prurigo nodulaire avec une efficacite2 rapide ainsi qu’une possibilité d’espacement rapide mais le prix est important.
La durée du ttt est variable. L’évaluation est à faire à 6 à 12 mois. Un espacement est possible après un an de ttt efficace. Un ttt de plusieurs années est la règle.
Pour les vaccins non vivants il n’y a aucun problème.
Pour les vaccins vivants atténués envisagés, il faut arrêter les TTT (immunosuppresseurs, corticothérapie ou biothérapie) 3 mois avant de faire les vaccins (ROR, fièvre jaune, varicelle). Les TTT peuvent être repris 3 semaines après d’après le GREAT.
Des études montrent qu’il faut être rassurants en ce qui concerne les vaccins vivants même s’ils sont faits pendant le ttt.
Il faut prévoir sur l’ordonnance des larmes artificielles, collyres AH1 au cas où il y aurait une conjonctivite (10%), du tacrolimus topique s’il y a une atteinte palpébrale.
Ces ttt augmentent le risque d’infections parasitaires, il faut donc penser à déparasiter et à refaire des tests au retour de voyage.
Attention aux enfants atteints d’asthme, il faudra une gestion pluridisciplinaire (pédiatre, pneumologue).
L’urticaire chronique spontanée.
Omalizumab (xolair) a l’AMM pour les plus de 12 ans, à la dose de 300 mg toutes les 4 semaines (seringue ou stylo). Il est à utiliser en même temps en association avec des anti histaminiques. Il ne faut pas faire de bilan pré thérapeutique et il n’y a pas de contre-indication aux vaccins vivants. L’instauration est à faire par une IDE à domicile pour les 3 premières injections ou à l’hôpital si ATCD d’anaphylaxie.
La durée du TTT est variable, espacement après un an de TTT efficace. Un TTT de plusieurs années est la régle.
Il faut adresser à l’hôpital si le patient a moins de 12 ans, si l’indication est hors AMM, s’il y a un échec au ttt et si l’injection sous cutanée est douloureuse.
Le psoriasis.
Les psoriasis légers (PASI<10, BSA<10 ou DLQI<10) doivent être traités par des ttt topiques (dermocorticoïdes (DC) +analogues vit D3 ou DC + émollients). En cas de plaques hyperkératosiques importantes prescrire des kératolytiques topiques associés : urée (>15%) ou acide salicylique.
Pour les psoriasis modérés à sévères (PASI>10, BSA>10 ou DLQI>10), en première intention mettre les ttt non biologiques (MTX ou ciclosporine ou photothérapie ou acitrétine ou aprémilast (AMM>6ans et 20kg)).
En seconde intention les biothérapies (anti IL17, anti IL 23, anti-TNF alpha et anti IL12/23).
Le switch doit être progressif en initiation de ttt afin d’éviter une poussée.
Avant de débuter une biothérapie, il faut faire :
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
Par Dr Thomas Hubiche
Méningococcémie « subaigue »
Cela donne des purpuras fébriles qu’il faut traiter par de la ceftriaxone IV. Les PCR multiplex de la ponction lombaire sont négatives, on retrouve une PCR à méningocoque de type B dans la peau. Il faut rechercher un déficit immunitaire, vérifier que les vaccins sont à jour notamment le méningo B et le méningocoque ACWY qui est devenu obligatoire pour les nourrissons avec un rattrapage chez les 15-24 ans.
Augmentation des IST chez les 15-25 ans.
Il faut penser à parler de la santé sexuelle pendant nos consultations et proposer le vaccin HPV, car les 15-25 consultent essentiellement les dermatologues.
Les molluscum contagiosum.
Il y a 2 pics d’incidence 3-9 ans et 16-24 ans. Les facteurs de risque sont la DA, personne infectée dans l’entourage (voisin de classe, famille), transmission sexuelle.
Les lésions disparaissent en moyenne entre 6-9 mois, avec un maximum de 3-4 ans.
Aucune étude de bonne qualité n’établit l’efficacité d’un TTT.
La présence d’un placard eczémateux chez les enfants sans D serait associée à une régression des MC dans les 4 à 8 semaines. L’inflammation précède la régression entre 3 semaines te 5 mois.
Chez les adolescents il faut penser à faire un dépistage des IST.
Monkeypox
Chez les enfants c’est le plus souvent une transmission familiale et les enfants ont des lésions diffuses contrairement aux adultes qui ont des lésions de la sphère génitale.
Les infections cutanées folliculaires superficielles.
Le plus souvent sont à staphylocoque aureus,
Dans le cas de furoncle et abcès simple il faut faire des pansements humides, inciser et drainer. Ne pas mettre d’antibiotique.
Si ce sont des formes compliquées (>5cm, dermohypodermites, signes systémiques, âge < 1 an, atteinte du visage, comorbidité ou échec du drainage) il faut traiter par amoxicilline
+ acide clavulanique (80 mg/kg/j en 2 à 3 prises, ne pas dépasser 3g/j pendant 7j) ou cefalexine (50mg/kg/j en 2 à 3 prises, ne pas dépasser 2g/j pendant 7j).
Les alternatives sont le cotrimoxazole si < 6 ans et la clindamycine si > 6 ans. Si on a un SARM il ne faut pas adapter l’antibiothérapie si on a une guérison après le drainage.
L’impétigo.
S’il est localisé <2% de la surface corporelle ou moins de 5 lésions : il faut nettoyer et déterger avec de l’eau et du savon puis mettre 2 à 3 applications par jour pendant 7j. Le nettoyage et la détersion sont toujours utiles et souvent suffisants. Le TTT antibiotique local est à privilégier chaque fois que c’est possible. Il faut également prendre en charge les dermatoses sous-jacentes et faire une exclusion scolaire de 72 heures en cas de lésions non couvertes.
Si les lésions sont extensives, creusantes, >2% ou plus de 5 lésions ou immunodépression : il faut nettoyer et déterger avec de l’eau et du savon puis amoxicilline + acide clavulanique (80 mg/kg/j en 2 à 3 prises, ne pas dépasser 3g/j pendant 7j).
En alternative cefalexine, clarithromycine, clindamycine (>6 ans), cotrimoxazole.
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
Par Pr Romain Blaizot
La leishmaniose.
Il est important d’identifier l’espèce car en fonction on décidera si un TTT est nécessaire.
En Afrique du Sub saharienne il n’y a que du Leishmania (L) major alors qu’au Maghreb plusieurs types de L sont présents.
Le TTT n’est pas systématique. On peut juste faire des soins locaux si on a un L major non sévère du Maghreb ou un L donovani en lésion unique du Moyen Orient. L’enjeu est la cicatrice.
Dans les formes plus graves comme L braziliensis, tropica ou guyanensis, un ttt est nécessaire.
Les différents TTT utilisés sont :
PIAN
C’est une tréponomatose présente en Afrique et en Asie du Sud Est. Il existe un test rapide et on peut la traiter par azithromycine.
Haemophilus Ducreyi donne des ulcères chez l’enfant en Afrique et en Asie du Sud Est. Dans ces cas ce n’est pas une IST. On le traite comme le PIAN
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
Par Pr Olivier Chosidow
Les folliculites à T. mentagrophytes VII doivent être traitées par terbinafine 250mg/j pendant 6 wsemaines ou plus.
Le Lamisil n’est plus commercialisé, il risque y avoir des tensions sur les génériques.
Le T. indotineae nécessite un ttt par itraconazole 200-400 mg/j plus de 6 semaines. Plusieurs cas rapportés ont été sexuellement transmis.
La syphilis.
Une étude montre qu’une dose benzathine penicilline G (BPG) donne les mêmes résultats que 3 doses dans les syphilis précoces.
Un essai clinique randomisé montre que la doxycycline n’est pas inférieure à la BPG dans le ttt des syphilis précoces.
Ce sont des importantes au vu des tensions médicamenteuses actuelles.
Devant tout érythème polymorphe il faut suspecter un mycoplasme pneumoniae en premier lieu et traiter par macrolides (Clarithromycine 500 mg x2/j pendant 5j. ou azithromycine 500 mg J1 puis 250 mg/j J2-J5).
Gale.
Le meilleur essai actuel dans la gale classique montre que la permethrine est meilleure que l’ivermectine .
Il faut privilégier l’ivermectine si l’état cutané est mauvais, si l’application est difficile (climat chaud et humide), s’il y a de nombreuses personnes à traiter, si le patient est non observant.
Gale sévère profuse ou hyperkératosique.
Il faut traiter avec 3 doses d’Ivermectine J0 J7 et J14 associé à un ttt par permethrine à J0 et J7 et à de la vaseline salicylée dans les formes hyperkératosique.
Bénéfices neurologiques et cognitifs du vaccin contre le zona.
Plusieurs études confirme la réduction de 20-25% du risque de démence, incluant l’Alzheimer chez les vaccinés. Les hypothèses physiopathologiques expliquant cet effet sont une moindre réactivation du VZV et donc une réduction neuroinflammatoire ainsi qu’une stimulation immunitaire générale protectrice.
Rédigé par Joséfina MARCO-BONNET (Dermatologue à Montrouge)
Par Pr Marie-Aleth Richard
Les GLP-1RA et le psoriasis.
Ils ont une action sur le métabolisme du glucose avec des effets métaboliques directs et indirects sur divers organes. Ils ont un effet immunologique sur la voie IL17.
Une association biologique et GLP-1RA pourrait être bénéfique sur le blanchiment des lésions pour les patients psoriasiques en situation d’obésité ou en surpoids avec comorbidités (étude TOGETHER -PsO).
Les GLP-1RA pourraient protéger les patients Pso de l’évolution vers un psoriasis articulaire en réduisant le poids et par l’immunomodulation.
Il ne faut pas oublier que ces TTT ont une mauvaise tolérance digestive (diarrhée, vomissements). Ce sont les principales causes d’arrêt. Il faut faire attention à la prise en charge per opératoire des patients sous GLP-1RA car cela provoque un retard de la vidange gastrique et un risque d’inhalation pulmonaire.
Psoriasis et biothérapie (BT).
Les inhibiteurs d’IL23 offrent l’efficacité et la sécurité les plus longues.
L’utilisation antérieure de produits biologiques fait qu’on est moins bon répondeur à tous les produits biologiques mais surtout sur les anti-IL17.
Si on a un rhumatisme psoriasique il faut changer les anti-IL17.
Les antibiotiques pourraient via la dysbiose intestinale diminuer la persistance des biothérapies. Il faut donc être prudent dans la prescription d’antibiotiques chez les patients recevant des biologiques même si la causalité n’est pas encore prouvée.
Il faut penser à faire le vaccin anti-zona chez les patients sous anti-TNF.
Les patients sous anti Il 17 font plus d’infections fongiques, en particulier des candidoses, que ceux traités par d’autres biologiques. L’âge avancé au début du ttt et un diabète sont également des facteurs de risque d’infections fongiques.
La tuberculose est surtout un proble1me avec les anti-TNF. On pourrait donc ne pas dépister par quantiferon si on utilise une autre BT.
Les recommandations déconseillent l’utilisation de produits biologiques dans les 5 ans suivant un cancer en raison du manque de données sur leur innocuité. Une étude de surveillance compare les BT aux TTT conventionnels chez les patients atteints de psoriasis ayant des ATCD de cancer ou un cancer évolutif.
Dans l’ensemble, les BT ont été bien tolérés et ont démontré un profil d’innocuité comparable aux TTT conventionnels. Ils n’ont pas favorisé la progression du cancer et sont restés efficaces.
L’expérience en vraie vie montre que l’interchangeabilité des biosimilaires ne posent aucun souci.
Des rémissions prolongées entre les poussées de psoriasis en goutte avec un ttt précoce, transitoire et sur une courte période par anti Il 23 (risankizumzb) a été décrites. Cela entraine une rémission durable du psoriasis en goutte.
HS
Une revue systématique et une méta-analyse montre que :
L’adalumumab pourrait être moins efficace chez les patients ayant une CRP élevée.
Il semble que l’inhibiteur de Janus kinase 1 par voie orale (povorcitinib) chez les patients HS est efficace et qu’il n’y a aucune preuve d’un risque accru d’effet indésirable à travers les doses évaluées (phase 2, randomisée, en double aveugle, à doses croissantes vs placebo).
L’oxybutine combinée à une BT pourrait être un TTT valide dans l’HS en réduisant les poussées et en atténuant les symptômes.
La crème ruxolitinib a démontré un bénéfice clinique supérieur à celui de son véhicule dans les formes légères de HS et avec un bon profil de sécurité.
Des données rétrospectives suggèrent que l’ajout de sémaglutide aux ttt standard de l’HS s’associe à une diminution des poussées et une amélioration de la qualité de vie. Il a également des effets bénéfiques sur l’inflammation systémique, le poids et les marqueurs métaboliques tels que l’HbA1c.
Le phénol peut être particulièrement utile dans les zones où la chirurgie est plus complexe en raison de l’emplacement anatomique et sur des fistules simples, de petites tailles et drainantes.
CARADERM
C’est un réseau national incluant 3 axes avec chacun un coordinateur national.
LA MISSION DE CARADERM est de créer et alimenter une base numérique sécurisée, normes RGPD.
Il y a un maillage territorial avec des experts cliniciens et pathologistes.
Le premier axe est le carcinome de Merkel dont le Pr Mahtab Samimi est la coordinatrice (Tours).
Le second axe sont les carcinomes annexiels dont s’occupe le Dr Thomas Jouary (Pau).
Le troisième axe sont les carcinomes basocellulaires avancés dont le référent national est le Pr Laurent Mortier (Lille).
Il y a des RCP régionales compétences en cancers rares en dermatologie et des RCP nationales. Sur le site de Caraderm vous pouvez retrouver les experts.
Créez en toute simplicité votre compte professionnel
Je crée mon compteAméliorez vos connaissances professionnelles en profitant de nombreux services exclusifs dans le domaine de la dermatologie : plus de 500 visuels de pathologies, des cas cliniques, des vidéos d’experts…
Bénéficiez d’options uniques telles que l’offre de contenus audio et de supports à proposer à vos patients.
Restez informé(e) des événements et des webinaires à venir, des dernières publications scientifiques et des innovations produit.