1 professionals
Bioderma Congress Reports JADP 2026
Bioderma Congress Reports JADP 2026
Résumé par Mariam Deriouich, interne de dermatologie – CHU Caen
Sujets liés
Pr L. Martin, Dr C. Mallebranche, Dr C. Neyraud
Les maladies auto-inflammatoires (MAI) constituent un groupe hétérogène d’affections inflammatoires liées à une dysrégulation de l’immunité innée, par opposition aux maladies auto-immunes ou allergiques qui relèvent d’anomalies de l’immunité adaptative. Longtemps considérées comme rares, elles représentent aujourd’hui un champ en pleine expansion, tant sur le plan clinique que génétique.
Les MAI peuvent se manifester très précocement, parfois dès les premières semaines de vie, avec des tableaux spectaculaires et atypiques, par exemple :
-Urticaire sévère néonatale associée à fièvre et dysmorphie faciale,
-Encéphalopathie néonatale avec régression psychomotrice, lésions cutanées ischémiques et atteintes articulaires chez l’enfant,
-Formes de l’adolescent associant acné sévère résistante à l’isotrétinoïne, atteintes ostéo-articulaires inflammatoires et manifestations cutanées neutrophiliques.
Un point clé souligné est le caractère évolutif des manifestations, avec un enrichissement progressif du phénotype au cours du temps. Plus l’âge avance, plus le spectre clinique s’élargit.
Les MAI se caractérisent par :
-Des épisodes inflammatoires récurrents ou une inflammation chronique stérile,
-L’absence d’auto-anticorps spécifiques ou de lymphocytes T auto-réactifs pathogènes,
-Une prédisposition génétique, monogénique ou polygénique.
En 2024, plus de 50 pathologies et 60 gènes sont identifiés, un nombre en constante augmentation depuis notamment les avancées majeures en génétique qui ont profondément transformé la compréhension des MAI. Elles s’intègrent désormais dans le champ plus large des maladies de dysrégulation immunitaire.
Les mécanismes impliqués reposent sur :
-Des anomalies des récepteurs de reconnaissance du danger (PAMPs et DAMPs),
-Une activation excessive ou constitutive des voies inflammatoires intracellulaires,
-Un défaut de régulation ou d’inhibition de l’immunité innée.
La classification actuelle des MAI repose principalement sur les voies de signalisation et les profils cytokiniques prédominants, plutôt que sur la seule anomalie génétique. Cette approche fonctionnelle permet d’orienter vers des thérapeutiques ciblées, adaptées au mécanisme physiopathologique sous-jacent.
a. MAI monogéniques
Les MAI monogéniques représentent un sous-groupe particulier, lié à une anomalie génétique unique affectant les voies de l’immunité innée. Leur reconnaissance repose sur un faisceau d’arguments cliniques, biologiques et génétiques.
-Signes évocateurs à l’anamnèse :
oDébut précoce, souvent en période pédiatrique
oConsanguinité ou antécédents familiaux évocateurs
oFièvre récurrente, en l’absence d’infection documentée ou de cancer
oFièvre réfractaire aux antipyrétiques
oAssociation inhabituelle de symptômes ou d’atteintes multi-organiques
oRéponse spectaculaire à un traitement ciblé
-Signes cliniques : l’examen clinique doit être répété et structuré. L’utilisation d’un journal des symptômes, notamment via le score AIDAI (Auto-Inflammatory Disease Activity Index), est particulièrement utile pour objectiver la périodicité, la durée et la sévérité des poussées.
-Explorations complémentaires :
oLe bilan initial comprend : NFS, CRP, bilan hépatique et rénal, recherche d’auto-anticorps (pour éliminer une pathologie auto-immune), dosage des IgG, IgA, IgM et recherche d’acidurie mévalonique selon le contexte (pour éliminer un déficit en mévalonate kinase).
oToujours discuter de la signature interféron, notamment dans les formes évoquant une interféronopathie.
oSelon l’orientation clinique : séquençage ciblé, panel NGS, séquençage d’exome… La génétique est aujourd’hui centrale dans la démarche diagnostique.
-Transmission et hétérogénéité génétique : la transmission est le plus souvent autosomique dominante (AD), mais peut être autosomique récessive ou liée à l’X. Le spectre génétique est large, avec une hétérogénéité importante et des corrélations génotype–phénotype variables.
-Classification :
oINFLAMMASOPATHIES
Les inflammasomopathies sont des MAI liées à une dysrégulation de l’inflammasome, en particulier des voies IL-1β et IL-18.
Le modèle paradigmatique est le CAPS (Cryopyrin-Associated Periodic Syndromes), dû à des mutations gain de fonction du gène NLRP3 (chr 1), codant la cryopyrine, entrainant une activation constitutive de l’inflammasome NLRP3 et in fine une surproduction d’IL-1β et donc une inflammation systémique chronique stérile. Il s’agit d’une perte de contrôle du seuil d’activation de l’immunité innée, avec absence ou inefficacité des mécanismes inhibiteurs. La transmission est autosomique dominante, avec possibilité de mosaïcisme somatique.
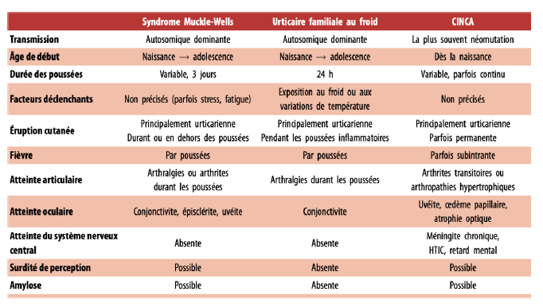
On observe un continuum clinique entre les différentes formes de cryopyrinopathies, qui sont, par odre de sévérité croissante : l’urticaire familiale au froid (FCAS), le syndrome de Muckle-Wells (MWS) et le CINCA / NOMID.
Les critères diagnostiques (d’après Kuemmerle-Deschner, 2017) comprennent : des marqueurs biologiques inflammatoires augmentés, une éruption de type urticarienne, des épisodes déclenchés par le froid/stress, une perte d’audition neurosensorielle, des symptômes musculo-squelettiques (arthralgies, arthrites, myalgies), une méningite chronique aseptique ainsi que des anomalies squelettiques (hypertrophie des épiphyses/bosse frontale).
Il est à noter que cette forme d’urticaire se distingue de l’urticaire au froid classique par : un début précoce dans l’enfance, des poussées chroniques, des symptômes systémiques associés, une absence de réponse aux antihistaminiques, anti-leucotriènes ou omalizumab +/- un syndrome inflammatoire biologique concomitant aux poussées.
Le traitement repose sur le blocage ciblé de l’IL-1 (ex : anakinra)
oRELOPATHIES (non détaillé ici)
oDEFICIT EN MECANISMES REGULATEURS DE L’INFLAMMATION (non détaillé ici)
oINTERFERONOPATHIES
Les IFNopathies de type 1 sont liées à une activation constitutive de la voie de l’IFN de type I et se caractérisent par une signature IFN élevée. Ces maladies possèdent un phénotype systémique variable mais les points d’appel peuvent être : un retard statural ou d’apprentissage, une atteinte neurologique (encéphalopathie, dystonie, épilepsie, surdité…), une vascularite systémique ou encore une fibrose d’organe.
On distingue 3 entités cliniques principales :
▪Le syndrome d’Aicardi-Goutières, avec cliniquement une encéphalopathie inflammatoire précoce, un retard développemental sévère, une spasticité/dystonie, des engelures ou encore une épilepsie. Radiologiquement, on note la présence de calcifications des noyaux gris centraux et d’une leucodystrophie
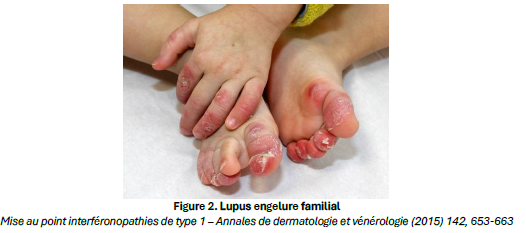
▪Le lupus engelure familial, souvent dû à une mutation de TREX1 ou SAMHD1, débutant dans l’enfance ou l’adolescence et se manifestant par des lésions de type engelures persistantes/récidivantes, des plaques érythémato-violacées des doigts, orteils, oreilles, déclenchées par le froid. Des ulcérations sont possibles. Tous les membres d’une même famille ne développent pas un lupus systémique mais il reste important de suivre annuellement les marqueurs auto-immuns.
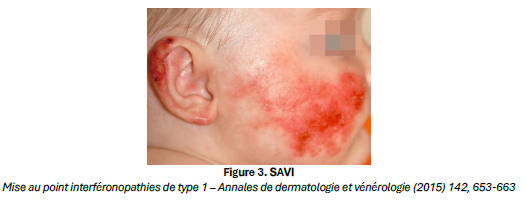
▪Le SAVI, lié à une mutation gain de fonction du gène STING (TMEM173), caractérisé par une vasculopathie cutanée très sévère pouvant aboutir à des lésions ulcérantes et nécrotiques précoces et à une fibrose pulmonaire progressive. Les enfants atteints présentes aussi un retard de croissance et une asthénie.
STRESS INFLAMMATOIRE :
▪Le TRAPS est une maladie de transmission autosomique dominante, liée à des mutations de TNFRSF1A. Le début peut être à tout âge mais est le plus souvent dans l’enfance. Elle se caractérise par des accès inflammatoires prolongés, > 5-7 jours, associés à un syndrome inflammatoire biologique. Les patients présentent une fièvre élevée, des douleurs abdominales, des myalgies migratrices, ainsi que des arthralgies ou des arthrites. L’atteinte cutanée est fréquente, avec des plaques érythémateuses et oedémateuses douloureuses, voir aspect de pseudo-érysipèle. Un oedème péri-orbitaire est retrouvé chez 20% des patients et constitue un signe évocateur. La corticothérapie est efficace pour contrôler les crises mais ne prévient pas le risque d’amylose AA, principale complication à long terme. Le traitement de fond repose donc sur les anti-IL-1.
b.MAI polygéniques
Les MAI polygéniques sont d’expression variable et peuvent s’intégrer dans des phénotypes mixtes. Des mosaïsmes somatiques peuvent être observés et expliquer certaines formes atypiques ou incomplètes. Pour la suite de ce topo, nous proposerons une approche par symptôme :
-Aphtose
oLe PFAPA survient typiquement chez l’enfant entre 0 et 5 ans. Il associe des aphtes buccaux petits et ronds à des épisodes de fièvre élevée récurrente à intervalle régulier. Les poussées durent 3 à 7 jours, avec pharyngite exsudative, adénopathies cervicales, altération de l’état général et inappétence, mais sans retard staturo-pondéral. L’évolution est spontanément favorable avec un espacement progressif des crises. Il faut toujours exclure une origine infectieuse. Les corticoïdes sont efficaces sur les crises, mais peuvent rapprocher leur fréquence, le traitement de fond repose donc sur la colchicine (0,5–1 mg/j) associée à la vitamine D. L’amygdalectomie n’est plus indiquée comme traitement curateur systématique et est réservée aux cas avec syndrome d’apnée du sommeil ou angines bactériennes récidivantes, en général après 6 ans.
oLa maladie de Behçet est rare avant 8 ans. Elle se caractérise par une aphtose bipolaire récidivante, douloureuse et invalidante, avec > 3 poussées/an. Les aphtes génitaux laissent des cicatrices, contrairement aux aphtes buccaux. Elle peut s’accompagner de lésions cutanées (acnéiformes, érythème noueux, folliculite nécrotique), d’arthralgies, de myalgies, d’uvéite non granulomateuse ainsi que d’atteintes neurologiques (céphalées, syndrome pyramidal, ataxie, méningo-encéphalite) ou vasculaires (thromboses veineuses ou artérielles migratrices, anévrismes). Les symptômes digestifs peuvent être inauguraux. Le traitement des poussées cutanéo-muqueuses repose sur une courte cure de corticoïdes. Le traitement de fond repose sur la colchicine ou les anti-TNFα. Une atteinte neurologique ou vasculaire nécessite un traitement immunosuppresseur.
-Rash fébrile prolongé
oLa maladie de Still débute le plus souvent entre 1 et 5 ans. Elle associe une fièvre élevée prolongée (> 15 jours) à un rash saumoné, fugace, non prurigineux, souvent concomitant aux pics fébriles. Elle s’accompagne d’atteintes musculo-squelettiques, de sérites, de pharyngite et d’adénopathies. Le risque majeur est le syndrome d’activation macrophagique (SAM). Le bilan comprend un bilan inflammatoire complet (NFS, CRP, fibrinogène, ferritine, triglycérides, bilan hépatique) et parfois une IRM corps entier. Le traitement repose en première intention sur les AINS (indométacine) ou les corticoïdes, puis sur les biothérapies ciblant l’IL-1 (anakinra) ou l’IL-6 (tocilizumab, disposant de l’AMM). L’évolution peut être monocyclique, polycyclique ou chronique.
Psoriasis, acné, pustulose :
oL’OCMR touche préférentiellement les filles entre 8 et 12 ans. Elle associe douleurs osseuses inflammatoires, lésions cutanées (psoriasis, pustulose, hidradénite suppurée, dermatoses neutrophiliques), aphtes buccaux récurrents et parfois troubles digestifs ou fièvre. Une atteinte vertébrale est possible. Le bilan comprend radiographies ou IRM corps entier, NFS, CRP, bilan hépatique et quantiféron pour exclure une infection, une hémopathie ou une maladie métabolique par exemple. Des lésions radiographiques peuvent être asymptomatiques. Le traitement repose sur les AINS (≥ 4 semaines), les bisphosphonates et parfois les anti-TNF. L’évolution tend vers l’amélioration à la puberté.
Pr A.Torrelo, Dr L.Colas
Les mastocytoses sont un groupe hétérogène d’affections bénignes, plus rarement malignes, liées à une accumulation clonale de mastocytes dans les tissus, principalement la peau chez l’enfant. Les mastocytes dérivent du précurseur myéloïde médullaire (avec probablement une contribution embryonnaire issue du sac vitellin) et s’accumulent préférentiellement dans les tissus conjonctifs. Ils expriment fortement le c-kit, activé par le SCF (stem cell factor). Le gène KIT est un oncogène codant une tyrosine kinase. Les mutations somatiques de KIT sont nécessaires mais non suffisantes au développement d’une mastocytose. Chez l’enfant, la mutation D816V (codon 816) est retrouvée dans environ 40 % des cas, tandis que d’autres mutations de KIT expliquent une proportion comparable.
a.Classification clinique proposée
En pratique pédiatrique, on distingue deux grands phénotypes :
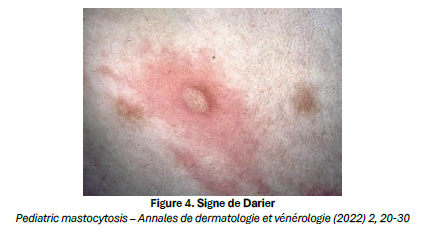
-Type 1 (forme « adulte-like ») : Il s’agit de macules ou papules mélaniques de petite taille (< 5 mm), parfois télangiectasiques, peu nombreuses. Le signe de Darier est discret et les symptômes systémiques sont rares. L’histologie montre des mastocytes fusiformes exprimant CD2/CD25, avec mutation D816V fréquente. Il n’y a pas de réponse à l’imatinib mais une possible réponse au midostaurine. Une régression spontanée est observée dans 50 à 70 % des cas pédiatriques.
-Type 2 (forme typiquement pédiatrique) : Les lésions sont jaunâtres ou brunâtres, non télangiectasiques, avec un signe de Darier très marqué et une urtication fréquente. La dégranulation chronique peut entraîner des anomalies du tissu conjonctif (anétodermie, cicatrices) et des formes bulleuses, surtout chez le nourrisson. L’histologie montre des mastocytes très granuleux, sans expression CD2/CD25, avec mutation de KIT hors codon 816. Ces formes répondent à l’imatinib ou au dasatinib. La régression est fréquente. Les formes familiales sont dans 99 % des cas des formes de type 2.
b.Atteinte systémique et gravité
Chez l’enfant, les manifestations systémiques sont le plus souvent liées à la dégranulation mastocytaire (flush, douleurs abdominales, diarrhée, nausées, douleurs osseuses, fatigue, choc anaphylactique) et non à une infiltration d’organe. L’hépatosplénomégalie ou les adénopathies orientent plutôt vers une infiltration (plus fréquent chez l’adulte). Les formes diffuses et extensives exposent à davantage de signes systémiques. Chez le jeune enfant, les flushs et douleurs abdominales sont particulièrement fréquents. Un syndrome d’activation mastocytaire doit toujours être évoqué devant des manifestations sévères.
En cas d’organomégalie, de tryptase très élevée (> 100 ng/mL) ou de symptômes importants, une biopsie ostéo-médullaire peut être discutée pour éliminer une atteinte systémique.
Il n’existe pas de facteur prédictif fiable d’évolution systémique. L’âge d’apparition (avant ou après 2 ans) et le nombre de lésions (moins il y en a, meilleur est le pronostic) sont les principaux facteurs pronostiques décrits. Les formes agressives pédiatriques restent rares mais graves.
c.Démarche diagnostique
Le diagnostic repose sur l’examen clinique et la mise en évidence du signe de Darier. Le bilan initial comprend NFS, bilan hépatique, bilan inflammatoire et dosage de la tryptase (en tenant compte de l’âge et d’une éventuelle hyperalpha-tryptasémie).
La biopsie cutanée est discutée en cas de doute diagnostique. En présence de signes d’appel, une échographie abdominale ou une recherche de mutation KIT peuvent être réalisées, bien que le dosage systématique du D816V ait peu d’intérêt en pédiatrie.
d.Évolution
La régression complète est rare mais une régression partielle est fréquente, indépendamment de la sévérité des signes systémiques. Les mastocytomes isolés évoluent souvent vers une disparition complète. Les formes diffuses cutanées sont celles où les symptômes systémiques persistent le plus volontiers.
La présence d’une atteinte systémique chez l’enfant ne préjuge pas de l’évolution ultérieure. Un suivi prolongé est recommandé.
e.Prise en charge
Le traitement vise à réduire les symptômes liés à la dégranulation et à améliorer la qualité de vie.
Il repose principalement sur :
-Les antihistaminiques anti-H1 ;
-Le cromoglicate de sodium en cas de symptômes digestifs ;
-L’omalizumab dans les formes avec symptômes sévères de dégranulation ;
-La prescription d’adrénaline auto-injectable (Epipen®) en cas de formes extensives ou d’antécédent d’anaphylaxie
La photothérapie est déconseillée en raison d’un risque accru de mélanome. Les régimes pauvres en histamine n’ont pas démontré d’efficacité et exposent à des carences. En cas d’anesthésie, il est recommandé d’éviter les curares histamino-libérateurs, tandis que les morphiniques peuvent être utilisés avec précaution.
f.Conclusion
Chez l’enfant, la mastocytose est le plus souvent cutanée et de bon pronostic, avec une tendance à la régression. Les manifestations systémiques sont principalement liées à la dégranulation mastocytaire. L’évaluation de la gravité repose davantage sur la clinique que sur la seule valeur de la tryptase. Un suivi au long cours est indispensable.
Dr A.Welfringer, Dr J.Coulombe
Les éruptions graves de l’enfant constituent une situation clinique fréquente dont l’enjeu principal est d’identifier rapidement les formes menaçant le pronostic vital tout en évitant le surdiagnostic de toxidermie. En pédiatrie, de nombreux enfants sont étiquetés à tort comme allergiques à un médicament, ce qui peut avoir des conséquences thérapeutiques durables. L’objectif est donc de savoir reconnaître les situations réellement évocatrices d’éruption médicamenteuse afin d’interrompre précocement le traitement suspect, sans porter ce diagnostic par excès.
La prise en charge débute par un interrogatoire systématique et structuré. Il convient de rechercher la présence d’une fièvre, de signes extra-cutanés, d’une altération de l’état général, d’un contage infectieux, d’un voyage récent, d’une vaccination, ainsi que de préciser la chronologie d’apparition de l’éruption et son site initial. Une attention particulière doit être portée aux prises médicamenteuses dans les huit semaines précédentes, même lorsqu’il s’agit de traitements considérés comme banals.
L’analyse d’imputabilité médicamenteuse repose sur des critères intrinsèques — respect de la chronologie, règle des 5 demi-vies, antécédents allergiques — et extrinsèques, incluant la notoriété du médicament et les données de la littérature. Tout médicament peut être en cause et doit être interrompu en cas de suspicion. Les molécules classiquement à risque de toxidermie incluent les antiépileptiques, les antibiotiques, les AINS, la névirapine, l’abacavir, les produits de contraste iodés et les inhibiteurs de la pompe à protons.
L’évaluation clinique initiale doit systématiquement apprécier la gravité : constantes hémodynamiques, état de conscience, signes respiratoires, adénopathies ou hépatosplénomégalie. La douleur cutanée constitue un signe d’alarme majeur, particulièrement évocateur de nécrolyse épidermique toxique (NET). Il est également indispensable d’éliminer une anaphylaxie, dont l’atteinte cutanée peut être absente dans 10 à 20 % des cas, en recherchant bronchospasme, hypotension, hypoxie, oedème de Quincke ou symptômes digestifs sévères.
Certaines présentations imposent une prise en charge urgente.
Devant un purpura fébrile, le diagnostic de purpura fulminans doit être évoqué en priorité, correspondant le plus souvent à une infection invasive à pneumocoque ou méningocoque. La prise en charge est immédiate, sans attendre les examens complémentaires : remplissage vasculaire, antibiothérapie probabiliste par céfotaxime 50mg/kg, isolement respiratoire et transfert en réanimation. Les hémocultures sont indispensables, la ponction lombaire pouvant être contre-indiquée en cas de CIVD. La biopsie cutanée peut avoir une forte valeur diagnostique notamment en cas d’infection à méningocoque.
En cas de décollement cutané, il est essentiel de distinguer une épidermolyse staphylococcique d’une NET. L’épidermolyse staphylococcique correspond à un clivage superficiel induit par les toxines exfoliantes du S.aureus, sans atteinte muqueuse et avec peu de fièvre ; le diagnostic est clinique et le traitement repose sur l’antalgie et l’antibiothérapie. À l’inverse, la NET survient typiquement dans un délai de 4 à 28 jours après l’introduction d’un médicament, précédée d’un syndrome pseudo-grippal avec fièvre et altération de l’état général, puis d’une éruption douloureuse avec atteinte muqueuse. L’étiologie peut être médicamenteuse, infectieuse ou idiopathique, ce qui impose un bilan exhaustif incluant notamment la recherche d’infections (Mycoplasma, HSV, virus respiratoires, EBV, CMV, HHV-6, parvovirus B19) et de causes auto-immunes.
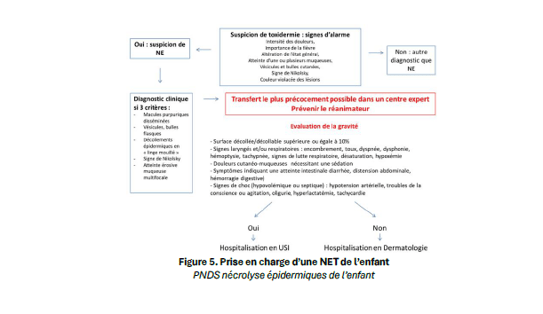
Lorsque l’atteinte muqueuse est prédominante, le diagnostic différentiel inclut la maladie de Kawasaki — en particulier chez l’enfant de 6 mois à 5 ans présentant une fièvre prolongée —, l’érythème polymorphe d’origine infectieuse, la NET, le PIMS ou encore les formes post-infectieuses. L’Alliance de dermatologie pédiatrique a proposé de distinguer les formes post-infectieuses regroupées sous le terme de RIME (Reactive Infectious Mucocutaneous Eruption) des formes médicamenteuses (Drug-induced Epidermal Necrolysis), bien que cette classification ne reflète pas toujours la complexité clinique.
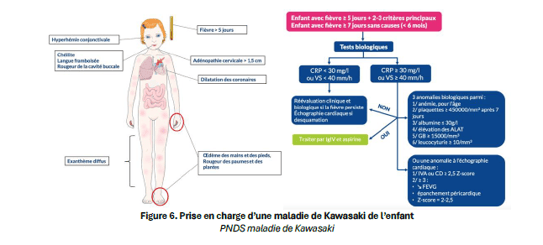
Le DRESS doit être évoqué devant une fièvre constante associée à un exanthème infiltré ou érythrodermique avec oedème facial, adénopathies et possible atteinte systémique. L’hyperéosinophilie peut être retardée et doit être recherchée de façon répétée. Le délai médian d’apparition est d’environ 30 jours après l’introduction du médicament.
La pustulose exanthématique aiguë généralisée (PEAG), quant à elle, survient rapidement après la prise médicamenteuse, avec fièvre élevée et pustules superficielles non folliculaires sans atteinte muqueuse.
L’étude multicentrique nord-américaine PROMISE a apporté un éclairage majeur en montrant qu’une proportion importante des enfants initialement diagnostiqués SJS/TEN relevaient en réalité de RIME, le plus souvent d’origine infectieuse, notamment à Mycoplasma pneumoniae. Les RIME se caractérisent par une atteinte muqueuse prédominante, une atteinte cutanée limitée et une évolution généralement plus favorable, contrairement aux SJS/TEN médicamenteux associés à un décollement étendu et à une morbidité plus importante. Cette reclassification souligne que toutes les éruptions sévères avec atteinte muqueuse ne sont pas médicamenteuses et qu’une distinction rigoureuse influence directement la prise en charge et le pronostic.
Enfin, il est essentiel d’éviter l’étiquetage abusif d’allergie médicamenteuse. L’exemple classique est l’éruption sous amoxicilline au cours d’une mononucléose infectieuse, situation dans laquelle une exploration allergologique avec éventuelle réintroduction encadrée doit être discutée, car une proportion significative d’enfants n’est pas réellement allergique.
En conclusion, une éruption grave chez l’enfant ne rime pas systématiquement avec médicament. La démarche doit être structurée, rigoureuse et prudente, visant à identifier rapidement les urgences vitales et les toxidermies sévères, tout en évitant les diagnostics excessifs d’allergie. La standardisation des critères diagnostiques et la meilleure distinction entre formes médicamenteuses et post-infectieuses constituent un enjeu majeur pour améliorer la qualité des soins en dermatologie pédiatrique.
Dr C. Chiaverini
La paupière constitue un organe cutané complexe associant une peau particulièrement fine, des glandes sudorales et sébacées ainsi que des annexes pilaires. Cette richesse anatomique explique la grande variété des tableaux cliniques observés et la fréquence des diagnostics différentiels, certains relevant d’atteintes systémiques ou de situations d’urgence.
Devant un oedème inflammatoire bilatéral isolé des paupières, sans fièvre ni prise de godet, la cinétique d’installation oriente fortement le diagnostic. Une installation progressive, asymptomatique, s’aggravant sur plusieurs jours, doit faire évoquer une dermatomyosite. Il convient alors de rechercher systématiquement une faiblesse musculaire proximale, une photosensibilité et des lésions des mains. Il s’agit d’un signe de gravité nécessitant un bilan systémique rapide. À l’inverse, une installation aiguë en moins d’une heure évoque un angio-oedème, parfois douloureux ou prurigineux, pouvant s’associer à une urticaire. La recherche de signes d’anaphylaxie (dyspnée, dysphonie, hypotension) est impérative. Enfin, un prurit intense évoluant depuis 48 heures oriente vers un eczéma de contact ; l’interrogatoire doit rechercher une sensibilisation directe (cosmétiques, collyres), de proximité (produits capillaires, topiques du visage), manuportée ou aéroportée.
La présence d’un hématome en « raton laveur » impose une analyse étiologique rigoureuse. En contexte néonatal traumatique, il peut s’agir d’une diffusion d’un hématome sous-galéal, notamment après extraction par ventouse, avec un risque d’anémie aiguë ou de coagulation intravasculaire disséminée. Chez l’enfant de moins de quatre ans présentant une altération de l’état général, un neuroblastome métastatique doit être évoqué, la tumeur étant le plus souvent surrénalienne avec possibles localisations orbitaires. Enfin, une fracture antérieure de la base du crâne doit être éliminée, en particulier dans un contexte suspect de maltraitance, en raison du risque de brèche méningée constituant une urgence neurochirurgicale.
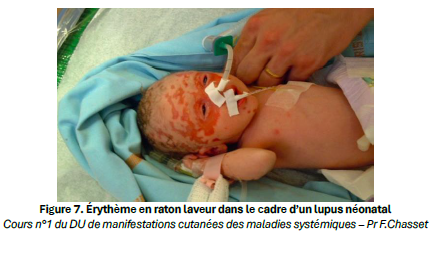
Une éruption érythémateuse en « raton laveur » peu ou pas symptomatique, isolée et respectant les lèvres, oriente vers une dermite péri-orificielle, rare avant l’âge de 2 ans et souvent favorisée par l’usage de corticoïdes topiques ou inhalés. Chez le nouveau-né, une éruption similaire apparaissant après quelques jours ou semaines de vie doit faire rechercher un lupus néonatal, secondaire au passage transplacentaire d’anticorps maternels anti-Ro/SSA ou SSB, en raison du risque majeur de bloc auriculo-ventriculaire.
Devant une paupière achromique acquise, la morphée se manifeste initialement par un érythème évoluant vers une plaque blanc nacré puis une scléro-atrophie progressive, généralement asymptomatique. Le vitiligo segmentaire, forme la plus fréquente de vitiligo chez l’enfant, se caractérise par une achromie sur peau cliniquement normale, visible en lumière de Wood, avec atteinte fréquente des poils et parfois un discret érythème périphérique.
Les paupières érythémato-squameuses relèvent principalement du psoriasis ou de la dermatite atopique. Le psoriasis facial de l’enfant est fréquent, souvent peu prurigineux, et peut s’associer à des atteintes du cuir chevelu, des plis, des ongles ou de la langue. La dermatite atopique se manifeste par des lésions érythémateuses sèches, parfois lichénifiées ou pigmentées, volontiers péri-orbitaires et prurigineuses, associées au signe de Dennie-Morgan et à un terrain atopique personnel ou familial. Un eczéma de contact associé doit toujours être envisagé.
Une paupière dépilée impose un examen dermoscopique attentif. La trichotillomanie se traduit par une atteinte uni- ou bilatérale avec cils cassés de longueurs variables, points noirs et cils normaux persistants, sans signe inflammatoire associé. La pelade peut être partielle ou complète, asymptomatique, uni- ou bilatérale, et nécessite la recherche d’autres localisations ; la dermoscopie peut montrer des points jaunes, des points noirs ou des cheveux en point d’exclamation.
Devant un « bouton » palpébral, le chalazion correspond à l’obstruction d’une glande sébacée palpébrale et se manifeste par un nodule inflammatoire parfois suppuré, souvent indolore en l’absence d’infection et susceptible de récidiver. L’orgelet correspond à une folliculite aiguë du cil, douloureuse, se présentant comme un petit nodule purulent centré par un poil. Le Molluscum contagiosum, lié à un Poxvirus, peut siéger sur la paupière, s’inflammer ou s’eczématiser ; les options thérapeutiques restent limitées en dehors d’une attitude expectative et de soins émollients.
Enfin, des plaques érythémateuses palpébrales associées à une photosensibilité doivent faire évoquer une connectivite. L’atteinte palpébrale de la dermatomyosite peut être étendue tout en respectant classiquement la pointe du nez ; elle n’est habituellement pas cicatricielle mais peut comporter des lésions nécrotiques. Le lupus discoïde touche préférentiellement les zones photo-exposées céphaliques et évolue vers une atrophie et une hypochromie cicatricielle.
Ainsi, l’analyse sémiologique fine, la cinétique d’apparition, l’interrogatoire ciblé et l’apport de la dermoscopie constituent les éléments clés d’une démarche diagnostique rigoureuse face aux dermatoses des paupières.
Pr A. Maruani
L’acceptation des marques cutanées chez l’enfant et l’adolescent constitue un enjeu central en dermatologie pédiatrique, dépassant largement la seule dimension esthétique. Elle engage la construction identitaire, l’estime de soi et l’intégration sociale. Dans ce contexte, les échelles MARKS ont été développées comme outils d’évaluation standardisés, utilisables à la fois en pratique clinique et en recherche, auprès des enfants, des adolescents, des adultes porteurs de marques, ainsi que de leurs parents.
Chez les patients, l’outil MARKS explore six dimensions complémentaires :
-Confiance en soi en lien avec la marque (peur de ne pas être aimé plus tard).
-Acceptation de la visibilité corporelle (besoin de cacher la marque).
-Impact positif de la différence (valorisation identitaire).
-Dépassement des limitations socio-professionnelles ou scolaires.
-Perception du ressenti parental (regard et attentes perçus).
-Insouciance face à la marque (capacité à en parler ou à en plaisanter).
Chez les parents, cinq dimensions sont évaluées :
-Acceptation de la visibilité corporelle de l’enfant
-Partage décisionnel
-Valorisation de la différence
-Perception de l’acceptation sociale de l’enfant
-Ressenti parental.
Cette structuration permet de dépasser une vision binaire (acceptation vs rejet) et d’identifier des leviers d’intervention personnalisés.
Le discours médical constitue un facteur modifiable majeur. Il doit apporter une clarification diagnostique et pronostique, proposer des options thérapeutiques réalistes et aborder précocement la question de l’acceptation. Il doit permettre de responsabiliser sans culpabiliser (« on est une équipe ») et de dédramatiser notamment la crainte anticipée du harcèlement scolaire.
L’acceptation est un processus évolutif, nécessitant du temps et un accompagnement adapté.
Plusieurs variables modulent le processus :
-L’âge (enfant, adolescent, adulte).
-Le moment du diagnostic (congénital versus acquis).
-Le soutien familial et social.
-Le parcours de soins antérieur (errance, échecs).
-Les ressources psychiques et la personnalité.
Le dermatologue, intégré au réseau de soutien, représente un acteur clé dans cette dynamique.
Pour conclure, les échelles MARKS offrent un cadre structuré pour évaluer l’acceptation des marques cutanées dans toutes ses dimensions. Elles permettent d’orienter la prise en charge vers une approche globale, centrée sur l’enfant et sa famille, où le soin dermatologique s’articule à un accompagnement psychologique et relationnel. L’acceptation ne se décrète pas : elle se construit, dans le temps, grâce à un environnement soutenant et un discours médical ajusté.
Dr S. Mallet
Les recommandations récentes du Conseil National Professionnel (CNP) de Dermatologie ont permis de clarifier et d’actualiser la prise en charge de la gale chez l’enfant, en tenant compte de l’âge, du poids, des situations d’échec thérapeutique et du contexte familial.
a.Gale
Chez le nourrisson de moins de deux mois, le traitement de première intention repose sur l’application de perméthrine topique à 5 %, bien que son utilisation soit hors AMM dans cette tranche d’âge. Le traitement doit être appliqué une 1ère fois à J1, puis impérativement répété entre J8 et J14 afin d’éliminer les parasites issus des oeufs ayant éclos après la première application. En cas d’échec, il est essentiel de ne pas conclure trop rapidement à une résistance. Il convient d’analyser rigoureusement les causes possibles : mauvaise observance, recontamination par un contact non traité, décontamination insuffisante du linge ou de la literie. Une fois ces éléments vérifiés et corrigés, le même schéma thérapeutique par perméthrine est recommandé. Selon le contexte clinique ou social, une hospitalisation peut être discutée. Pour des raisons de meilleure tolérance cutanée, la perméthrine est préférée au benzoate de benzyle, même si ce dernier dispose d’une AMM à partir de l’âge d’1 mois. La pommade au soufre, historiquement utilisée et réputée efficace quel que soit l’âge, n’est toutefois pas disponible en France. A noter que chez le nourrisson, les présentations cliniques peuvent être atypiques, avec des nodules scabieux du tronc ou des aisselles et une atteinte plus fréquente du visage et du dos des pieds.
Chez l’enfant de 2 à 24 mois, deux options thérapeutiques sont proposées en première intention. La perméthrine 5 % reste privilégiée, notamment chez l’enfant de moins d’1 an, en cas d’atteinte du visage (régions périorbitaires ou périorales) ou lorsque la peau est lésée. Le schéma d’application reste identique. Le benzoate de benzyle 10% constitue une alternative. Il doit être appliqué à J1 puis à J8–J14, avec un temps de contact adapté à l’âge : 6 h chez l’enfant < 12 mois et 12 h entre 12 et 24 mois. En cas de récidive, après analyse des conditions d’échec, il est possible de reconduire la même molécule ou d’opter pour l’alternative. L’ivermectine orale à la dose de 200 μg/kg, en 2 prises (J1 et J8–J14), peut être envisagée hors AMM lorsque l’observance est incertaine, lorsque l’état cutané rend les traitements locaux difficiles ou en cas de cas groupés. Un avis infectiologique est recommandé chez les enfants ayant séjourné en zone tropicale, en raison du risque de loase.
Chez les enfants de plus de 24 mois et de moins de 15 kg, la perméthrine 5 %, le benzoate de benzyle 10 % et l’ivermectine orale constituent des options de première intention. L’ivermectine doit être administrée à la dose de 200 μg/kg par prise, avec 2 prises espacées de 7 à 14 jours. Il est recommandé de l’administrer au cours d’un repas afin d’optimiser son absorption. En l’absence de forme sirop en France, l’adaptation galénique peut nécessiter de couper le comprimé de 3 mg (1 comprimé correspondant à 15 kg) en demi ou quart de comprimé selon le poids, puis de l’écraser et de le diluer si besoin. En cas de récidive, l’une des trois molécules peut être utilisée, mais l’ivermectine orale est à privilégier si l’observance des traitements locaux est douteuse ou en présence de cas groupés.
Chez l’enfant, l’application des topiques doit être réalisée sur l’ensemble du corps, y compris le cuir chevelu et le visage, en évitant strictement les muqueuses. Les paumes, les plantes et les zones sous-unguéales doivent faire l’objet d’une attention particulière, car elles sont fréquemment atteintes. Il est recommandé d’appliquer le traitement lorsque l’enfant est endormi, notamment sur les mains, qui pourront ensuite être protégées par des gants ou des chaussettes pour éviter le léchage ou l’ingestion accidentelle du produit.
Le traitement des cas contacts intrafamiliaux doit être systématique et simultané, même en l’absence de symptômes, afin de prévenir les rechutes. La décontamination du linge et de la literie doit être réalisée le jour même de l’application du traitement topique ou le lendemain de la prise d’ivermectine. Le linge peut être lavé à 60°C lorsque cela est possible ou à défaut, être placé en quarantaine dans un sac hermétique pendant trois jours (gale commune) ou huit jours (gale profuse). Les textiles fragiles peuvent être placés 48 heures au congélateur. L’aspiration soigneuse des tapis et coussins est recommandée, ainsi que le traitement du matelas, du mobilier, de la poussette et des sièges auto. Il convient toutefois d’éviter toute anxiété excessive ou destruction inutile du mobilier.
Selon le Centre de Référence sur les Agents Tératogènes (CRAT), l’ivermectine peut être utilisée chez la femme enceinte, recommandée en 1ère intention aux deuxième et troisième trimestres, et en 2nd intention quel que soit le terme. Elle est également compatible avec l’allaitement.
b.Pédiculoses
La prise en charge des poux repose désormais en uniquement sur les lotions à base de diméticone, appliquées sur cheveux secs à J1 puis à J7. Ce traitement est non remboursé mais compatible avec la grossesse. Le malathion et les pyréthrines ont été retirés du marché. Le peignage minutieux et répété constitue un élément essentiel du traitement. Il n’est pas nécessaire d’exclure l’enfant de l’école. Le linge doit être lavé à 60°C ou placé en quarantaine 3 jours. Tous les membres du foyer doivent être examinés et traités en cas d’infestation.
En alternative, notamment en cas d’échec, l’ivermectine orale à double dose (400 μg/kg) a montré une efficacité supérieure au malathion dans une étude randomisée en cluster, mais son utilisation doit tenir compte du risque potentiel de résistance. L’ivermectine topique dispose d’une AMM aux États-Unis, avec là aussi une vigilance concernant l’émergence de résistances.
c.Morpions
Les morpions peuvent atteindre le cuir chevelu dans environ 50 % des cas. Le traitement repose sur une approche occlusive (par exemple vaseline) ou sur l’ivermectine. Ils ne doivent pas faire conclure par excès aux sévices sexuels et ne doivent plus être considérés comme une IST.
Pr J. Martin, Dr H. Aubert, Dr C. Thomas
Le système immunitaire assure un équilibre complexe entre défense contre les agents infectieux, tolérance vis-à-vis de la flore commensale et prévention des réponses auto-immunes. L’induction d’une réponse adaptative repose sur l’activation des cellules dendritiques par un agent infectieux, la présentation antigénique aux lymphocytes T, puis l’activation coordonnée des lymphocytes T et B. Les lymphocytes T CD4 jouent un rôle central en orchestrant l’activation des lymphocytes B, des phagocytes, des lymphocytes T CD8 et des cellules immunitaires innées dans les tissus infectés.
Les déficits immunitaires primitifs (DIP), ou erreurs innées de l’immunité, concernent environ 1 naissance sur 3 000. La transmission est autosomique récessive dans 65 % des cas, autosomique dominante dans 28 % et liée à l’X dans 7 %. Si la majorité des DIP sont diagnostiqués dans l’enfance, près d’un quart le sont après l’âge de 15 ans, soulignant l’importance d’une vigilance prolongée.
a.Signes d’alerte
Les infections répétées constituent le mode de révélation principal (60 %), notamment sinusites (>2/an après 6 ans), otites moyennes aiguës (>6–8/an avant 4 ans, >2–4/an après 4 ans), pneumopathies (>1/an), infections bactériennes invasives, infections virales chroniques ou mycoses cutanéo-muqueuses chroniques. Cependant, les manifestations dermatologiques peuvent être inaugurales : eczéma sévère ou atypique (atteinte du siège, des paumes/plantes), infections virales cutanées extensives, candidose chronique, lésions pétéchiales associées au prurit, ou encore manifestations auto-immunes.
Les Primary Atopic Disorders (PAD), impliquant actuellement 55 gènes identifiés, illustrent cette interface dermato-immunologique. L’élévation des IgE est inconstante. Les manifestations atopiques peuvent être atypiques, précéder les infections, s’accompagner d’un retard de croissance, d’anomalies du tissu conjonctif ou d’un risque accru de cancer. Les signes sont parfois isolés et leur association variable, expliquant un retard diagnostique fréquent.
b.Le dépistage néonatal des DICS
Depuis le 1er septembre 2025, le dépistage néonatal inclut les déficits immunitaires combinés sévères (DICS) par dosage des TRECs sur carte de Guthrie. Cette stratégie permet d’identifier précocement les nourrissons présentant un déficit profond en lymphocytes T, exposés à des infections graves dès les premiers mois de vie.
En cas de test positif, une prise en charge urgente par un pédiatre immunologiste est organisée :
-Confirmation biologique avec immunophénotypage lymphocytaire (quantification des LT naïfs/RTE),
-Isolement protecteur,
-Prophylaxie anti-infectieuse à large spectre, immunoglobulines intraveineuses, support nutritionnel,
-Analyse génétique par panel NGS dédié aux erreurs innées de l’immunité (plus de 500 gènes), voire séquençage du génome en trio si nécessaire.
Le dépistage néonatal transforme le pronostic : la greffe de cellules souches hématopoïétiques réalisée précocement (autour de 3 mois) améliore significativement la survie. Il modifie également les pratiques, avec une prise en charge d’enfants asymptomatiques au moment du diagnostic.
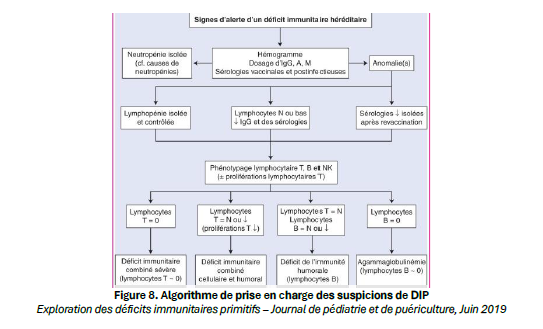
c.Le syndrome de Wiskott-Aldrich :
oTransmission récessive liée à l’X, et incidence estimée entre 1 et 9/million de garçons. Il associe thrombopénie à petites plaquettes, eczéma et déficit immunitaire. Les pétéchies sur zones de grattage constituent un signe d’orientation majeur. La prise en charge comprend immunoglobulines, corticothérapie, analogues de la thrombopoïétine, antibioprophylaxie ; l’allogreffe est le traitement de choix des formes sévères.
-Déficit en DOCK8 :
oCaractérisé par un eczéma constant avant l’âge de 1 an, souvent associé à des comorbidités atopiques et à une hyper-IgE avec éosinophilie. Les anomalies touchent la régulation du cytosquelette dépendante de l’actine, la migration des cellules dendritiques et les réponses interféron de type I. Il en résulte des infections virales cutanées sévères (herpès, HPV, molluscum contagiosum, EBV), bactériennes et fongiques, ainsi qu’un risque auto-immun et tumoral. L’absence de lymphocytes T résidents mémoire cutanés contribue à la sévérité des atteintes dermatologiques.
-Le syndrome d’Omenn :
oVariant de DICS lié le plus souvent à des mutations hypomorphes de RAG1/2. Il associe érythrodermie, desquamation, alopécie, diarrhée chronique, retard staturo-pondéral, adénopathies et hépatosplénomégalie, avec présence de lymphocytes T autologues auto-réactifs. Le diagnostic différentiel avec une réaction du greffon contre l’hôte est essentiel.
-Candidose cutanéo-muqueuse chronique :
oElle doit faire évoquer un défaut des voies IL-17/IL-22 et des réponses immunitaires de type 3, parfois en lien avec des anomalies de STAT3 ou d’autres voies moléculaires spécifiques.
d.Conclusion
Le champ des erreurs innées de l’immunité connaît une expansion rapide grâce aux progrès du séquençage génétique et à l’intégration du dépistage néonatal des DICS. La compréhension fine des mécanismes immunologiques ouvre la voie à des thérapeutiques ciblées.
Pour le dermatologue, les messages clés sont clairs : penser au DIP devant tout eczéma sévère, atypique ou associé à des infections répétées ; rechercher des signes systémiques (retard de croissance, infections inhabituelles, auto-immunité) ; adresser précocement en immunologie pédiatrique.
Pr L. Martin, Dr T. Hubiche, Dr F. Morice Picard, Dr M. Nizon
a.Diagnostic prénatal et pré-implantatoire des maladies monogéniques : enjeux actuels
Le développement du diagnostic prénatal non invasif (DPNI) appliqué aux maladies monogéniques soulève des enjeux économiques et sociétaux majeurs. Son coût est souvent supérieur aux techniques invasives conventionnelles, et son accessibilité croissante impose une vigilance éthique : il ne s’agit pas « d’une simple prise de sang ».
Le conseil génétique pré-test est indispensable afin d’évaluer les implications pour la grossesse en cours, mais aussi pour la patiente et son conjoint. L’élargissement potentiel des indications expose à un risque de dérives, justifiant un encadrement institutionnel strict et une validation systématique des indications par le Centre pluridisciplinaire de diagnostic prénatal (CPDPN).
Le diagnostic prénatal invasif (DPN) repose sur la biopsie de trophoblaste entre 12 et 14 SA, après identification préalable de la variation familiale. L’analyse génétique (chromatogramme) permet un diagnostic ciblé mais expose à un risque de fausse couche spontanée. En cas d’atteinte sévère confirmée, une interruption médicale de grossesse peut être demandée par la patiente, après validation par le CPDPN et consentement écrit.
Actuellement réalisé dans 5 centres en France, le diagnostic pré-implantatoire (DPI) permet le transfert d’embryons indemnes, évitant une IMG. Après fécondation in vitro avec ICSI, une biopsie embryonnaire est réalisée au 3ᵉ jour de développement sur cellules totipotentes, suivie de la sélection des embryons non porteurs. Le taux de grossesse évolutive est d’environ 30 % par FIV. Le DPI n’est pas proposé en cas de risque de mosaïque germinale. Les indications les plus fréquentes incluent la maladie de Huntington, la mucoviscidose, la dystrophie myotonique de Steinert, la drépanocytose, le syndrome de l’X fragile ou la neurofibromatose de type 1. L’âge maternel constitue un facteur majeur d’échec, certains centres limitant l’accès après 36 ans.
Le DPNI des maladies monogéniques repose sur le séquençage de l’ADN foetal circulant dans le sang maternel. Initialement développé pour le dépistage des aneuploïdies (trisomie 21, 13…), il s’étend désormais aux maladies monogéniques. Contrairement au dépistage des aneuploïdies, un résultat positif pour une maladie monogénique ne nécessite pas systématiquement de confirmation invasive. Les variations paternelles, de novo ou récessives peuvent être identifiées même si absentes chez la mère. L’étape suivante vise à détecter les variations maternelles transmises (étude DANNI). Toutefois, les implications économiques et sociétales restent majeures, et toute demande doit être validée par le CPDPN.
Le séquençage d’exome en période anténatale élargit encore le champ diagnostique, posant la question du cadre d’interprétation, du rendu des résultats et du risque de découvertes incidentales.
b.Albinisme : actualités cliniques et prise en charge
L’albinisme regroupe un ensemble d’affections génétiques caractérisées par un défaut de production ou de transport de la mélanine, responsable d’une hypopigmentation cutanée et oculaire associée à une atteinte visuelle constante. La majorité des formes sont autosomiques récessives (OCA1 à OCA8), avec une importante hétérogénéité génétique. Certaines formes sont syndromiques (avec risque d’atteintes plaquettaires, digestives, pulmonaires ou immunitaires), plus rarement liées à l’X.
Les patients présentent classiquement cheveux blond platine, peau très claire et photosensibilité marquée. Dans l’OCA2, la production résiduelle de phéomélanine peut donner une coloration orangée des cheveux. Il n’existe pas de corrélation entre la pigmentation cutanéo-pilaire et la sévérité de l’atteinte ophtalmologique. Les nævus sont présents quel que soit le type d’albinisme, parfois achromiques dans l’OCA1. Les éphélides sont fréquentes, volontiers étoilées et profuses dans l’OCA2.
Par ailleurs, les dommages actiniques sont précoces et cumulatifs. Environ 10 % des patients développent des carcinomes épidermoïdes, indépendamment du type mutationnel. Les mélanomes sont rares mais majoritairement amélanotiques, imposant une vigilance clinique accrue.
L’atteinte visuelle est constante et nécessaire au diagnostic. Elle associe :
-
Déficit d’acuité visuelle (corrélé au degré d’hypoplasie fovéale)
-
Nystagmus
-
Hypopigmentation rétinienne
-
Transillumination irienne
-
Anomalies du routage des nerfs optiques
L’hypoplasie fovéale et l’hypopigmentation relèveraient de mécanismes physiopathologiques distincts.
La prise en charge est multidisciplinaire et précoce, ophtalmologique (correction des amétropies, verres teintés avec protection UV, aides visuelles et aménagements scolaires, chirurgie du nystagmus ou du strabisme si nécessaire…) annuellement jusqu’à 6–8 ans, et dermatologique (surveillance clinique, photoprotection stricte dès l’enfance, supplémentation en vitamine D, éducation thérapeutique…).
c.Actualités dans les traitements des génodermatoses
Les progrès récents en génétique moléculaire ont profondément modifié la prise en charge des génodermatoses. Alors que le traitement était historiquement symptomatique, l’identification précise des anomalies géniques permet désormais d’envisager des approches ciblées, voire causales. Plusieurs stratégies thérapeutiques sont aujourd’hui discutées : la thérapie génique visant à corriger ou remplacer un gène altéré, la modulation de l’expression génique (correction d’épissage, inhibition d’ARNm), les thérapies cellulaires utilisant des cellules corrigées, les traitements substitutifs enzymatiques ou non, les petites molécules ciblant une voie de signalisation spécifique, et, lorsque ces options ne sont pas accessibles, des approches symptomatiques ou palliatives.
Dans la kératodermie palmo-plantaire d’Olmsted, l’identification d’une activation anormale de la voie EGFR a permis l’utilisation rationnelle d’inhibiteurs de cette voie, tels que l’erlotinib. Cette approche ciblée a montré une amélioration des douleurs et de l’hyperkératose, illustrant l’intérêt du repositionnement de traitements initialement développés en oncologie vers des maladies génétiques cutanées rares.
Le pseudoxanthome élastique constitue un autre modèle physiopathologique éclairant. Les variants pathogènes du gène ABCC6, majoritairement exprimé dans le foie, entraînent une diminution de l’ATP extracellulaire puis du pyrophosphate circulant, inhibiteur physiologique de la calcification. Il en résulte des calcifications ectopiques cutanées, rétiniennes et vasculaires. Plusieurs stratégies sont en cours d’évaluation pour restaurer l’équilibre minéral ou inhiber la calcification des tissus mous, notamment le magnésium, la vitamine K, le thiosulfate de sodium, l’étidronate, des inhibiteurs de TNAP ou encore des approches de remplacement enzymatique comme eNPP1.
Dans l’angioedème héréditaire, le déficit constitutionnel en C1-inhibiteur lié à des variants de SERPING1 conduit à une production excessive de bradykinine responsable des épisodes d’oedème. Au-delà des traitements déjà disponibles (concentrés de C1-inhibiteur, inhibiteurs de la kallikréine, antagonistes des récepteurs B2), une thérapie génique reposant sur l’édition du gène KLKB1 afin de réduire la pré-kallikréine plasmatique a récemment été rapportée dans le New England Journal of Medicine (2025), ouvrant la voie à des stratégies d’édition génique systémique.
Les ichtyoses congénitales bénéficient également d’avancées thérapeutiques. Une étude rétrospective internationale portant sur 98 patients atteints majoritairement de syndrome de Netherton ou d’ichtyose érythrodermique congénitale a évalué différentes biothérapies ciblant l’inflammation. Les inhibiteurs de l’IL-17, de l’IL-12/23 et du récepteur de l’IL-4 ont été utilisés, avec une réponse globale observée chez près de la moitié des patients. Les meilleurs résultats ont été obtenus dans les formes à forte composante inflammatoire, tandis que les ichtyoses lamellaires et épidermolytiques répondaient peu, soulignant l’importance du phénotype inflammatoire dans le choix thérapeutique.
Dans l’épidermolyse bulleuse dystrophique, l’activation de l’inflammation de type Th2 a conduit à l’utilisation du dupilumab dans des séries de cas encourageantes. Surtout, la première thérapie génique topique, le beremagene geperpavec (B-VEC, Vyjuvek®), est désormais disponible. Les données françaises à 17 mois d’accès précoce montrent des taux variables de cicatrisation complète des plaies cibles selon les temps d’évaluation, avec une satisfaction rapportée par la moitié des patients et familles. Il s’agit d’une étape majeure, marquant l’entrée concrète de la thérapie génique en dermatologie clinique.
Enfin, dans la sclérose tubéreuse de Bourneville, l’activation constitutive de la voie mTOR justifie l’utilisation du sirolimus, conformément aux recommandations nationales. L’implication de cette même voie dans certaines formes d’épidermolyse bulleuse simple illustre la possibilité de cibler des mécanismes de signalisation communs à plusieurs génodermatoses.
Au-delà de ces exemples, un message clé se dégage : la décision thérapeutique repose impérativement sur un diagnostic génétique précis et une compréhension fine de la physiopathologie. Le choix du traitement doit intégrer le rationnel mécanistique, le profil de tolérance, les contraintes pratiques et le cadre réglementaire, souvent discutés en réunion de concertation pluridisciplinaire au sein des filières spécialisées. La mise en place d’essais cliniques adaptés aux maladies rares et compatibles avec les exigences des agences réglementaires européennes et américaines constitue un enjeu majeur. Ainsi, la prise en charge des génodermatoses entre progressivement dans l’ère de la médecine de précision, où l’identification de la voie pathologique activée conditionne une stratégie thérapeutique de plus en plus personnalisée.
Dr C.Abasq
La découverte d’un nodule cutané chez l’enfant constitue un motif fréquent de consultation. Si l’hémangiome infantile est souvent évoqué en première intention, tout nodule n’est pas une tumeur bénigne, et tout nodule n’est surtout pas un hémangiome. En particulier, toute lésion apparaissant après l’âge de 18 mois ne doit pas être considérée comme un hémangiome jusqu’à preuve du contraire. L’âge de l’enfant, la topographie, la couleur, la consistance, la mobilité par rapport aux plans profonds et l’évolutivité sont des critères déterminants pour orienter le diagnostic.
Les tumeurs malignes cutanées de l’enfant sont rares et souvent confondues avec des lésions vasculaires bénignes. Parmi les diagnostics à évoquer figurent les leucémides, les localisations cutanées de lymphome lymphoblastique, la papulose lymphomatoïde, certaines histiocytoses, les carcinomes, les métastases cutanées de neuroblastome, les tumeurs rhabdoïdes, le dermatofibrosarcome ou encore le fibrosarcome infantile. Une consistance ferme, une fixation aux plans profonds, une coloration inhabituelle ou une croissance rapide doivent alerter et conduire à des explorations complémentaires.
Chez le nouveau-né et le nourrisson, les lésions bénignes les plus fréquentes sont les nævus congénitaux, les hémangiomes, les hamartomes épidermiques ou annexiels, les mastocytomes, l’histiocytose céphalique bénigne, l’hamartome fibreux infantile et certaines tumeurs adipeuses ou fibroblastiques.
Chez le petit enfant, le pilomatricome, le xanthogranulome juvénile, le botryomycome ou encore l’hamartome conjonctif dermique sont plus fréquemment rencontrés.
Chez le grand enfant, on observe davantage de nævus acquis, d’histiocytofibromes, d’angiofibromes, de tumeurs annexielles pilaires ou sudorales (trichoépithéliomes, trichilemmomes, syringomes, syringocystadénome papillifère), ainsi que des neurofibromes.
Il est important de rappeler que certaines tumeurs bénignes peuvent constituer le premier signe d’une maladie génétique sous-jacente et doivent alors s’intégrer dans une réflexion syndromique.
Conduite à tenir selon l’âge et la topographie
-Période néonatale
oNodule unique médian
Un nodule médian doit faire évoquer un dysraphisme spinal jusqu’à preuve du contraire. Une IRM est indiquée en cas de signes associés à haut risque (hypertrichose localisée, fossette atypique ou complexe, fistule dermoïde, hémangiome infantile > 2,5 cm, appendice cutané, acrochordon, lipome). Une échographie médullaire peut être réalisée précocement avant l’ossification des arcs postérieurs. Les diagnostics différentiels incluent kyste dermoïde, lipome, céphalocèle, gliome nasal, hétérotopie méningée ou cérébrale, hémangiome infantile, ou encore bourgeon charnu ombilical révélant une anomalie du canal vitellin nécessitant une échographie abdominale.
oNodule unique non médian
Les principales hypothèses sont l’hématome, l’abcès, la cytostéatonécrose du nouveau-né, la fibromatosis colli ou plus rarement une maladie génétique rare.
La cytostéatonécrose du nouveau-né survient chez un enfant en bon état général dans les 15 jours suivant l’accouchement. Elle se manifeste par un érythème évoluant vers un placard d’hypodermite rouge violine, parfois fistulisé et douloureux, siégeant préférentiellement au dos, au cou ou aux membres supérieurs. Une surveillance prolongée de la calcémie pendant 3 mois est indispensable en raison du risque d’hypercalcémie.
La fibromatosis colli correspond à une pseudotumeur du muscle sterno-cléido-mastoïdien apparaissant entre 2 et 8 semaines de vie, souvent associée à un traumatisme obstétrical et pouvant entraîner un torticolis.
La Fibrodysplasie ossifiante progressive doit être évoquée devant des nodules précoces du scalp associés à des malformations congénitales des hallux. Cette affection autosomique dominante, le plus souvent liée à une mutation de novo du gène ACVR1, se caractérise par une ossification hétérotopique déclenchée par les traumatismes.
o
Nodules multiples dans les plis
Dans les plis, des abcès staphylococciques néonataux peuvent se présenter sous forme de nodules bilatéraux prédominant dans les grands plis, sans signes généraux, avec isolement de Staphylococcus aureus et hémocultures stériles. L’évolution est souvent favorable sous antibiothérapie.
o
Nodules multiples en dehors des plis
En dehors des plis, l’aspect en « blueberry muffin baby » doit faire évoquer une hématopoïèse extramédullaire cutanée. Il est alors indispensable de rechercher une infection congénitale, une hémolyse néonatale, un syndrome transfuseur-transfusé ou une pathologie tumorale telle qu’un neuroblastome, une leucémie congénitale, un rhabdomyosarcome ou une histiocytose. Le syndrome de Bean, associant malformations veineuses multiples et atteinte digestive, constitue un autre diagnostic à évoquer.
-Enfance
oMalformations vasculaires
Il convient de distinguer les malformations à flux lent (veineuses, lymphatiques) des malformations à flux rapide (artérioveineuses), dont la prise en charge et les complications diffèrent.
oNodules du visage
La pyodermite froide, parfois considérée comme appartenant au spectre de la rosacée pédiatrique, peut toucher les paupières inférieures et s’accompagner de séquelles cicatricielles importantes, notamment en localisation sous-orbitaire. Elle est fréquemment associée à des chalazions (42%) et nécessite une prise en charge prolongée, les antibiotiques étant souvent peu efficaces.
oNodules cervicaux
Les adénites à mycobactéries non tuberculeuses sont en augmentation chez l’enfant immunocompétent, principalement entre 2 et 5 ans. Elles surviennent volontiers en hiver ou au printemps et se manifestent par une adénopathie cervicale unilatérale, indolore, inflammatoire, parfois fistulisée. Une attitude conservatrice peut être discutée, notamment lorsque la lésion est proche du nerf facial, et la décision thérapeutique doit être partagée avec la famille.
oNodules de la cuisse
Le granulome post-vaccinal persistant se présente comme un placard infiltré, nodulaire, érythémateux et prurigineux, parfois associé à une hypertrichose locale. Le délai d’apparition varie de 1 mois à 6 ans après l’injection. L’administration intramusculaire stricte des vaccins est recommandée. L’évolution peut être prolongée sur plusieurs années et une exérèse est parfois nécessaire.
oNodules des plis
Le nodule scabieux doit être évoqué en cas de gale. Le granulome annulaire sous-cutané du scalp est fréquent chez l’enfant et représente près de 40 % des formes pédiatriques. Une recherche de diabète est recommandée, bien que celui-ci ne soit retrouvé que dans une minorité de cas. La rémission spontanée survient dans environ 90 % des cas avec un délai médian d’1 an, mais les récidives sont fréquentes. Les chéloïdes complètent les diagnostics possibles dans cette localisation.
Pr E. Launay
En février 2025, la Haute Autorité de santé a actualisé ses recommandations concernant la borréliose de Lyme et les autres maladies vectorielles transmises par les tiques. La maladie de Lyme est due à une infection par Borrelia burgdorferi et transmise par des tiques du genre Ixodes. D’autres infections peuvent également être transmises par ces tiques, notamment la fièvre récurrente à tiques, la tularémie, les rickettsioses, l’anaplasmose, la babésiose ou encore l’encéphalite à tiques.
En France, l’étude CITIQUE estime qu’environ 15 % des tiques sont porteuses de Borrelia burgdorferi, un chiffre comparable aux données européennes (11–15 %). L’incidence pédiatrique est estimée entre 10 et 50 cas pour 100 000 enfants par an, avec une augmentation observée entre 2012 et 2020. Les enfants représentent environ 32 % des cas, avec un pic d’incidence entre 5 et 9 ans. Le risque de transmission après une piqûre de tique est estimé entre 1 et 4 %. Les tiques sont plus actives du printemps à l’automne. Il n’a pas été démontré de lien direct entre température et densité de tiques, mais celles-ci sont plus abondantes dans les zones à faible variation thermique et végétale. La densité des petits rongeurs principaux réservoirs, joue un rôle majeur, notamment en lien avec la disponibilité en fruits à coques et baies. La déforestation, en réduisant les prédateurs, favorise la prolifération des rongeurs et indirectement celle des tiques.
Il n’y a pas d’indication à une antibioprophylaxie systématique après morsure de tique. La surveillance clinique est essentielle, avec recherche d’un érythème migrant dans les 4 semaines suivant la piqûre. La prévention repose principalement sur le port de vêtements longs en zone à risque. Les répulsifs appliqués sur les vêtements ne sont plus recommandés en raison de leur toxicité environnementale et individuelle. Les répulsifs cutanés sont contre-indiqués avant l’âge de 6 mois et leur utilisation ultérieure doit être discutée au cas par cas, le plus souvent évitée chez l’enfant.
L’érythème migrant (EM) est la forme localisée précoce de la maladie et peut être unique ou multiple (forme disséminée précoce). Il apparaît après une incubation de 3 à 30 jours. Il s’agit d’une lésion érythémateuse ronde ou ovalaire, s’étendant de manière centrifuge autour du site de piqûre, indolore et non prurigineuse. Des signes généraux discrets (fébricule, myalgies) peuvent être associés. Le diagnostic est exclusivement clinique. Il n’y a aucun intérêt à réaliser une sérologie ou un autotest à ce stade.
La principale évolution des recommandations concerne la place de la doxycycline. La doxycycline est désormais recommandée en première intention, y compris chez l’enfant de moins de 8 ans, à la posologie de 4 mg/kg/jour (maximum 200 mg/jour) en 2 prises, pendant 10 jours en cas d’EM isolé et 14 jours en cas d’EM multiple. Le risque de coloration dentaire définitive est essentiellement décrit pour des traitements supérieurs à 3 semaines. L’amoxicilline constitue une alternative, notamment chez l’enfant de moins de 20 kg ou en cas d’impossibilité de prise de comprimés, à la posologie de 50 mg/kg/jour en 3 prises pendant 14 jours. L’azithromycine représente une 3ème option. En pratique, la doxycycline peut être délayée dans l’eau, prise avec un grand verre d’eau, au cours d’un repas sans produit laitier, et il est recommandé d’attendre 1h avant le coucher.
Le lymphocytome borrélien correspond à une forme disséminée précoce. Il se manifeste par un nodule ou une plaque rouge violacée, indolore, de 1 à 5 cm, d’évolution lente, parfois associé à un érythème migrant. Les signes généraux sont le plus souvent absents. La sérologie est positive dans plus de 70 % des cas. Le traitement repose sur les mêmes molécules que pour l’EM, mais pour une durée de 21 jours.
La neuroborréliose survient dans 90 % des cas au stade disséminé précoce. Le diagnostic repose sur la mise en évidence d’une synthèse intrathécale d’immunoglobulines, plus précoce que la sérologie sanguine dans les 6 premières semaines. Une ponction lombaire doit être discutée chez l’enfant présentant une paralysie faciale périphérique, en particulier si elle est bilatérale (environ un quart des cas), associée à un érythème migrant récent, à des céphalées, des douleurs radiculaires ou d’autres symptômes inhabituels (arthralgies, myalgies, asthénie), et survenant en période saisonnière compatible. La doxycycline est recommandée en 1ère intention (4 mg/kg/j, maximum 200 mg/j) pendant 14 jours en cas de forme précoce et 21 jours en cas de forme tardive. La ceftriaxone constitue l’alternative, notamment chez l’enfant de moins de 20 kg. Le suivi est purement clinique et une sérologie de contrôle systématique n’est pas indiquée.
Parmi les autres formes pédiatriques, on peut citer l’arthrite de Lyme, plus fréquente aux États-Unis qu’en Europe. Elle se présente typiquement sous forme de mono- ou oligoarthrite, touchant surtout le genou, sans fièvre. Le diagnostic repose sur la sérologie et l’analyse du liquide articulaire, avec PCR. Le traitement repose sur une antibiothérapie prolongée de 28 jours : doxycycline chez l’enfant de plus de 8 ans ou amoxicilline chez l’enfant plus jeune. En 2nd intention, la ceftriaxone peut être utilisée. En cas de forme réfractaire avec PCR négative, une prise en charge rhumatologique est indiquée, incluant AINS, infiltrations ou immunomodulateurs. Il peut aussi exister des atteintes cardiaques à type de blocs auriculo-ventriculaires, bien que rares, ils doivent être recherchés en cas de forme disséminée. Le traitement repose sur la ceftriaxone intraveineuse avec relais par doxycycline pour une durée totale de 21 jours. Les atteintes ophtalmologiques sont quant à elles très rares et peuvent se manifester par une uvéite, une kératite ou une neuropathie optique et justifient un traitement par ceftriaxone pendant 21 jours.
Le syndrome post-borréliose de Lyme traitée correspond à la persistance de symptômes pendant plus de 6 mois après une borréliose documentée et correctement traitée, en l’absence de cause alternative identifiée. Les symptômes associent asthénie, douleurs musculosquelettiques et troubles cognitifs, avec altération de la qualité de vie.
Il n’y a pas d’indication à une antibiothérapie prolongée. La prise en charge est similaire à celle des troubles neuro-fonctionnels et repose sur la rééducation, l’activité physique adaptée et l’accompagnement psychologique. Une vigilance particulière est nécessaire afin d’éviter des situations de surmédicalisation ou de maltraitance médicale.
En résumé : Les recommandations insistent sur l’absence d’antibioprophylaxie après morsure de tique, la restriction des répulsifs (abandon des produits vestimentaires et contre-indication avant 6 mois pour les répulsifs cutanés), la place centrale de la doxycycline en 1ère intention y compris chez les enfants de moins de 8 ans, la réduction de la durée de traitement de l’érythème migrant, une meilleure définition des indications de la ponction lombaire en cas de paralysie faciale, et une approche structurée du syndrome post-borréliose sans recours aux antibiothérapies prolongées
Dr M. Blanchard
Les lymphoproliférations T cutanées pédiatriques constituent des entités rares, dominées par 2 diagnostics principaux : le mycosis fongoïde et la papulose lymphomatoïde. Leur reconnaissance est essentielle pour éviter les retards diagnostiques, limiter les surtraitements et informer de manière adaptée les familles, compte tenu d’un excellent pronostic global.
Le Mycosis fongoïde est le plus fréquent des lymphomes cutanés, appartenant au groupe des lymphomes non hodgkiniens. Les formes pédiatriques, définies par un diagnostic avant l’âge de 18 ans, représentent environ 3 à 20 % de l’ensemble des cas. Il s’agit d’une maladie rare chez l’enfant, pour laquelle les données reposent essentiellement sur des séries rétrospectives et des consensus d’experts. Chez l’enfant, la maladie se manifeste majoritairement par des patchs et des plaques, plus rarement par des nodules. Les formes hypopigmentées et folliculotropes sont plus fréquentes que chez l’adulte. L’évolution est généralement chronique et indolente, avec un taux de survie spécifique supérieur à 97 % à 10 ans dans les formes précoces. Les stades précoces (IA à IIA) correspondent à une maladie à surveiller, pas nécessairement à traiter. Ils se distinguent clairement des formes avancées (≥ IIB), beaucoup plus rares en pédiatrie. Le diagnostic repose sur une corrélation anatomo-clinique rigoureuse. La classification TNMB nécessite une biopsie cutanée avec immunohistochimie. Une échographie des aires ganglionnaires et abdominales est recommandée, complétée au cas par cas par des examens d’imagerie supplémentaires. L’objectif thérapeutique n’est pas de modifier le pronostic vital, mais de contrôler les manifestations cliniques et leurs conséquences (prurit, retentissement esthétique, fonctionnel et psychologique), tout en limitant les effets indésirables à long terme. Aucune donnée ne démontre à ce jour un impact des traitements sur l’évolution à long terme dans les formes précoces. Une attitude expectative est donc légitime et fréquente aux stades précoces. En 1ère intention, les dermocorticoïdes topiques et la photothérapie UVB sont proposés, bien que cette dernière soit moins efficace dans les formes folliculotropes. La PUVA-thérapie peut être discutée en cas de plaques épaisses. Le méthotrexate est parfois utilisé. En 2nd intention, peuvent être envisagés la photothérapie, la chlorméthine topique, le béxarotène topique, les rétinoïdes systémiques, l’IFN-alpha ou le méthotrexate.
La Papulose lymphomatoïde est une lymphoprolifération T cutanée CD30+ bien décrite chez l’adulte, avec un pic entre 40 et 50 ans. Elle se caractérise par une survie spécifique proche de 100 % à 10 ans, mais expose à un risque accru de lymphomes associés, principalement mycosis fongoïde et lymphome anaplasique à grandes cellules (ALCL). Chez l’enfant, la maladie est rare et les données limitées. L’âge moyen au diagnostic est d’environ 7 ans, avec une prédominance masculine. Le délai diagnostique peut être long en raison de la polymorphie clinique et des diagnostics différentiels fréquents (piqûres d’insectes, pityriasis lichénoïde, rash para-infectieux, molluscum contagiosum, varicelle ou autres lymphomes cutanés T). Cliniquement, il s’agit de papules ou de petits nodules du tronc et des membres, évoluant par poussées spontanément résolutives en quelques semaines. Les caractéristiques histologiques sont comparables à celles de l’adulte, avec mise en évidence fréquente d’un clone T en biologie moléculaire (environ 76 % des cas). En l’absence de point d’appel clinique, aucun bilan systémique n’est recommandé en première intention en dehors de la biopsie cutanée. Les explorations complémentaires sont discutées au cas par cas. Une attitude expectative est envisageable et proposée dans près d’un cinquième des cas. Les traitements visent essentiellement à contrôler les symptômes et l’impact cosmétique : dermocorticoïdes topiques, UVB, voire méthotrexate dans certaines formes plus étendues. Un suivi prolongé est recommandé en raison du risque, estimé à environ 10 % chez l’enfant, de développer ultérieurement un mycosis fongoïde ou un lymphome anaplasique à grandes cellules, parfois également d’âge pédiatrique. Le suivi proposé est annuel pendant cinq ans, puis tous les deux ans.
Les lymphoproliférations T cutanées de l’enfant sont des maladies rares, encore peu décrites. Leur pronostic en termes de survie est excellent, ce qui impose une approche mesurée. L’annonce diagnostique doit être particulièrement prudente compte tenu de la charge émotionnelle associée au terme de « cancer » chez l’enfant. Le diagnostic repose sur une corrélation anatomo-clinique précise. Dans la majorité des cas, notamment aux stades précoces du mycosis fongoïde et dans la papulose lymphomatoïde, une attitude expectative est justifiée. Le traitement vise avant tout le contrôle symptomatique et la qualité de vie, dans le cadre d’un suivi à long terme adapté.
Dr L. Chouchana, Dr J-M. Debarre
La prescription hors autorisation de mise sur le marché (hors AMM) constitue une réalité quotidienne en dermatologie pédiatrique. Elle se définit comme un usage non conforme au résumé des caractéristiques du produit (RCP), mais conforme aux données acquises de la science. Elle doit être distinguée du mésusage ou des erreurs médicamenteuses. Dans un contexte où la majorité des médicaments n’ont pas été spécifiquement évalués chez l’enfant, cette pratique reflète le décalage persistant entre besoins cliniques et données réglementaires disponibles.
Selon les études européennes, entre 30 et 80 % des enfants reçoivent au moins un médicament sans ou hors AMM, avec des taux particulièrement élevés chez les nouveau-nés et nourrissons. Une analyse européenne de 2017 rapportait des taux de prescriptions hors AMM allant de 13 à 69 % en milieu hospitalier et de 2 à 100 % en ambulatoire.
En dermatologie, cette situation est particulièrement marquée dans les maladies rares, les dermatoses inflammatoires chroniques et les indications systémiques (biothérapies, immunosuppresseurs, rétinoïdes). L’enfant reste historiquement sous-représenté dans les essais cliniques pour des raisons éthiques, méthodologiques et économiques, si bien que de nombreuses molécules disposent d’une AMM chez l’adulte sans extension pédiatrique formelle, malgré un usage validé par l’expérience clinique et les recommandations d’experts.
Les antibiotiques, les inhibiteurs de la pompe à protons (par exemple l’oméprazole chez le nourrisson), la mélatonine, certaines vitamines ou encore des psychotropes illustrent cette problématique. Même en dermatologie, l’AMM du propranolol pour l’hémangiome infantile est relativement récente, témoignant du délai entre pratique clinique et reconnaissance réglementaire.
En France, la prescription hors AMM est légale, sous réserve de respecter plusieurs conditions : absence d’alternative disposant d’une AMM adaptée, existence de données scientifiques soutenant l’efficacité et la tolérance, respect des recommandations en vigueur, information claire et loyale des titulaires de l’autorité parentale et traçabilité dans le dossier médical. Le prescripteur engage sa responsabilité et doit procéder à une évaluation rigoureuse du rapport bénéfice/risque, particulièrement chez l’enfant en raison des incertitudes sur les effets à long terme. Des dispositifs spécifiques peuvent encadrer certaines situations, notamment l’accès précoce ou compassionnel, ainsi que des protocoles hospitaliers ou recommandations temporaires d’utilisation.
L’enfant n’étant pas un « adulte en miniature », son immaturité d’organes et de système enzymatiques, notamment des cytochromes hépatiques, entraîne des différences majeures de pharmacocinétique et de pharmacodynamie. Les formes galéniques sont souvent inadaptées, et certaines maladies diffèrent dans leur expression et leur évolution. Ces éléments renforcent la nécessité d’études spécifiques.
Le risque d’effets indésirables est plus élevé en cas de prescription hors AMM. Un risque relatif de 1,67 d’événement indésirable médicamenteux a été rapporté, et près de 30 % des effets indésirables à l’origine d’une hospitalisation seraient associés à des prescriptions hors AMM.
En 2007, le règlement européen a instauré le plan d’investigation pédiatrique (PIP), qui impose aux laboratoires un programme complet d’études pédiatriques avant la demande d’AMM, sauf dérogation ou report accordé par le Paediatric Committee. Les objectifs sont d’encourager le développement de médicaments adaptés aux enfants, de garantir leur sécurité et leur efficacité, d’améliorer l’information disponible et d’encadrer la recherche dans un cadre éthique et réglementaire. Toutefois, les résultats restent en deçà des attentes : entre 2007 et 2015, seulement 25 % des nouveaux médicaments disposaient d’un volet pédiatrique.
La prise en charge des teignes illustre concrètement les conséquences du retrait ou de l’absence d’AMM. La griséofulvine, seul traitement systémique disposant d’une AMM pédiatrique en France, a été retirée du marché en 2021, créant une impasse thérapeutique. La terbinafine, bien que disposant d’une AMM de la FDA pour certaines dermatophytoses, ne bénéficie pas d’une validation complète chez les jeunes enfants, notamment en dessous de 4 ans ou 20 kg, faute d’études pharmacocinétiques. L’itraconazole, dont la forme buvable a été retirée du marché en 2025, reste autorisé dès 6 mois. Un groupe de travail sous l’égide de l’ANSM a été constitué pour discuter des posologies adaptées. Une étude nationale multicentrique rétrospective (2022–2024) chez des enfants de moins de 10 kg montre la diversité des pratiques (itraconazole, terbinafine, fluconazole), illustrant l’hétérogénéité des prescriptions hors AMM en situation réelle.
La prescription hors AMM en dermatologie pédiatrique est une pratique fréquente, souvent indispensable, mais non dénuée de risques. Elle nécessite une expertise, une argumentation scientifique solide et une information claire des familles. Le développement d’essais pédiatriques adaptés demeure un enjeu majeur pour sécuriser les pratiques et réduire les inégalités d’accès à des traitements validés.
Pr L. Martin, Dr E. Riquin, Pr P. Vabres
La dermato-pédopsychiatrie met en lumière l’impact majeur de l’apparence cutanée sur la construction psychique de l’enfant et de l’adolescent. Les dermatoses visibles exposent fréquemment à des situations de stigmatisation, pouvant entraîner harcèlement, isolement social et auto-stigmatisation.
Le concept de stigmate, décrit par Erving Goffman en 1963, désigne une caractéristique qui discrédite un individu et devient son trait dominant aux yeux des autres. Il distingue les stigmates corporels, les stigmates moraux et les stigmates d’appartenance. En dermatologie, la différence visible peut ainsi réduire l’enfant à sa maladie, avec un retentissement important sur l’estime de soi.
La stigmatisation peut être externe, ressentie ou intériorisée. À l’adolescence, le « spotlight effect » majore la conviction d’être constamment observé et jugé. Certains jeunes développent des stratégies d’adaptation centrées sur le problème, comme la recherche de traitement ou la réévaluation positive, tandis que d’autres adoptent des stratégies centrées sur l’émotion, comme l’évitement ou le déni, souvent moins efficaces à long terme.
L’impact psychique est particulièrement marqué dans des pathologies comme l’acné sévère. Près d’1/5 adolescent rapporte des idées suicidaires, proportion encore plus élevée en cas d’acné importante. Les données récentes suggèrent que l’isotrétinoïne n’augmente pas le risque suicidaire et que l’amélioration clinique peut au contraire réduire la détresse psychologique, sous réserve d’un suivi attentif.
La chevelure possède également une forte valeur symbolique. Elle est associée à la séduction, à l’identité et à la puissance, comme l’illustre la figure biblique de Samson, dont la force était liée à ses cheveux. Les pathologies capillaires chez l’enfant et l’adolescent peuvent ainsi atteindre profondément le sentiment d’identité et d’appartenance.
Les scarifications, ou NSSI (Non-Suicidal Self-Injury), correspondent à des atteintes corporelles volontaires sans intention suicidaire. Elles constituent le plus souvent un mode de régulation émotionnelle. L’acte permet une diminution transitoire d’une tension interne intense et peut procurer un soulagement lié à la libération d’endorphines. Il ne s’agit pas d’une recherche de plaisir au sens hédonique, mais d’une tentative de contrôle d’une détresse psychique.
En conclusion, le dermatologue a un rôle clé dans le repérage de ces situations. Face à des cicatrices évocatrices ou à une souffrance manifeste liée à l’apparence, une attitude empathique et un relais vers une prise en charge pédopsychiatrique sont essentiels. Une approche intégrée, associant traitement dermatologique, soutien psychologique et travail sur la stigmatisation sociale, permet d’améliorer à la fois la santé cutanée et le bien-être global de l’enfant.
Pr L. Martin, Pr S. Barbarot
a.La saga de la prévention primaire de la dermatite atopique (DA) par les émollients : saison 2
Emollients to Prevent Pediatric Eczema: A Randomized Clinical Trial – JAMA Dermatol – Eric L.Simpson et Al.
La prévention de la DA par l’application précoce et quotidienne d’émollients chez le nourrisson a suscité un fort intérêt, sur l’hypothèse qu’un renforcement précoce de la barrière cutanée pourrait limiter la sensibilisation allergénique et l’inflammation cutanée.
En 2020, les essais BEEP (Barrier Enhancement for Eczema Prevention) et PreventADALL (Skin emollient and early complementary feeding to prevent infant atopic dermatitis) sont sont penchés sur la question. Dans la 1ère étude l’on a évalué l’application quotidienne d’un émollient dès les premières semaines de vie chez des nourrissons à haut risque atopique. Les résultats n’ont pas montré de réduction significative de l’incidence de l’eczéma à 2 ans dans le groupe traité par rapport au groupe contrôle. Dans la 2nd, l’application régulière d’émollients dès la naissance, seule ou associée à une diversification alimentaire précoce était étudiée. Là encore, aucune diminution significative de la prévalence de la dermatite atopique n’a été démontrée à l’âge d’un an. L’intervention combinée (émollients + introduction alimentaire précoce) n’a pas montré d’effet préventif supplémentaire. Cette problématique avait donc été abandonnée jusqu’en 2025 où un nouvel essai a vu le jour évaluant l’intérêt d’une application quotidienne d’émollients dès les premières semaines de vie et pendant 1 an pour prévenir la survenue d’un eczéma atopique chez des nourrissons à risque (antécédent familial d’atopie). Les résultats ont montré une incidence plus faible de dermatite atopique à 2 ans : 36,1 % dans le groupe émollient vs 43,0 % dans le groupe contrôle, avec RR de 0,84 (95 % CI 0,73–0,97 ; P = .02). L’effet préventif était plus marqué chez les enfants non à haut risque atopique et dans les foyers avec un chien.
Ces données, suggèrent que la prévention de la DA ne dépend pas du concept "émollient" en soi, mais du bon produit, au bon moment, chez la bonne population.
b.Nouvelle ère pour les épidermolyses bulleuses sévères : les thérapies géniques enfin accessible
Trial of Beremagene Geperpavec (B-VEC) for Dystrophic Epidermolysis Bullosa – NEJM – Guide SV et al.
Cette étude publiée dans The New England Journal of Medicine en 2022 portait sur un essai de thérapie génique topique, le beremagene geperpavec (B-VEC), pour l’épidermolyse bulleuse dystrophique. Le B-VEC est un vecteur viral délivrant une version fonctionnelle du gène COL7A1 directement dans les zones de peau lésée, afin de restaurer la production de collagène de type VII et favoriser la cicatrisation. Dans cet essai contrôlé randomisé, des patients atteints d’épidermolyse bulleuse dystrophique ont reçu à la fois une application topique de B-VEC sur une de leur plaie et un placebo sur une autre, le contrôle était donc intra-patient.
Les résultats ont montré que l’application de B-VEC améliorait significativement la cicatrisation des plaies et les douleurs en lien avec celles-ci. Cette amélioration biologique et clinique s’est accompagnée d’un bon profil de tolérance, sans événements indésirables graves attribués au traitement.
Cet essai constitue une démonstration clinique de l’efficacité d’une thérapie génique locale dans une génodermatose sévère, ouvrant la voie à de nouvelles approches personnalisées pour les maladies cutanées génétiques jusqu’ici sans traitement curatif.
Cet essai à également ouvert la voie à l’accès précoce de ce traitement en France depuis octobre 2025.
c.Pronostic des mélanonychies de l’enfant : un risque de mélanome ?
Five and 10-year evolution of longitudinal melanonychia appearing before the age of 5: A multicenter prospective cohort study from the International Dermoscopy Society – J Am Acad Dermatol – Pham F.K et Al
Cette étude prospective multicentrique a suivi des enfants présentant une mélanonychie longitudinale apparue avant l’âge de 5 ans, avec un suivi à 5 et 10 ans. La majorité de ces bandes pigmentées se sont révélées bénignes, souvent associées à des nævi matriciels ou congénitaux et ont régressées spontanément. Les caractéristiques dermatoscopiques inquiétantes, comme l’irrégularité ou la multicoloration, n’ont pas permis de prédire l’apparition d’un mélanome, lequel reste exceptionnel chez l’enfant prépubère. Ces résultats suggèrent qu’une surveillance régulière est préférable à une excision systématique, et que les interventions invasives doivent être réservées aux cas présentant des modifications cliniques défavorables. Aucun cas de mélanome n’a été observé après 10 ans de suivi.
d.Taches pigmentées congénitales : quelles sont les causes ?
Mosaic disorders affecting pigmentation - part 2: how to make a genetic diagnosis – Br J Dermatol – Kinsler V.
Les troubles mosaïques affectant la pigmentation sont des affections génétiques caractérisées par la présence de cellules génétiquement différentes dans un même individu, entraînant des anomalies segmentaires ou linéaires de la pigmentation cutanée. La démarche diagnostique repose sur une anamnèse détaillée et un examen clinique précis, incluant la distribution des lésions selon les lignes de Blaschko, la présence éventuelle de anomalies extra-cutanées et l’histoire familiale. Les investigations génétiques nécessitent souvent un prélèvement cutané ciblé sur la zone affectée, car le variant pathogène peut être absent dans le sang périphérique. Les techniques de séquençage modernes, comme le NGS (Next-Generation Sequencing) et le séquençage profond à très haute sensibilité, permettent d’identifier les mosaïques somatiques même à faible proportion. La confirmation génétique est essentielle pour préciser le diagnostic, le pronostic, et le conseil génétique, notamment en cas de risque de transmission germinale.
e.Changement de paradigme dans la prise en charge des hémangiomes infantiles
Paradigm shift in the management of infantile hemangiomas in the beta-blocker era: A retrospective cohort study – J Am Acad Dermatol – Fernandez-Faith et al.
Cette étude rétrospective analyse l’évolution de la prise en charge des hémangiomes infantiles depuis l’avènement des bêta‑bloquants, en particulier le propranolol. Les auteurs ont comparé des cohortes d’enfants traités avant et après l’intégration systématique des bêta‑bloquants dans les protocoles thérapeutiques. L’introduction du propranolol a transformé la pratique, avec une forte réduction de l’utilisation de corticostéroïdes systémiques, d’interventions chirurgicales et de complications résiduelles. La majorité des hémangiomes répond bien à une initiation précoce de propranolol, avec une amélioration significative de la taille et de la couleur des lésions, un meilleur profil de tolérance et une réduction des séquelles fonctionnelles ou esthétiques. Les effets indésirables observés étaient généralement bénins et contrôlables, renforçant le rapport bénéfice/risque de cette approche. Enfin, l’étude souligne l’importance de protocoles structurés, d’une surveillance cardiovasculaire adaptée et d’un suivi multidisciplinaire pour optimiser les résultats chez les nourrissons traités par bêta‑bloquants.
f.Prise en charge de l’hémangiome infantile : sommes-nous tous d’accord ?
Paradigm shift in the management of infantile hemangiomas in the beta-blocker era: A retrospective cohort study – J Am Acad Dermatol – Fernandez Faith et Al.
Cette étude évalue la consistance des décisions thérapeutiques entre cliniciens (accord interobservateur) et au sein d’un même clinicien au fil du temps (accord intraobservateur) concernant la prise en charge des hémangiomes infantiles. Les résultats montrent que, malgré des recommandations claires et l’usage généralisé des bêta‑bloquants comme traitement de référence, il existe une variabilité significative dans les choix thérapeutiques entre praticiens, notamment pour les lésions à risque modéré ou les indications moins évidentes. Cette variabilité s’explique par des différences d’interprétation clinique, des évaluations discordantes du risque de complications, ainsi qu’une expérience pratique hétérogène. L’accord intraobservateur était généralement meilleur que l’accord interobservateur, ce qui suggère que chaque clinicien est relativement cohérent dans ses propres décisions, mais qu’il n’existe pas encore de consensus partagé parfaitement appliqué dans la pratique. Ces observations mettent en évidence la nécessité d’outils décisionnels standardisés, de lignes directrices claires et d’une formation concertée pour réduire la variabilité de prise en charge et optimiser les résultats fonctionnels et esthétiques des enfants atteints d’hémangiomes infantiles.
g.Prédisposition génétique au cancer : des signes cutanés visibles ?
Constitutional Mismatch Repair Deficiency: Scoping Review of a Cancer-Predisposition Syndrome With Distinctive Cutaneous Findings – Pediatr Dermatol – Mar et Al.
Le déficit constitutionnel du système de réparation des mésappariements est un syndrome de prédisposition aux cancers héréditaires autosomique récessif, résultant de variants pathogènes bi-alléliques dans les gènes du mismatch repair (MLH1, MSH2, MSH6, PMS2). Cette revue de la littérature souligne que ce déficit se caractérise par une incidence élevée de tumeurs pédiatriques multiples, incluant des cancers du système nerveux central, des lymphomes et des tumeurs gastro-intestinales, avec un âge de survenue souvent très précoce. La dermatologie joue un rôle clé car ce syndrome s’accompagne de manifestations cutanées évocatrices, notamment des macules café‑au‑lait atypiques souvent nombreuses, des tâches hypopigmentées, des lésions cutanées de type séborrhéique ou verruqueuse, ainsi que des lésions pseudo‑xanthomateuses, qui doivent alerter. Certaines de ces lésions peuvent ressembler à celles observées dans d’autres syndromes de prédisposition, mais leur association avec des antécédents familiaux de cancers précoces ou des tumeurs multiples en enfance devrait inciter à suspecter ce déficit. Le diagnostic repose sur une combinaison d’arguments cliniques et biologiques, incluant l’immunohistochimie des protéines MMR, la discrimination microsatellite et la confirmation génétique des variants bialléliques. La reconnaissance précoce de ce syndrome est essentielle car elle permet une surveillance oncologique adaptée, une prise en charge multidisciplinaire précoce et un conseil génétique précis pour les familles.
h.Pronostic : entre espoir et incertitudes
Hope and Uncertainty in Prognostic Discussions – Pediatrics – Superdock A. et Al.
Cet article explore comment les discussions pronostiques peuvent équilibrer l’honnêteté avec les familles et le maintien de l’espoir, notamment lorsque le pronostic est défavorable ou incertain. Les auteurs ont mené des entretiens semi‑structurés avec des enfants atteints de cancers à mauvais pronostic, des parents, des parents en deuil et des oncologues pour comprendre leurs recommandations sur la communication pronostique. La grande majorité des participants ont estimé que les cliniciens peuvent soutenir l’espoir tout en restant honnêtes sur le pronostic et les incertitudes associées. Quatre grands axes de recommandations ont émergé : (1) privilégier l’honnêteté, même sur l’incertitude ; (2) fournir expertise et leadership ; (3) offrir un soutien compatissant et individualisé ; et (4) reconnaître que l’incertitude. En pratique, ces résultats suggèrent que des outils de communication adaptés peuvent aider les cliniciens à naviguer les conversations difficiles, en intégrant à la fois transparence et soutien psychologique.
i.Incertitude : les internes sont-ils préparés ?
Educational Strategies to Prepare Trainees for Clinical Uncertainty – NEJM – Ilgen J. et Al.
Cet article met en évidence que l'incertitude clinique est une composante inévitable de la pratique médicale. Les auteurs insistent sur la nécessité de préparer les étudiants en médecine à gérer cette incertitude de manière réfléchie et sécurisée. Ils recommandent que les formateurs modélisent leur propre raisonnement clinique, en partageant ouvertement les hypothèses et les doutes. Il est également essentiel d'encourager la réflexion itérative et les discussions autour des décisions incertaines. La formation doit inclure la planification prospective, la surveillance continue des signes cliniques et l'évaluation constante des indices disponibles. Enfin, le développement de l'expertise adaptative par le mentorat, la pratique réflexive et un encadrement structuré permet aux futurs médecins de prendre des décisions éclairées, même dans des situations cliniques incertaines, améliorant ainsi la sécurité et la qualité des soins.
Créez en toute simplicité votre compte professionnel
Je crée mon compteAméliorez vos connaissances professionnelles en profitant de nombreux services exclusifs dans le domaine de la dermatologie : plus de 500 visuels de pathologies, des cas cliniques, des vidéos d’experts…
Bénéficiez d’options uniques telles que l’offre de contenus audio et de supports à proposer à vos patients.
Restez informé(e) des événements et des webinaires à venir, des dernières publications scientifiques et des innovations produit.