2 professionals
Coup d’œil du congrès WCPD 2025
Coup d’œil du congrès WCPD 2025
Améliorez vos connaissances professionnelles en profitant de nombreux services exclusifs dans le domaine de la dermatologie : plus de 500 visuels de pathologies, des cas cliniques, des vidéos d’experts…
Bénéficiez d’options uniques telles que l’offre de contenus audio et de supports à proposer à vos patients.
Restez informé(e) des événements et des webinaires à venir, des dernières publications scientifiques et des innovations produit.
Vous avez déjà un compte ? Se connecter
Rapports rédigés par le Dr Maria Florencia Martinez (pédiatre et dermatologue pédiatrique, Argentine) et le Dr Paola Stefano (dermato-pédiatre, Argentine).

Sujets liés
Rapports rédigés par le Dr Maria Florencia Martinez (pédiatre et dermatologue pédiatrique, Argentine)
Intervenant : Enrique Salvador Rivas Zaldivar (Guatemala)
| Caractéristique | Psoriasis | Dermatite séborrhéique |
|---|---|---|
| Squames | Blanc argentées, épaisses | Grasses, jaunâtre ou sèches |
| Plaques | Bien délimitées | Contour mal défini |
| Érythème | Important, surtout au-delà de la racine des cheveux | Contour moins bien défini, plus discret |
| Démangeaisons | Présentes | Également présentes → pouvant provoquer des lésions dues au grattage |
| Atteinte rétro-auriculaire | Fréquente | Moins fréquente |
| Desquamation périphérique | Plus fréquente dans la DS, la desquamation suit les tiges des cheveux |
Observée dans la DS, rarement dans le psoriasis |
Remarque : Les deux maladies peuvent présenter un érythème et une desquamation, ce qui rend le diagnostic clinique difficile à établir de manière isolée.
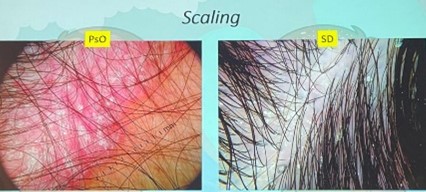
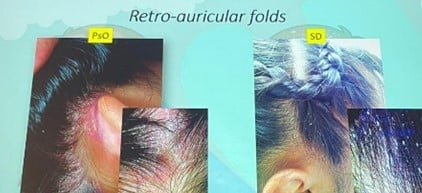
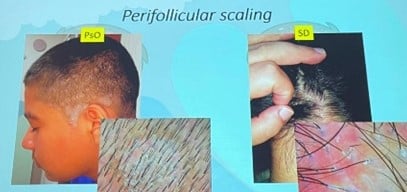
L’histologie elle-même peut ne pas être concluante dans certaines présentations concomitantes.
C’est là que la dermoscopie (trichoscopie) joue un rôle essentiel.
Les schémas vasculaires, principal facteur de différenciation :
| Observation dermoscopique | Psoriasis | Dermatite séborrhéique |
|---|---|---|
| Type de vaisseau | Points rouges, vaisseaux glomérulaires, boucles rouges torsadées |
Vaisseaux flous en arborescence, schémas atypiques |
| Localisation | Capillaires dermiques superficiels |
Vaisseaux plus profonds et moins bien définis |
| Aspect des squames | Épaisses, sèches, blanches | Jaunâtres, grasses |
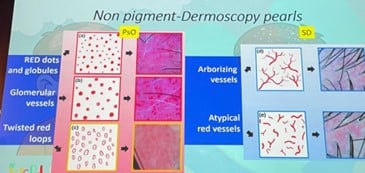
(Bruni et al., 2021)
Facteur aggravant : prolifération de Malassezia spp. dans tous les groupes d’âge.
Références :
- Bruni F, et al. Clinical and trichoscopic features in various forms of scalp psoriasis. J Eur Acad Dermatol Venereol. 2021 Sep ;35(9) :1830-1837.
- Silverberg NB. Scalp hyperkeratosis in children with skin of color: diagnostic and therapeutic considerations. Cutis. 2015 Apr;95(4):199-204
- Waśkiel-Burnat A et al. Differential diagnosis of red scalp: the importance of trichoscopy, Clinical and Experimental Dermatology, 2024, Setp; 49 (9): 961–968
- Kim GW et al. Dermoscopy can be useful in differentiating scalp psoriasis from seborrhoeic dermatitis. Br J Dermatol. 2011 Mar;164(3):652-6
Intervenant : Arturo Lopez Yañez Blanco (Mexique)
L’intervenant a commencé par donner une vue d’ensemble de la teigne du cuir chevelu en soulignant qu’il s’agit d’une infection fongique du cuir chevelu touchant principalement les enfants (98 %) et causée par des dermatophytes des genres Trichophyton et Microsporum.
Epidémiologie et formes cliniques
Les agents étiologiques varient selon les régions : M. canis, T. tonsurans, M. audouinii, T. mentagrophytes, T. verrucosum.
Deux formes cliniques principales :
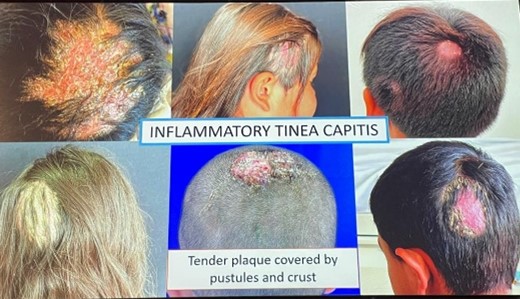
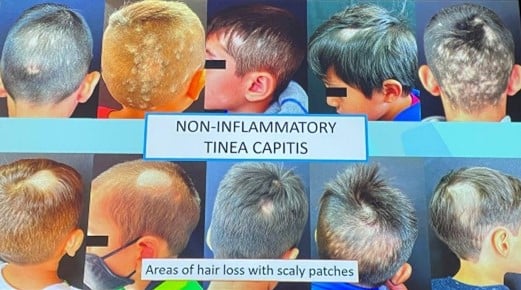
| Teigne du cuir chevelu inflammatoire | Teigne du cuir chevelu non inflammatoire |
| Plaques souples avec pustules et croûtes |
Plaques de perte de cheveux unitaires ou multiples
|
| Abcès douloureux | Plaques squameuses |
| Lymphadénopathie | Prurit |
Outils diagnostiques
| Teigne du cuir chevelu inflammatoire | Teigne du cuir chevelu non-inflammatoire |
| Pustules folliculaires | Cheveux en tire-bouchon |
| Croûtes | Gaine pilaire blanche |
| Desquamation périfolliculaire | Desquamation périfolliculaire et diffuse |
| Vaisseaux linéaires | Points noirs |
| Érythème | Cheveux en code Morse |
| Cheveux en virgule / en zigzag | |

Triade de signes (perte de cheveux, plaques squameuses, atteinte péritonéale) = valeur prédictive élevée (95 %).
Diagnostics différentiels :
Recommandations thérapeutiques
Les questions les plus souvent posées par les parents ont été abordées :
Présentation :
Diagnostics différentiels :
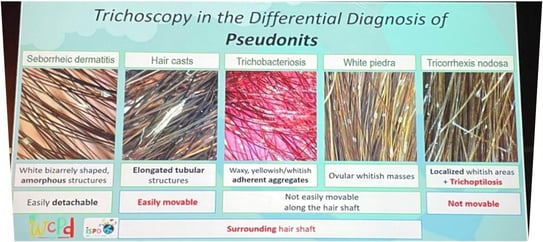
Différences trichoscopiques :
Vraies lentes : brunes avec des têtes ovales.
Pseudo-lentes : translucides, grisâtres, à extrémités noires.
Signes cliniques :
Traitement :
Aucun nouveau traitement majeur. Le traitement conventionnel reste efficace.
Il est essentiel d’informer les parents sur le comportement des poux et le mode de contagion.
TRAITEMENT SUR ORDONNANCE
PERMÉTHRINE
LOTION 1 %. Appliquer et laisser agir 10 minutes avant de laver les cheveux. Renouveler l’application au bout d’une semaine.
MALATHION
LOTION 0,5 %. Appliquer et laisser agir 8 à 12 heures avant de laver les cheveux. Renouveler l’application au bout d’une semaine.
ALCOOL BENZYLIQUE
LOTION 5 %. Appliquer et laisser agir 10 minutes avant de laver les cheveux. Renouveler l’application au bout d’une semaine.
IVERMECTINE
LOTION 0,5 %. Appliquer et laisser agir 10 minutes avant de laver les cheveux. Renouveler l’application au bout d’une semaine.
COMPRIMÉS ORAUX : 0,2 mg/kg/jour pendant 2 jours. Renouveler la prise au bout d’une semaine.
TMS
VOIE ORALE : 10 mg/kg/jour, 2 fois par jour pendant 3 jours. Renouveler la prise au bout d’une semaine.
Références :
Intervenante : Cecilia Navarro Tuculet (Argentine)
Présentation :
Types d’effluvium télogène :
Déclencheurs courants de l’effluvium télogène chez l’enfant :
Prévalence dans la population pédiatrique :
Diagnostic et évaluation :
Diagnostics différentiels :
Prise en charge :
Informations à retenir :
Références :
Intervenant : Arturo Lopez Yañez Blanco (Mexique)
Définition :
Épidémiologie :
Physiopathologie :
Caractéristiques cliniques :
Résultats diagnostiques :
Définition :
Épidémiologie :
Physiopathologie :
Caractéristiques cliniques :
Résultats diagnostiques :
Diagnostics différentiels :
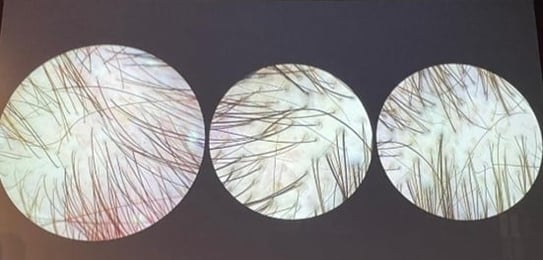

| Caractéristique | SAC | SAL |
|---|---|---|
| Âge au moment du diagnostic | 2 à 6 ans | 6 à 10 ans |
| Prédominance du sexe | Sexe féminin | Sexe féminin > Sexe masculin |
| Aspect des cheveux | Courts (moins de 10 cm), clairsemés, fins |
Fins, courts (moins de 20 cm), faciles à tirer |
| Test de traction | Négatif ou légèrement positif |
Positif, indolore |
| Trichoscopie | Normale | Points noirs rectangulaires/circulaires, points « sales » |
| Trichogramme | ↑ des cheveux télogènes | Cheveux anagènes (70 %) bulbes et racines déformés |
| Microscopie | Tiges de cheveux normales | Altération de la gaine interne de la racine du cheveu |
| Physiopathologie | Phase anagène raccourcie | Mauvais ancrage des cheveux anagènes |
| Composante génétique | Mutation WNT10A (40 %) | Défauts du gène de la kératine |
| Syndromes associés | Sclérodermie, micronychie, etc. | Syndrome de Noonan, TRPS |
| Pronostic | Bénin, s’améliore avec l’âge | |
| Utilisation du minoxidil | Possible si indiqué sur le plan psychosocial | |
Références :
Cranwell WC, et al. Loose anagen hair syndrome: Treatment with systemic minoxidil characterised by marked hair colour change. Australas J Dermatol. 2018;59(4):e286-e287.
Lemes LR, et al. Topical and oral minoxidil for hair disorders in pediatric patients: What do we know so far? Dermatol Ther. 2020;33(6):e13950.
Starace M, et al Short anagen syndrome: A case series and algorithm for diagnosis. Pediatr Dermatol. 2021;38(5):1157-1161
Intervenante : Miguel Marti (Argentine)
Symptômes fréquents :
Signes cliniques :
Présentation clinique :
| Modalités thérapeutiques | |
|---|---|
| Corticostéroïdes topiques | Traitement de première intention |
| Corticoïdes intralésionnels | Efficace en cas de maladie localisée |
| Corticostéroïdes systémiques | Dans les cas les plus graves |
| Hydroxychloroquine, méthotrexate | Réservé aux cas réfractaires |
Caractéristiques cliniques :
Références :
Intervenante : Lizet Rojano Fritz (Colombie)
| Patient | Fillette âgée de 8 ans. Pas d’antécédents médicaux personnels ou familiaux pertinents |
|---|---|
| Diagnostic initial | Pelade (déc. 2024) |
| Traitement | Clobétasol + Prednisone → Pas de réponse |
| Culture | Positive pour Microsporum canis |
| Traitement n° 1 | Terbinafine pendant 3 mois |
| Suivi | Alopécie centrale persistante → trichoscopie répétée : points noirs, cheveux cassés |
| Culture | Toujours positive |
| Traitement n° 2 | Griséofulvine pendant 6 mois |
| Observation | Vertex présentant une faible repousse, trichoptilose, cheveux fins |
| Diagnostic final | Teigne du cuir chevelu + trichotillomanie (la patiente a admis qu’elle s’arrachait les cheveux la nuit) |
Point à retenir :
Envisager un double diagnostic en cas d’alopécie chez l’enfant. Il faut toujours confirmer la présence d’une teigne du cuir chevelu au moyen d’une culture.
Résultats de la trichoscopie en fonction de la pathologie
| Caractéristique | Trichotillomanie | Teigne du cuir chevelu |
|---|---|---|
| Cheveux cassés Points noirs |
✅✅ | ✅ |
| Trichoptilose Cheveux en forme de flamme Cheveux en forme de tulipes Forme en V Aspect en point d’exclamation de micro cheveux |
✅ | ❌ |
| Points jaunes | ✅/❌ | ❌ |
| Patient | Fillette âgée de 8 ans |
|---|---|
| Antécédents | Plaque linéaire sur le visage depuis le vertex jusqu’au front/sourcils pendant 5 ans |
| Symptômes | Repli social, pas d’antécédents médicaux |
| Biopsie | Morphée linéaire |
| Trichoscopie | Perte des ouvertures folliculaires, cheveux cassés, points noirs, zones roses, pili torti. |
| IRM | Perte d’épaisseur du tissu sous-cutané (cuir chevelu et région du visage) |
| Panel auto-immun | Négatif |
| Traitement | Greffe de cheveux après 4 ans de lésion inactive |
| Résultat | Repousse efficace, amélioration de l’estime de soi |
Point à retenir :
La greffe de cheveux peut être efficace en cas de morphée inactive sans inflammation permanente.
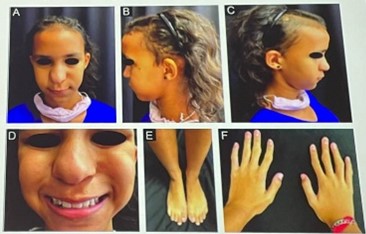
| Patient | Jeune fille de 15 ans |
|---|---|
| Antécédents | Hypotrichose congénitale |
| Trichoscopie | Normale |
| Trichogramme | Bulbes anagènes dystrophiques |
| Caractéristiques phénotypiques | Nez bulbeux, épiphyses des mains et des pieds en forme de cône, prognathisme maxillaire, lèvre supérieure mince |
| Test génétique | Délétion du chromosome 8q24.12 |
| Diagnostic | TRPS de type I |
| Traitement | Minoxidil topique → Bonne densité capillaire à 6 mois |
Point à retenir :
En cas d’hypotrichose congénitale, toujours rechercher des caractéristiques syndromiques et procéder à des tests génétiques.
Références :
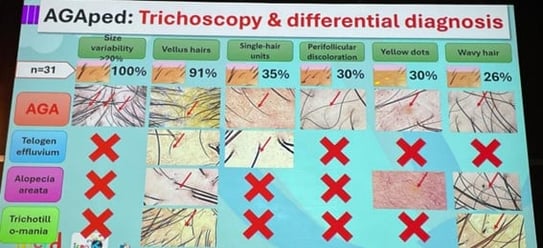
Intervenant : Luis Sanchez Dueñas (Mexique)
| Caractéristique | Fréquence |
|---|---|
| Variabilité du diamètre des cheveux | 100 % |
| Duvets | Élevée |
| Points jaunes | Occasionnelle |
| Signe péripilaire | Fréquente |
| Cheveux ondulés | Présente |
| Atrophie focale | Rare |
| Indication d’orientation | Mesures recommandées |
|---|---|
| Apparition pré-pubertaire | Orientation en endocrinologie |
| Patient de sexe masculin présentant un schéma de perte de cheveux féminin |
Panel hormonal |
| Patient de sexe féminin présentant des signes d’hyperandrogénie |
Panel hormonal |
| Tests de laboratoire suggérés | Testostérone, DHEA-S, SHBG, LH/FSH, vitamine D, glucose, insuline |
Diagnostic différentiel : effluvium télogène, pelade, trichotillomanie
Première intention (pour les deux sexes) :
En cas de réponse partielle :
Traitement complémentaire :
Traitement intensif (en cas de réponse insuffisante) :
| PATIENTS DE SEXE FÉMININ | PATIENTS DE SEXE MASCULIN | |
|---|---|---|
| PRÉPUBÈRES | MINOXIDIL TOPIQUE 2 % | |
| PUBÈRES | MINOXIDIL TOPIQUE 5 % | |
| AMÉLIORATION PARTIELLE | Minoxidil oral 0,25 à 0,5 mg/jour Finastéride topique Spironolactone topique/orale |
Minoxidil oral 1 à 2,5 mg/jour Finastéride topique |
| AMÉLIORATION LIMITÉE | Finastéride oral 2,5 mg/jour |
Finastéride oral 1 mg/jour |
| Médicaments | Événement | Mesures prises |
|---|---|---|
| Finastéride oral | Gynécomastie (homme) | Arrêt → Réversible |
| Minoxidil oral | Trichomégalie (excès de cils) | Réduction de la dose |
Références :
Intervenante : Sonia Ocampo-Garza (Mexique)
| Groupe | Modèle clinique | Traitement de première intention | Autres options |
|---|---|---|---|
| 1 | Moins de 50 % du cuir chevelu, activité légère, avec repousse | Corticostéroïdes topiques + Minoxidil | Anthraline, triamcinolone intralésionnelle, impulsions de dexaméthasone |
| 2 | Plus de 50 % du cuir chevelu, forte activité/résistance, modèle ophiasique | Dexaméthasone par voie orale + Clobétasol ou minoxidil topique | Méthotrexate, Cyclosporine, Hydroxychloroquine |
| 3 | Alopécie totalis/universalis | Immunothérapie de contact ± corticoïdes topiques | Inhibiteurs de JAK, stéroïdes oraux, méthotrexate |
| Type | Posologie | Remarques |
|---|---|---|
| Application topique | 2 à 5 % | Largement utilisé |
| Voie orale | 0,5 mg/jour | 71 % d’amélioration dans des séries de cas (l’hypertrichose est l’EI le plus fréquent) |
Agents :
Protocole :
Événements indésirables :
| Médicament | JAK ciblée | Utilisation chez l’enfant | Remarques |
|---|---|---|---|
| Tofacitinib | Pan-JAK | Hors AMM | 87 % de réponse chez 31 patients |
| Baricitinib | JAK1/2 | Hors AMM | Baisse du score SALT de 68 % |
| Ritlécitinib | JAK3/TEC | Approuvé par la FDA chez les plus de 12 ans | SALT inférieur à 20 dans 25 à 50 % des cas à 48 semaines |
| Étendue | Activité | Approche primaire | Options secondaires |
|---|---|---|---|
| Localisé | Actif | Corticostéroïdes topiques + Minoxidil | Anthraline |
| Inactif | Immunothérapie | ||
| Très large | Actif | Corticostéroïdes systémiques, inhibiteurs de JAK (Ritlécitinib : approuvé pour les plus de 12 ans), immunosuppresseurs | |
| Inactif | Immunothérapie ou inhibiteurs de JAK, corticostéroïdes systémiques |
Références :
Intervenante : Lawrence Eichenfield (États-Unis)
Malgré les avancées récentes en ce qui concerne les agents systémiques, les soins topiques restent essentiels dans la prise en charge de la DA, même chez les patients sous traitement systémique.
Le traitement topique comprend :
L’intervenante a abordé la question critique concernant le fait que les nouveaux agents topiques sont généralement étudiés par rapport à des véhicules, plutôt que par rapport à des comparateurs actifs tels que les corticostéroïdes, et généralement en monothérapie, ce qui ne reflète pas la pratique réelle où la thérapie combinée est courante.
Le principal message adressé aux patients est qu’il faut viser un contrôle à long terme de la maladie, que l’on peut définit de la façon suivante :
Les corticostéroïdes topiques restent le traitement de première intention dans de nombreux cas.
L’intervenante a parlé de la peur des stéroïdes, en notant l’existence d’un changement notable puisque les préoccupations liées à l’atrophie ont fait place à une croyance grandissante concernant la « dépendance aux stéroïdes topiques » (TSA - Topical steroid addiction). L’oratrice a cité la vidéo intitulée « Skin on Fire » (peau en feu) afin d’illustrer ce type de message. (https://www.youtube.com/watch?v=GuaBbsL1qKA)
Alors que le syndrome de sevrage des stéroïdes topiques (TSW - Topical Steroid Withdrawal) est un phénomène reconnu, en particulier chez l’adulte (rare dans la population pédiatrique) avec une utilisation à long terme, le concept de dépendance généralisée aux stéroïdes topiques manque de preuves.
Une enquête suédoise menée sur Internet auprès de patients se déclarant atteints de TSW (recrutés via Facebook) a permis de recueillir les informations suivantes :
Les données des essais cliniques peuvent surestimer l’efficacité perçue. Dans le cadre d’une étude sur des corticostéroïdes de puissance moyenne administrés deux fois par jour pendant quatre semaines :
Ces résultats reflètent une efficacité modeste à court terme, même pour les agents traditionnels, ce qui renforce le besoin de nouvelles thérapies.
1. Ruxolitinib topique (inhibiteur de JAK1/2)
Données pédiatriques : chez les 2 à 12 ans, environ 56 % ont obtenu une peau claire ou presque claire avec une application 2 fois/jour.
2. Tapinarof (agoniste des récepteurs d’aryl hydrocarbone)
Données à long terme :
3. Crisaborole (inhibiteur topique de la PDE4)
4. Roflumilast (inhibiteur de la PDE4)
| Formulation | Indication | Âge | Remarques |
|---|---|---|---|
| crème à 0,3 % | Psoriasis | à partir de 6 ans | Approuvé pour la première fois |
| mousse à 0,3 % | Dermatite séborrhéique | Adulte | Formulation plus récente |
| crème à 0,15 % | Dermatite atopique | à partir de 6 ans | Récemment approuvé |
| crème à 0,05 % | DA (étude sur des enfants âgés de 2 à 5 ans) | 2 à 5 ans | Pas encore approuvé |
5. Delgocitinib (inhibiteur de Pan-JAK)
Options topiques actuelles
Défis en matière de coûts et d’accès :
La thérapie combinée et la pratique concrète
Références :
Intervenant : Carsten Flohr (Royaume-Uni)
Alors que les traitements approfondis de la dermatite atopique (DA) gagnent en importance, les traitements systémiques conventionnels restent fondamentaux. Cette présentation aborde l’utilisation stratégique des traitements conventionnels et des nouveaux traitements systémiques, en s’appuyant sur des preuves cliniques et une étude de cas détaillée.
La dermatite atopique se caractérise par un cycle chronique de démangeaisons et de grattages qui entretient l’inflammation. Les facteurs d’exacerbation doivent être pris en charge avant l’instauration d’un traitement systémique :
Une prise en charge efficace doit comprendre les éléments suivants :
Méthotrexate
Cyclosporine
Après des réponses sous-optimales ou compliquées aux agents conventionnels, il est possible de mettre en place des traitements approfondis.
Dupilumab
Inhibiteurs de JAK (par ex., baricitinib, upadacitinib, abrocitinib)
Les méta-analyses en réseau (NMA) fournissent des données comparatives sur l’efficacité et la sécurité des traitements systémiques. Parmi les applications possibles, la plateforme d’aide à la décision clinique [EczemaTherapies.com] a été conçue pour :
Pour les patients dont la maladie évolue sur plusieurs fronts ou qui ne peuvent pas suivre une monothérapie, il peut s’avérer nécessaire de recourir à des combinaisons thérapeutiques.
Aperçu d’une étude de cas :
Un patient atteint d’une forme sévère et précoce de DA (EASI supérieur à 50 à l’âge de 10 ans) présentait :
Cette approche thérapeutique est désormais publiée dans Pediatric Dermatology comme un exemple d’intégration thérapeutique avancée.
La prise en charge optimale de la dermatite atopique nécessite un équilibre subtil entre les stratégies basées sur les lignes directrices, les preuves émergentes et les complexités concrètes. Le panorama thérapeutique est en croissance constante et, avec lui, la possibilité d’adapter les interventions en fonction de la sévérité de la maladie, des comorbidités et des préférences du patient - toujours entrée sur une approche pluridisciplinaire.
Références :
Noda S et al. The translational revolution and use of biologics in patients with inflammatory skin diseases. J Allergy Clin Inmunol. 2015;135(2):423-336
Intervenante : Elaine Siegfried (États-Unis)
Liste de contrôle avant l’instauration d’un traitement systémique :
| Éléments à prendre en compte | Descriptif |
|---|---|
| Endotype | Par ex., la DA classique, la dermatite de contact, le psoriasis et le chevauchement psoriasiforme. |
| Comorbidités non atopiques | Comorbidités systémiques, troubles du sommeil, HSV (herpès incognito), otite moyenne chronique, pneumonie. |
| Comorbidités atopiques | Particulièrement oculaire (risque de conjonctivite induite par le dupilumab). |
| Exposition aux corticostéroïdes | Topique et systémique. |
| Facteurs psychosociaux | Obstacles à l’observance, anxiété, phobie des aiguilles. |
| IMC et croissance | Tenir compte du statut nutritionnel. |
| Antécédents familiaux | Atopie, auto-immunité, immunodéficience. |
| Accès et coût | Susceptible d’influer sur le choix du traitement. |
Sous-types identifiés :
| Biomarqueur | Interprétation |
|---|---|
| IgE totales/spécifiques | Degré de sensibilisation atopique |
| Nombre d’éosinophiles | SHE si plus de 1500 × 3 |
| Albumine, protéines totales, globulines | Marqueurs nutritionnels et immunologiques |
| ANA, histone | Corrélation possible avec la formation d’anticorps anti-médicaments |
| Vitamine D | Souvent en déficit ; dépistage du rachitisme |
| Dépistage de la maladie cœliaque | En particulier dans le cas d’un retard de croissance |
| Panel immunologique | Les infections récurrentes justifient le dépistage de la salpingite |
Outils d’évaluation cliniques :
| Réponse è | Critères |
|---|---|
| Optimal è | IGA 0 (normal) |
| Acceptable è | IGA 1 (presque normale), maladie légère stable |
| Échec è | Pas d’amélioration significative (par ex., baisse de l’IGA de moins de 2 points) |
| Cause | Remarque |
|---|---|
| Déséquilibre psoriasiforme | Mauvaise réponse aux inhibiteurs de type 2 |
| Dermatite de contact allergique | Difficile à détecter, les tests épicutanés sont limités |
| Absence d’observance | Souvent sous-estimée |
| Phobie des aiguilles | Impacts sur l’utilisation biologique Prise en charge : Techniques comportementales à domicile Anesthésiques topiques Soutien pharmacologique Orientation vers un professionnel de la santé mentale |
| Anticorps anti-médicaments | Encore mal étudié dans la DA |
| Infection non diagnostiquée | Peut être démasquée après immunomodulation |
| Immunodéficience primaire | Souvent manquée en l’absence d’un bilan immunitaire complet |
| Hypersensibilité aux excipients | Par ex., polysorbates (présents dans la plupart des produits biologiques) Polysorbate 80 - Dupilumab, tralokinumab Polysorbate 188 - Némolizumab |
| Indice clinique | Éléments à prendre en compte |
|---|---|
| Inflammation persistante | Augmentation des corticoïdes topiques ou ajout d’un corticoïde systémique |
| Refus de l’injection | JAKi par voie orale ou alternatives systémiques |
| Réaction à l’excipient | Changer de classe si possible (pas toujours faisable) |
| Risque lié aux JAKi à long terme | Retour à un traitement biologique lorsque la situation est stable |
| Mauvaise réponse au dupilumab | Transition vers un JAKi (par ex., upadacitinib) |
| Phénotype de la dermatite de contact allergique | Test épicutané, méthotrexate |
| Suspicion d’anticorps anti-médicaments | Passage à une autre classe (par ex., JAKi) |
| Phénotype psoriasiforme | Le blocage des IL-12/23 (par ex., ustékinumab) peut être plus efficace. |
| Problèmes d’adhésion | Schémas posologiques plus simples, options orales |
Références :
Intervenante : Amy S. Paller (États-Unis)
1. Traitements topiques : évolution des options
| Agent | Statut | Tranche d’âge | Remarques |
|---|---|---|---|
| Roflumilast | Émergent | Probablement en expansion | Sensation de picotements/brûlure minimales |
| Ruxolitinib | Approuvé | à partir de 12 ans | Possibilité d’une utilisation future chez de plus jeunes patients |
| Tapinarof | Approuvé | à partir de 2 ans | Faible profil d’irritation |
2. Nouvelles cibles et voies d’accès
3. Innovations en matière d’administration des médicaments
| Méthode | Limites |
|---|---|
| Micro-aiguilles | Impossible à mettre en œuvre pour les volumes élevés de produits biologiques |
| Injecteurs sans aiguille | Limites en termes de volume (par ex., dupilumab = 2 mL) |
| Dispositifs de rétroaction déclenchés par des capteurs | Intervention comportementale possible |
4. Traitements systémiques : présents et futurs
5. Les démangeaisons, une frontière thérapeutique
| Voie | Agent ou cible |
|---|---|
| IL-31 | Némolizumab |
| IL-4/IL-13 | Dupilumab, inhibiteurs de JAK |
| Substance P | Essais infructueux jusqu’à présent |
| Protéases (par ex., protéase V8) | Médicaments antiplaquettaires comme nouveaux traitements topiques |
| Activation de PAR2 | Inhibition de la kallicréine en cours d’étude |
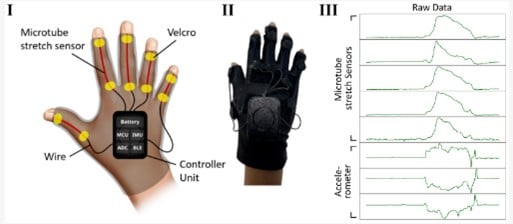
Essais cliniques à distance :
Réalisable par :
Technologie portative :
Permet de suivre :
Exemples :
8. Technologies nouvelle génération :
| Technique | Application |
|---|---|
| Protéomique (5000 protéines) | Analyse de sérum à partir de petits volumes de sang |
| Transcriptomique unicellulaire | Données sur la peau en haute résolution |
| Écouvillonnage du microbiome | Génomique et protéomique |
| Écouvillonnage épidermique à base de détergent | Profilage immunitaire non invasif |
| Zone | Perspective d’avenir |
|---|---|
| Thérapeutique | Davantage de produits topiques non stéroïdiens, de produits biologiques indolores, d’inhibiteurs à petites molécules |
| Surveillance | Capteurs portatifs objectifs, rétroaction en temps réel |
| Accès et équité | Nécessité de réduire les coûts et d’assurer une disponibilité à l’échelle mondiale |
| Essais cliniques | Vers des méthodes à distance et assistées par la technologie |
Références :
Intervenante : Jane Bellet (États-Unis)
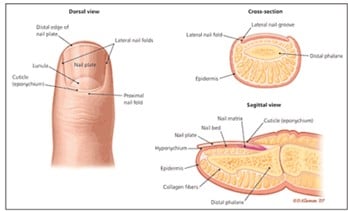
1. Examen de l’anatomie des ongles :
3. Éléments à prendre en compte dans les cas pédiatriques :
4. Planification préopératoire :
5. Techniques d’anesthésie :
6. Options de garrot : champ exsangue
7. Procédures fréquentes :
A. Biopsie à l’emporte-pièce :
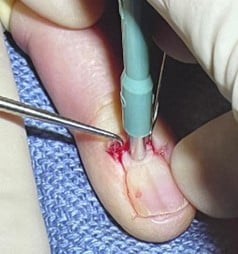
B. Avulsion partielle de l’ongle proximal :
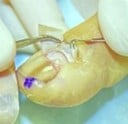
C. Excision par rasage de la matrice unguéale :
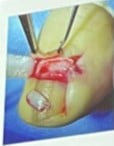
8. Manipulation des échantillons :
9. Retrait du garrot :
« Le moment le plus important de votre journée. »
10. Conseils relatifs au bandage :
11. Soins post-opératoires :
12. Éléments particuliers à prendre en compte dans les cas pédiatriques :
13. Quand ne pas opérer :
Références :
Intervenant : Robert Silverman (États-Unis)
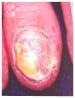
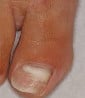
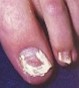
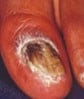
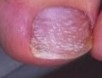
Indices à la dermoscopie :
Topique :
Systémique :
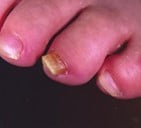
Références :
Intervenante : Judith Dominguez Cherit (Mexique)
La mélanonychie longitudinale (ML) chez les patients pédiatriques constitue un défi diagnostique. Même si elle est bien étudiée chez l’adulte, il existe peu de données disponibles chez l’enfant. Cette affection peut être due à une activation mélanocytaire (d’origine raciale/ethnique ou fonctionnelle) ou à une prolifération (par ex., nævus, mélanome).
| Caractéristique | Adultes | Enfants |
|---|---|---|
| Mélanonychie ethnique | Fréquente, en particulier dans les types de peau foncés | Rare, même dans les types de peau foncés |
| Risque de mélanome | La ML peut être un signe précurseur | Extrêmement rare |
| Critères de diagnostic | Bien établis | Souvent peu fiables lorsqu’il s’agit d’enfants |
| Aspect histologique | Prédictif | Peut imiter un mélanome, même s’il est bénin |
Les colorations BRAFV600E, HMB-45 et PNL2 peuvent permettre de différencier les lésions mélanocytaires bénignes et malignes. Les résultats négatifs pour BRAFV600E sont généralement associés à des nævus bénins.
Références :
Intervenante : Maria Sol Dia (Argentine)
Deux contextes cliniques :
Associations dermatologiques :
Associations systémiques :
Sous-types cliniques
| Sous-type | Descriptif |
|---|---|
| Trachyonychie opaque |
Le plus fréquent et le plus grave. Les ongles paraissent rugueux, minces, avec des stries longitudinales et une perte de brillance. |
| Trachyonychie brillante | Inflammation intermittente avec aspect vitreux, réflexion de la lumière et fines stries. |
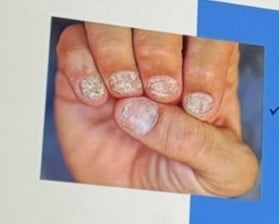
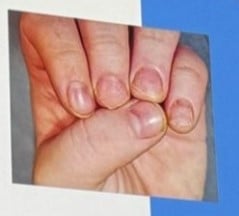
Constatations fréquentes dans les deux types :
Approche clinique
Outils :
Biopsie :
| Approche | Indication |
|---|---|
| Observation | La plupart des cas pédiatriques se résolvent spontanément dans les 6 ans. |
| Traitements topiques | Problèmes esthétiques ou dermatoses associées |
| Corticoïdes intralésionnels | Maladie localisée réfractaire (douloureuse voire pénible) |
| Traitement systémique | Maladie sévère ou associée au psoriasis, à la pelade, etc. |
Agents topiques courants :
Agents systémiques dans les cas graves/associés :
Garçon de 5 ans présentant une rugosité progressive des ongles, précédemment traitée avec divers produits topiques sans amélioration.
Fillette de 4 ans ayant des antécédents de dermatite atopique.
Références :
Intervenante : Lourdes Navarro Campoamor (Espagne)
Importance du diagnostic de l’ongle chez l’enfant
Hypertrophie congénitale des replis latéraux
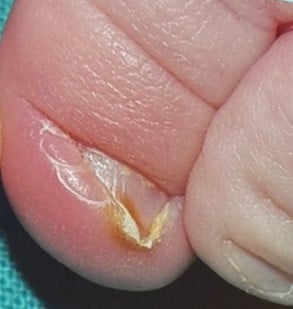
Malformation congénitale des ongles du pied
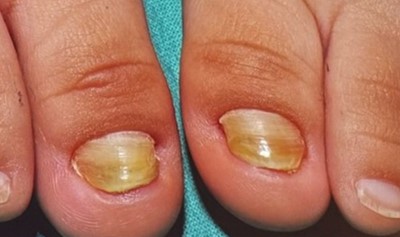
Anonychie congénitale
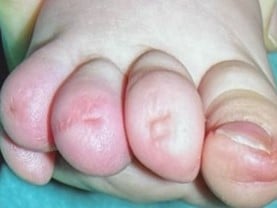
Syndrome d’Iso-Kikuchi
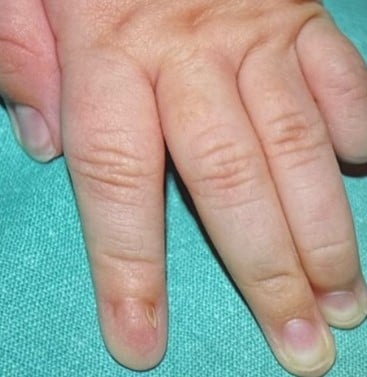
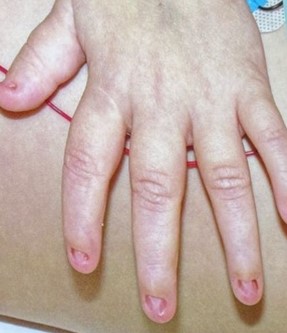
Syndrome Nail-Patella
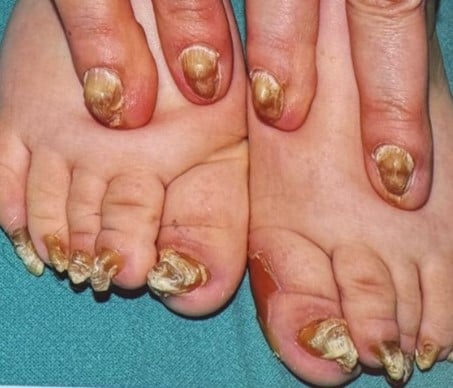
Pachyonychie congénitale
Sclérose tubéreuse complexe
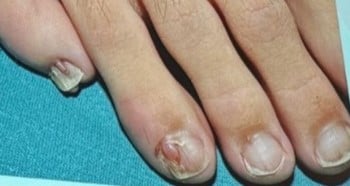
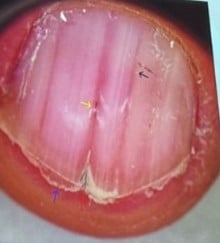
Maladie de Darier
Mélanonychie et fibromes
| Observation | Éventuelles pathologies associées |
|---|---|
| Lunule triangulaire | Syndrome Nail-Patella |
| Micronychie | Syndrome d’Iso-Kikuchi, syndrome Nail-Patella |
| Anonychie/Micronychie des index |
Syndrome d’Iso-Kikuchi |
| Épaississement des ongles des pieds | Pachyonychie congénitale |
| Fibromes périunguéaux | Sclérose tubéreuse complexe |
| Stries longitudinales rouges/blanches, kératose distale cunéiforme sous-unguéal, encoche en forme de V |
Maladie de Darier |
Références :
Intervenante : Kelly Cordoro (États-Unis)
Intervenant : Henry W. Lim (États-Unis)
Les photodermatoses sont des affections cutanées causées ou aggravées par la lumière du soleil.
Catégories :
Gros plan sur :
1. Lucite polymorphe (LP)
Caractéristiques cliniques :
Variantes :
Diagnostic :
Physiopathologie :
Prise en charge :
2. Prurigo actinique
Traitement :
3. Hydroa vacciniforme (HV) et lymphoproliférations de type HV
| Hydroa vacciniforme (HV) classique | Lymphoprolifération de type HV |
|
|---|---|---|
| Fréquence | Rare | Variante sévère |
| Âge d’apparition | Enfance | Enfance ou adolescence |
| Lésions cutanées | Éruptions papulo-vésiculeuses formant des cicatrices vacciniformes en guérissant | Lésions sur les zones exposées et non exposées au soleil |
| Symptômes systémiques | Absents | Œdème facial, fièvre, lymphadénopathie |
| Association avec l’EBV |
Forte | Présente |
| Photosensibilité | Peut présenter une sensibilité aux UVA lors d’un phototest | Non signalé de manière spécifique |
| Pronostic | Variable, le traitement est complexe | Risque d’évolution vers un lymphome |
| Traitement principal | Photoprotection | Prise en charge onco-hématologique |
4. Urticaire solaire
Conseil clinique :
évaluez toujours les patients immédiatement après l’exposition/le test - attendre 24 heures peut faire passer le diagnostic inaperçu.
Traitement :
5. Protoporphyrie érythropoïétique (PPE) et protoporphyrie liée à l’X (PPLX)
Physiopathologie :
Indices cliniques :
Justification : bloque l’accumulation de porphyrine en amont de la voie.
| Affection / Type | Âge typique d’apparition | Morphologie clinique | Diagnostic | Traitement / Prise en charge | Points à retenir |
|---|---|---|---|---|---|
| Lucite polymorphe (LP) | Enfants, adolescents (plus fréquente chez l’adolescent) | Papules, vésicules ; la morphologie varie en fonction du phototype de la peau. | Clinique (en fonction des antécédents et de la morphologie) ; les phototests sont souvent normaux. | Photoprotection, corticostéroïdes topiques, UVB à bande étroite, prednisone orale (en cas de poussées). | Apparition retardée après l’exposition au soleil ; s’améliore avec une exposition progressive au soleil (épaississement cutané) |
| Prurigo actinique | Enfance | Chéilite, conjonctivite, papules lichénifiées sur la peau exposée au soleil | Évaluation clinique | Photoprotection, corticostéroïdes topiques/oraux, thalidomide, UVB, dupilumab (stade expérimental) | Amérique latine ; exposition intense au soleil |
| Hydroa vacciniforme (HV) classique | Enfants | Papules, vésicules, croûtes, cicatrices vacciniformes | Clinique, potentiellement associée à l’EBV |
Photoprotection, soins symptomatiques | Cicatrices permanentes, réaction phototoxique grave |
| Lymphoproliférations de type HV | Enfants et adolescents | Lésions de type HV sur la peau exposée ou non au soleil, œdème facial, fièvre, lymphadénopathie. | Clinique + biopsie + hématologie | Orientation en oncologie, surveillance étroite | Peut évoluer vers un lymphome (environ 10 % des cas), mortalité élevée (environ 40 % des cas), plus grave en Amérique latine |
| Urticaire solaire | Enfants, adolescents, adultes |
Se manifeste sur les zones exposées au soleil ; apparition rapide (quelques minutes) | Évaluation clinique et évaluation post-exposition immédiate | Antihistaminiques, omalizumab, photoprotection | Déclenchée même par la lumière visible ; résolution rapide mais réapparition en cas de nouvelle exposition. |
| Protoporphyrie érythropoïétique (PPE/PPLX) | Petite enfance |
Douleur, brûlure, érythème peu après l’exposition au soleil ; modifications chroniques au niveau des articulations et sur le visage | Taux élevés de protoporphyrine IX ; tests génétiques | Afamélanotide (implant), derzimegalone (oral), inhibiteurs du transporteur de glycine 1 (essais en cours), photoprotection | Avancées thérapeutiques majeures ; amélioration significative de la qualité de vie |
Références :
Intervenante : Jean Bologna (États-Unis)
| Terme utilisé | Remarques |
|---|---|
| Nævus lentigineux tacheté (SLN) | Privilégié par certains cliniciens ; l’accent est mis sur le modèle clinique. |
| Nævus spilus | Plus couramment utilisé dans la littérature (rapport PubMed 2:1) ; signifie littéralement « tache tachée ». |
| Autres termes | On note une terminologie trop abondante ; il est nécessaire de parvenir à une standardisation. |
| Caractéristique | Descriptif |
|---|---|
| Taille | Généralement 3 à 4 cm de diamètre |
| Base | Fond maculeux couleur café au lait |
| Superposition | Lentigines, nævi jonctionnels, nævi composites |
| Évolution | De plus en plus de « points » apparaissent avec l’âge ; ils peuvent être discrets au moment de la naissance. |
| Schémas de répartition | Peut suivre les lignes de Blaschko ou des motifs en forme de blocs, pas toujours en damier. |
| Syndrome/entité | Association avec le SLN |
|---|---|
| PPK (phacomatose pigmento-kératosique) | SLN papuleux |
| PPV (phacomatose pigmento-vasculaire) | SLN maculeux |
| Mélanocytose neurocutanée | Peut survenir chez les patients présentant un NMC de taille moyenne apparaissant dans un SLN. |
| Rhabdomyosarcome | Signalé chez un patient présentant des nævi de Spitz dans le SLN (rare). |
| Syndrome de Noonan (RASopathies) | Mentionné comme ayant des caractéristiques qui se chevauchent |
| Argument | Preuves |
|---|---|
| Lésion congénitale | Les lésions suivent les schémas embryologiques (par ex., les lignes de Blaschko), ce que confirment les présentations hybrides. Les preuves confirment l’origine congénitale. |
| « Acquisition » apparente | La base hypopigmentée peut être discrète à la naissance, les taches apparaissant plus tard, ce qui conduit à une classification erronée. |
Références :
Intervenante : Aniza Giacaman Contreras (Espagne)
| Structure | Descriptif |
|---|---|
| Points | Petites zones de pigmentation ponctuelles. |
| Globules | Plus grands que les points, leur forme peut varier. Ils correspondent à des nids mélanocytaires. |
| Lignes | Peut former des motifs dermoscopiques distincts tels que des réseaux ou des branches. |
| Réseau pigmenté | Reflète la mélanine présente dans les kératinocytes à la jonction dermo-épidermique. |
| Aspect en pavés | Globules regroupés en mosaïque, fréquemment observés dans le NMC. |
| Structures cibles | Globules à l’intérieur d’un réseau avec des points centraux ; peut suggérer une apoptose des mélanocytes. |
| Points bleus/gris | Indique une apoptose des mélanocytes ou une atteinte du derme. |
| Vaisseaux | La présence peut varier en fonction de l’évolution de la lésion ; peut inclure des vaisseaux grossiers. |
| Hypertrichose | Souvent associée à des nævi congénitaux, elle augmente avec l’âge. |
| Localisation | Modèles fréquents |
|---|---|
| Tête | Modèle homogène |
| Tronc | Modèle globulaire prédominant |
| Extrémités | Réticulaire ou mixte globulaire-réticulaire |
| Paumes des mains/plantes des pieds | Sillons ou crêtes parallèles, aspect de « pois dans une cosse ». |
Modèle globulaire classique
Réseau mixte et globules
Changements dans le temps
Zones acrales (paumes des mains, plantes des pieds)
Atteinte de la matrice de l’ongle
| Scénario | Évolution clinique |
|---|---|
| Nodules stables au fil des ans | Souvent bénins en l’absence de caractéristiques dermoscopiques suspectes. |
| Globules en forme de pavés sans atypie | En faveur d’une évolution bénigne ; une surveillance continue est recommandée. |
| Nodules de couleur bleue | Peut susciter des inquiétudes ; l’histologie peut malgré tout être bénigne. |
| Prolifération rapide des nodules en peu de temps | Une biopsie est nécessaire pour écarter la possibilité d’une tumeur maligne (par ex., tumeur de Spitz atypique). |
Références :
Intervenante : Julia Schaeffer (États-Unis)
| Terme | Définition |
|---|---|
| Nævus mélanocytaire congénital (NMC) | Présent à la naissance ou au cours des premières semaines de vie |
| Classification basée sur la taille | Sur la base de la taille adulte prévue : petit (moins de 1,5 cm), moyen (1,5 à 20 cm), grand (plus de 20 cm), géant (plus de 40 cm) |
| NMC ciblé / nævus de type congénital | Lésions apparaissant au cours des 2 à 3 premières années ; similaires aux véritables nævi congénitaux sur les plans histologique et moléculaire. |
Modèles dermoscopiques fréquents par localisation
| Cuir chevelu |
|
| Tronc |
|
| Régions acrales |
|
| Ongles |
|
| Caractéristique | Interprétation |
|---|---|
| Modèle globulaire | Typique du NMC, caractéristique bénigne |
| Globules réticulaires/bleus-gris | Observés dans les cas de prolifération mélanocytaire plus profonde ; pas toujours inquiétant. |
| Globules cibles | Globules au sein d’un réseau, associés à l’activité mélanocytaire |
| Modèle fibrillaire en brosse (ongles) | Fréquent chez l’enfant, bénin |
| Caractéristiques vasculaires | Peuvent apparaître au fil du temps ; pas toujours évocateurs de la présence d’un mélanome. |
| Estimation du risque | Preuves |
|---|---|
| moins de 0,5 à 1 % de risque au cours de la vie | Revues systématiques et données de cohortes (par ex., risque sur 15 ans : environ 0,007 %) |
| Apparition du mélanome | Généralement après la puberté, rare dans la petite enfance. |
Surveillance clinique
Indications pour l’excision
| Indication | Raison |
|---|---|
| Cosmétique/psychosociale | Indication la plus fréquente de nos jours, en particulier pour les lésions du visage |
| Préoccupations fonctionnelles | Lésions situées à proximité des articulations, des paupières, etc. |
| Changements évocateurs d’une tumeur maligne | Modifications focales de la couleur, de la texture ou de la vascularisation |
| Anxiété des parents | Lorsque l’impact psychologique est important et persistant |
Techniques d’excision
Thérapie au laser
Traitements topiques
Moment de l’excision :
| Type de lésion | Remarque concernant la prise en charge |
|---|---|
| Nævi de Sutton | Bénin |
| Composants nodulaires | Nécessité d’une anamnèse et d’une surveillance approfondies |
| Lésions du cuir chevelu | Tend à s’estomper |
| Lésions acrales/unguéales | Identifier les formes dermoscopiques bénignes |
- Aucune intervention n’est nécessaire en l’absence de caractéristiques atypiques.
- Éviter les biopsies prématurées.
- Biopsie uniquement en cas d’inquiétude.
Références :
Intervenante : Fatima Giusti (Argentine)
L’oratrice a évoqué son expérience de la dermoscopie numérique en dermatologie pédiatrique, en insistant sur la nécessité de bien définir les indications cliniques. La présentation s’appuyait sur une étude rétrospective menée dans un hôpital tertiaire spécialisé en dermoscopie numérique et en soins pédiatriques.
Données démographiques et type de peau
Suivi et utilisation
Facteurs de risque et syndromes cliniques
On notera que la prévalence du syndrome du grain de beauté atypique était significativement plus élevée que dans les cohortes pédiatriques publiées, ce qui suggère le bénéfice potentiel d’un suivi numérique structuré.
Modèles dermoscopiques
Indications pour la dermoscopie numérique
Excision et histopathologie
Les résultats confirment le rôle de la dermoscopie numérique pour éviter les interventions chirurgicales inutiles tout en identifiant les lésions cliniquement significatives.
Nombre de nævi
Maladies génétiques
Références :
Intervenante : Elena Hawryluk (États-Unis)
| Catégorie de taille | Risque de mélanome au cours de la vie |
|---|---|
| NMC petit/moyen | moins de 1 % Risque surtout après la puberté |
| NMC de grande taille | 2 % environ |
| NMC géant avec satellites | 6 à 15 % Groupe à haut risque |
Définition et risques :
Stratégie en termes d’imagerie :
| Critères (variables selon les lignes directrices) |
|---|
| NMC de plus de 3 cm ou 25 NMC et plus |
| Plus de 1 NMC indépendamment de la taille |
| NMC géant, NMC multiples de taille moyenne |
| 4 NMC ou plus, associés à des résultats anormaux au niveau du SNC (cohorte générale) |
Les lignes directrices relatives au dépistage par IRM ne sont pas standardisées et dépendent des ressources disponibles dans les différentes régions. Il est essentiel de procéder à une prise de décision partagée avec les parents.
Références :
Intervenante : Veronica Kinsler (Royaume-Uni)
Cette présentation a fourni un examen approfondi des mécanismes génétiques qui sous-tendent les nævi mélanocytaires congénitaux (NMC), en se concentrant sur les mutations en mosaïque, en particulier les gènes NRAS, BRAF et les gènes de fusion BRAF, ainsi que sur leur signification clinique. L’exposé a également exploré le rôle émergent de la thérapie ciblée, en particulier des inhibiteurs de MEK, dans le traitement des patients présentant des NMC à phénotypes problématiques.
| Gène | Prévalence | Type de mutation | Caractéristiques cliniques |
|---|---|---|---|
| NRAS | Le plus fréquent | Mutations faux-sens |
Présente dans la peau, le SNC et les tumeurs ; constante dans tous les tissus |
| BRAF | Moins fréquente | Mutations faux-sens | Souvent associée à de nombreux nodules dermiques mous |
| Fusions BRAF | Sous-groupe nouvellement reconnu | Fusion de gènes (partenaires variés) | Souvent associée à un NMC multinodulaire résistant au traitement |
| Principales caractéristiques |
|---|
|
Références :
Intervenant : Marius Rademaker (Nouvelle-Zélande)
| Rosacée | Dermatite périorale (DP) | |
|---|---|---|
| Présentation fréquente | Érythème facial, rougissement, papules/pustules | Papules autour de la bouche, du nez et des yeux |
| Rougissement | Quasi universel | Généralement absent |
| Atteinte oculaire | Fréquente (blépharite, conjonctivite) |
Pas typique |
| Comédons | Absents | |
| Démodécie | Possible | |
| Description des symptômes | Brûlures ou picotements | Démangeaisons douloureuses |
| Aggravé par les corticostéroïdes topiques | Oui | |
Principes généraux
Traitements topiques
Traitements systémiques
Antibiotiques : à utiliser avec précaution
Isotrétinoïne (hors AMM)
Ivermectine orale
Récapitulatif :
Références :
Intervenante : Irene Lara Corrales (Canada)
1. Induites par les corticoïdes
2. Induites par les thérapies ciblées (par ex., inhibiteurs de l’EGFR et de MEK)
3. Induites par les inhibiteurs de JAK (JAK-ny)
1. Folliculite à pityrosporum (Malassezia)
2. Folliculite à Gram négatif (bain chaud)
| Caractéristique | Acné | Éruption acnéiforme |
|---|---|---|
| Comédons | Présents | Absents |
| Apparition | Progressive | Soudaine, en quelques jours ou semaines |
| Distribution | Variable | Symétrique, folliculocentrique |
| Déclencheurs | Endogènes | Exposition médicamenteuse ou infectieuse |
Références :
Intervenante : Maria Lertora (Argentine)
1. Pathogénie traditionnelle de l’acné élargie
2. Diversité du microbiome dans la peau saine par rapport à la peau acnéique
3. Interactions microbiennes
4. Influences externes sur le microbiome
Souches probiotiques fréquemment étudiées :
1. Probiotiques oraux
2. Soins topiques respectueux des biomes
3. Prise en charge personnalisée de l’acné
Références :
Intervenante : Agnes Schwieger (Suisse)
Contexte hormonal : l’acné est souvent une manifestation externe de changements hormonaux, principalement associés à deux voies de développement :
Parmi ceux-ci, les androgènes surrénaliens, et plus particulièrement l’activation de l’axe HPA, joueraient un rôle plus important dans l’apparition précoce de l’acné. Cette activation, connue sous le nom d’adrénarche, commence vers l’âge de six ans. Il entraîne une augmentation de la production de DHEAS, un androgène faible qui peut être converti en formes plus puissantes, favorisant la prolifération des glandes sébacées et la production de sébum. Cette activité hormonale favorise l’acné, les odeurs corporelles et le développement des poils pubiens.
Orientation clinique : l’exposé était axé sur l’acné infantile (à partir de l’âge de 8 semaines) et l’acné de la moyenne enfance (entre 1 et 7 ans), en soulignant que l’acné néonatale est rare et souvent mal diagnostiquée (communément confondue avec la pustulose céphalique néonatale).
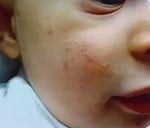
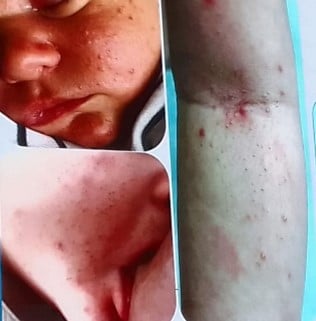
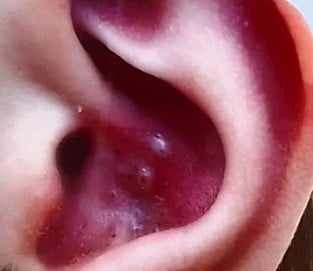
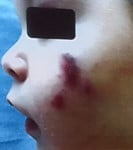
Perles cliniques :
| Comédons - Papules | Acide azélaïque, rétinoïdes topiques + BP |
| Pustules | + ATB topique/ ATB oral (érythromycine) |
| Nodules - Pseudokystes | ATB oral, rétinoïde oral (0,3 à 0,5 mg/kg/jour) +/- stéroïde |
L’acné infantile, en particulier dans la petite et la moyenne enfance, justifie une évaluation approfondie. Bien que la plupart des cas soient bénins et d’origine hormonale, il est important d’exclure les troubles systémiques ou endocriniens. Avec une prise en charge appropriée, comprenant des traitements topiques et systémiques si nécessaire, ces enfants peuvent obtenir d’excellents résultats sans conséquences à long terme.
Références :
Intervenante : Karen Chernoff (États-Unis)
Chez la femme, l’acné peut être une affection dermatologique isolée ou un marqueur clinique potentiel d’hyperandrogénie, c’est-à-dire une présence excessive d’androgènes de sources ovariennes, surrénaliennes ou périphériques. Les dermatologues jouent un rôle clé dans l’identification des signes cliniques de déséquilibres hormonaux et la mise en place d’évaluations ou d’orientations appropriées.
L’hyperandrogénie résulte d’une augmentation de la production d’androgènes ou de leur conversion périphérique. L’hypophyse stimule les ovaires et les glandes surrénales, entraînant ainsi la production de testostérone, qui est convertie en dihydrotestostérone (DHT) par la 5-alpha-réductase, ce qui donne lieu à des manifestations cliniques telles que l’acné.
Tests de dépistage de base
Testostérone totale et libre (si disponible par LC-MS/MS)
Autres analyses en laboratoire :
Résumé des points à retenir
Références :
Intervenante : Andrea Zaenglein (États-Unis)
1. Le peroxyde de benzoyle dans le traitement de l’acné
2. Isotrétinoïne et troubles sexuels
Références :
Intervenante : Pearl Kwong (États-Unis)
Exemples d’utilisation positive :
| Cas/Tendance | Descriptif |
|---|---|
| Complication liée à un soin exfoliant du pied | Un adolescent âgé de 15 ans a utilisé un masque pour les pieds à la mode après une blessure → il a développé un écoulement douloureux de pus « bleu ». |
| Produit de comblement fait maison | Tentative d’auto-injection à partir d’un tutoriel en ligne. |
| Mauvaise utilisation de l’huile d’arbre à thé | Utilisation chez les garçons prépubères → gynécomastie. |
| Mauvais usage des corticoïdes topiques | Une femme enceinte a appliqué du clobétasol pour traiter son acné, ce qui a aggravé son état. |
| Utilisation abusive du portail | Les patients envoient des photos via un portail de DME en espérant un diagnostic à distance (par ex., absence de squames ou de gonflement visible, mais catégorisé comme tel par le patient). |
| Un coach de vie plutôt que des soins médicaux | Retard dans le traitement d’un hémangiome ulcéré et infecté car les parents ont fait appel à un coach de vie non qualifié. |
| Échec du traitement de l’acné | Un patient de longue date a cherché des traitements en ligne contre l’acné, qui ont aggravé la maladie avant qu’il retourne consulter. |
| Remède maison contre le molluscum | L’application d’un remède topique inconnu a provoqué une hyperpigmentation extrême et des lésions cutanées. |
| Tendance de la mucine d’escargot | Produit populaire chez les adolescents malgré l’absence de preuves solides. |
Intervenante : Veronica Kinsler (Royaume-Uni)
Exemple d’étude - Malformations artérioveineuses (MAV) :
Conclusions :
Stratégie ARNsi :
Références :
Intervenant : Pierre Vabres (France)
La présentation portait sur un groupe nouvellement défini de troubles en mosaïque caractérisés non seulement par des caractéristiques cliniques mais aussi par leurs causes moléculaires sous-jacentes. Ces troubles, précédemment décrits à l’aide de divers termes cliniques (par ex., hypomélanose de Ito, mosaïcisme pigmentaire), sont de plus en plus souvent classés en fonction des altérations génétiques et de l’implication des voies de signalisation.
1. Hypomélanose de Ito liée à mTOR
| Gène | Syndrome/Phénotype | Caractéristiques |
|---|---|---|
| AKT3 | Syndrome MPPH | Hémimégalencéphalie, PMG |
| PTEN | Syndrome de Cowden/des hamartomes | Macrocéphalie |
| PIK3CA | Syndrome MCAP | Malformations capillaires, croissance excessive |
| PIK3R2 | Syndrome MPPH | Anomalies de la substance blanche |
2. Syndrome en mosaïque lié à RhoA
3. Syndrome en mosaïque lié à GNA13
Conclusion : De nouvelles variantes somatiques dans mTOR, RhoA et GNA13 soulignent l’importance du séquençage de l’exome dans les tissus cutanés et contribuent à reclasser ces troubles dans des entités génétiquement définies.
Références :
Intervenant : Gianluca Tadini (Italie)
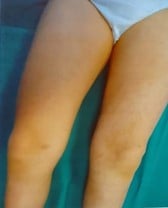
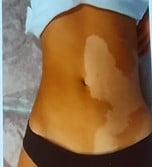
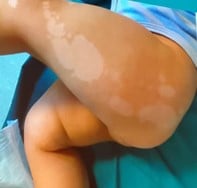
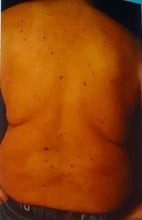
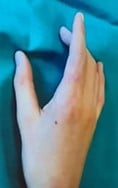
Références :
Intervenante : Nicole Knoepfel (Suisse)
Méthodologie :
| Gène | Nombre de patients | Remarques cliniques | Charge allélique | Sang |
|---|---|---|---|---|
| GNAS | 3 | Un cas a développé une hyperthyroïdie à l’âge de 12 ans. | Très faible | Négatif |
| NRAS | 2 | Enfants à la peau claire avec une pigmentation discrète, un présentant des nævi. | Faible | Négatif |
| PTPN11 | 1 | Pigmentation inégale, aucun nævus, teint rosé. | S/O | Négatif |
| BRAF | 1 | Pigmentation segmentaire avec présence de nævi. | S/O | Négatif |
| Mosaïcisme chromosomique | 1 | Épilepsie due à une carence en carnitine, gain de 5q dans la peau. | S/O | Négatif |
Intervenante : Aniza Giacaman Contreras (Espagne)
| Lésion | Caractéristiques | Remarques cliniques |
|---|---|---|
| Macules hypomélanotiques | Ovale, feuille de frêne, polygonal, confetti | Souvent le premier signe ; à distingue du vitiligo, du nævus anémique/achromique. |
| Poliose | Zone de cheveux blancs | Rare mais diagnostiqué |
| Angiofibromes faciaux | Papules rose-rouge sur le centre du visage, épargnant la lèvre supérieure. | Peut ressembler à l’acné ou à la rosacée ; la dermoscopie peut montrer des queues de Demodex dans le cas de la rosacée. |
| Plaque fibro-céphalique | Plaques jaunâtres à brunes au niveau du cuir chevelu ou du front. | Peut être congénital ou survenir dans la petite enfance. |
| Fibromes de la cavité buccale et des puits dentaires | Papules au niveau des gencives et piqûres de l’émail | Orientation vers un service dentaire obligatoire |
| Fibromes péri-/sous-unguéaux | Papules de couleur chair ou rose ; formation de sillons sur les ongles. | Plus fréquent au niveau des pieds ; peut également apparaître après un traumatisme chez des personnes en bonne santé. |
| Écusson de galuchat | Hamartome du tissu conjonctif avec texture en « peau d’orange ». | Généralement dans la région lombo-sacrée. |
| PRÉSENTATION PEU COURANTE DU CST | ||
| Lésions osseuses sclérotiques | Détection radiologique | Différentiel important : métastases ostéoblastiques |
|
Comètes rouges
|
Vaisseaux péri-unguéaux en forme de tire-bouchon avec halo blanchâtre. | Observées chez les femmes adultes atteintes de CST |
| Nævus épidermique blanc (NEB) | Papules blanches hyperkératosiques en début de vie. | Peut précéder les macules hypomélanotiques ; marqueur précoce potentiel du CST. |
| Hamartome folliculo-sébacé kystique et hamartome du collagène |
Tumeur congénitale du cuir chevelu ; ouvertures de type comédons avec des cheveux touffus | Histologie : kystes folliculaires, faisceaux de collagène et follicules rompus. |
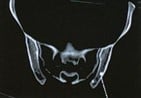
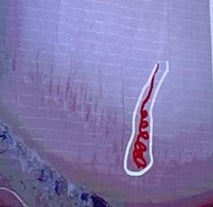
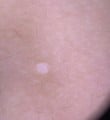
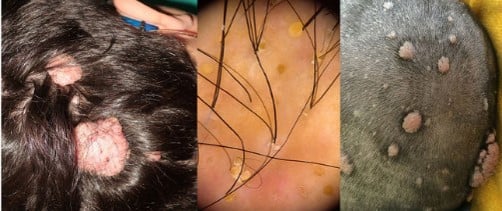
Le CST présente un large spectre phénotypique, et si de nombreux signes sont cutanés, plusieurs sont discrets ou méconnus. Une détection précoce, un examen approfondi et des soins pluridisciplinaires sont essentiels pour une prise en charge efficace.
Références :
Intervenante : Maria Rosa Cordisco (États-Unis)
1. Les malformations capillaires (MC)
Syndromes associés aux malformations capillaires
| Syndrome | Principales caractéristiques | Résultats de l’imagerie | Éléments à prendre en compte en matière de traitement |
|---|---|---|---|
| Syndrome MCAP | Malformation capillaire au niveau de la lèvre supérieure/ du philtrum, mégalencéphalie, anomalies digitales | Polymicrogyrie, anomalies du corps calleux, malformation de Chiari I | Orientation précoce vers un service neurologique, consultation génétique |
| Syndrome de Sturge-Weber (SWS) | MC faciale (bilatérale en forme de V), angiomatose leptoméningée, atteinte oculaire (glaucome) | IRM avec contraste, examens oculaires, imagerie de suivi pour les crises d’épilepsie | IRM précoce (à répéter si négatif à moins de 8 semaines), suivi ophtalmologique |
| Mutation GNA11 | MC étendue et réticulée, atteinte du SNC, moins agressive que le SWS | IRM cérébrale, atteinte neurologique moins sévère | Traitement des crises d’épilepsie, surveillance du glaucome |
Prise en charge du syndrome de Sturge-Weber
Malformations capillaires multifocales
2. Malformations artérioveineuses (MAV)
| Principales caractéristiques | Occurrence | Traitement |
|---|---|---|
| MAV dans le SNC | 90 % dans le SNC | Chirurgie, embolisation |
| CAMS (syndrome métamérique artérioveineux cérébro-facial) | Distribution unilatérale, métamérique | Embolisation neurochirurgicale |
3. Hémangiomes avec atteinte du SNC
| Type | Risque pour le SNC | Principales associations |
|---|---|---|
| Hémangiomes multifocaux | Lésions rares du SNC (peuvent être asymptomatiques) | Dépistage d’une atteinte viscérale |
| Hémangiomes segmentaires | Risque de syndrome PHACE | Nécessite une imagerie du SNC |
Syndrome PHACE
Imagerie : IRM tête/cou/poitrine, échocardiographie.
Surveillance : IRM précoce pour le risque d’AVC, imagerie moins fréquente après la première année.
Références :
Intervenante : Maria Teresa Garcia Romero (Mexique)
| Type de motif | Descriptif | Manifestations associées |
|---|---|---|
| Lignes de Blaschko | Lignes étroites ou larges suivant une distribution linéaire | Présent dans le mosaïcisme mélanocytaire et non mélanocytaire |
| Modèles en blocs | Taches bien définies et localisées | Associé à des troubles neurocutanés et à une atteinte systémique |
| Latéralisation | Atteinte unilatérale, souvent localisée | La mosaïque peut se manifester d’un seul côté du corps. |
| Motifs en écharpe | Rayures diagonales sur le corps | Typiquement associé à un mosaïcisme segmentaire |
| Taches étendues | Zones plus étendues et bien circonscrites | Observé dans des affections telles que l’hypomélanose de Ito |
Références :
Intervenante : Camila Downey (Chili)
Lien embryologique et pathogène :
Types et sévérité des RASopathies :
| Type de RASopathie | Degré d’atteinte des cellules | Exemples | Remarques |
|---|---|---|---|
| Lignée germinale (toutes les cellules atteintes) | Systémique | Syndrome de Noonan, NF1 | Une dysrégulation légère/modérée est nécessaire pour permettre la survie. |
| Mosaïque (propre au tissu) | Un/plusieurs tissus | Syndrome de Schimmelpenning | La sévérité dépend du moment de la mutation et des cellules touchées. |
Mutations génétiques et lésions dermatologiques :
| Mutation | Lésions associées | |
|---|---|---|
| K-RAS | Nævus sébacé, malformations capillaires, MAV | |
| H-RAS | Nævi épidermiques kératinocytaires, nævi de Spitz | |
| N-RAS | Nævi mélanocytaires congénitaux | |
| B-RAF | Nævi de Spitz, nævi mélanocytaires congénitaux | |
Syndromes cliniques (« véritables RASopathies ») à présentation en mosaïque :
Observations dermatologiques et extra-cutanées spécifiques :
| Syndrome | Mutation | Principales caractéristiques |
|---|---|---|
| Schimmelpenning (syndrome du nævus sébacé linéaire) | K-RAS | Nævus sébacé linéaire, colobome, DAP, malformations cérébrales |
| Syndrome du nævus épidermique kératinocytaire | Nævi kératinocytaires généralisés, malformation lymphatique, anomalies cardiaques | |
| Syndrome oculo-ectodermique | Aplasie cuticulaire, excroissances au niveau des paupières, dermoïdes, retard de développement neurologique, anomalies cardiaques | |
| Lipomatose encéphalo-crânio-cutanée | Alopécie, excroissances orbitales, lipomes du SNC, crises d’épilepsie, anomalies oculaires | |
| Phacomatose pigmento-kératosique | H-RAS | Nævi sébacés et mélanocytaires, scoliose, rhabdomyosarcome, épilepsie |
| Syndrome d’hypophosphatémie cutanée et squelettique | Nævi épidermiques, rachitisme, déminéralisation osseuse, atteinte des yeux/du SNC |
Corrélations entre génotype et phénotype :
Recommandations pour le bilan clinique :
Évaluer l’atteinte systémique lorsque :
Évaluations suggérées :
Aperçu de la recherche :
Points à retenir :
Références :
Intervenante : Irene Lara Corrales (Canada)
1. Nævus mélanocytaire congénital (NMC)
2. Sclérose tubéreuse complexe (STC)
3. Neurofibromatose de Type 1 (NF1)
| Trouble | Voie génétique | Thérapie ciblée | Résultats/Remarques |
|---|---|---|---|
| NMC (fusion NRAS/BRAF) | MAPK | Tramétinib | Diminution du volume de la lésion, du prurit, de l’érythème |
| NMC (lié à PIK3CA) | PI3K-AKT-mTOR | Inhibiteurs de PIK3CA | Baisse de densité des mélanocytes (données préliminaires) |
| Sclérose tubéreuse | mTOR | Évérolimus / Sirolimus | Diminution du nombre de tumeurs rénales ; réponse variable de l’angiofibrome |
| EGFR | Afatinib + évérolimus | Diminution des SEGA et des lésions corticales (préclinique) | |
| – | Sirolimus prénatal | Diminution des rhabdomyomes fœtaux (rapports de cas) | |
| Neurofibromatose de type 1 | RAS-MAPK | Sélumétinib | Moins de plexiformes inopérables, amélioration de la qualité de vie |
| Tramétinib (gliomes) | Approuvé par la FDA dans les tumeurs cérébrales |
Références :
Intervenante : Maria Agustina Acosta (Uruguay)
Rôle général et indications
Modalités de la photothérapie
| Modalité | Commentaires |
|---|---|
| UVB à bande étroite (NB-UVB) | Le plus souvent utilisé chez l’enfant |
| PUVA (Psoralène + UVA) | Rare en pédiatrie en raison de problèmes de sécurité |
| Photothérapie ciblée | Utilisé pour les lésions localisées |
| UVB à domicile | Alternative émergente nécessitant une supervision étroite |
Éléments particuliers à prendre en compte dans les cas pédiatriques
Photothérapie à domicile
La photothérapie par rapport aux produits biologiques
Références :
Intervenant : Matias Maskin (Argentine)
La photothérapie est désormais généralement utilisée comme traitement de deuxième intention ou en association avec des produits biologiques dans les cas graves.
La photothérapie est recommandée dans les cas modérés mais les traitements biologiques systémiques sont préférables dans les cas de dermatite atopique sévère.
La photothérapie reste une option viable dans les cas au stade précoce.
Le rôle de la photothérapie en dermatologie pédiatrique est en constante évolution. Si elle reste une option thérapeutique essentielle dans les affections légères à modérées, les nouveaux traitements biologiques s’imposent de plus en plus dans les affections plus graves. À l’avenir, la photothérapie sera probablement davantage intégrée dans les thérapies combinées, ce qui en fera un outil précieux et non plus un traitement de première intention dans la plupart des cas.
Références :
Intervenant : Henry W. Lim (États-Unis)
Composition et effets de la lumière du soleil
| Peaux foncées : |
Peaux claires
|
| Mélanosomes plus nombreux et plus grands, dispersés de manière individuelle | Mélanosomes plus petits, regroupés dans les kératinocytes |
| FPS intrinsèque ~13 | FPS intrinsèque ~3 |
Influence familiale et culturelle
Corrélations cliniques
Conseils en fonction de l’âge
Défis pratiques
Recommandations en fonction de la couleur de peau
| Type de peau | FPS recommandé | Protection anti-UVA | Protection contre la lumière visible |
|---|---|---|---|
| Type I-III (clair) | FPS 50 et plus | Modérée | Pas essentielle |
| Type IV-VI (foncé) | FPS 30 et plus | Plus élevée de préférence | Importante (risque de pigmentation) |
Crème solaire sur les zones exposées (FPS et spectre adaptés au type
de peau) +
Références :
Intervenant : Antonio Torrelo (Espagne)
Vue d’ensemble : La photothérapie est un outil précieux en dermatologie, y compris dans les cas pédiatriques, bien que les protocoles soient souvent centrés sur les adultes. Son application chez l’enfant doit être individualisée, en particulier dans les cas rares ou graves. Ce qui suit résume les connaissances actuelles sur les photodermatoses telles que la lucite polymorphe (LP) et le prurigo actinique (PA), ainsi que les nouveautés récentes en matière de traitement.
Antioxydants systémiques : sans danger pour les enfants (p. ex. bêta-carotène), moins standardisés chez l’enfant.
| Affection | Présentation chez l’enfant | Traitement de première intention | Option émergente/Alternative | Remarques |
|---|---|---|---|---|
| Lucite polymorphe (LP) | Rare, bénigne ; éruption printanière juvénile | Protection anti-UVA, antioxydants | Omalizumab (adultes), tacrolimus topique |
Désensibilisation rarement utilisée chez l’enfant de moins de 7 ans |
| Le prurigo actinique (PA) | Fréquent en Amérique latine, rare en Europe | Corticoïdes (faible réponse), évitement | Talidomide, inhibiteurs de JAK, nicotinamide | Associé à des types HLA spécifiques |
| Photodermatoses (réfractaires) | Sévère, résistant au traitement topique | Photoprotection, antioxydants | Inhibiteurs de JAK, nicotinamide | Nécessite une approche individualisée |
Références :
Intervenant : Fernando M. Stengel (Argentine)
Sources de pollution
Récifs coralliens et filtres UV
Données géographiques
| Composé | Catégorie | Préoccupation environnementale | Sécurité des personnes | Commentaire |
|---|---|---|---|---|
| Oxybenzone (BP-3) | Organique | Blanchiment des coraux, perturbateur endocrinien chez les poissons | Perturbateur endocrinien potentiel | Interdit dans plusieurs régions |
| Octinoxate | Toxicité des coraux, pollution marine | Absorption modérée, données hormonales | Interdit dans les zones coralliennes sensibles |
|
| Octocrylène | Toxicité marine, bioaccumulation | Susceptible de s’accumuler dans les tissus | Encore largement utilisé dans de nombreux pays | |
| Dioxyde de titane |
Inorganique (minéral) |
Précipite dans l’eau de mer, faible interaction avec les coraux | Non absorbé par voie cutanée | Considéré comme sûr, utilisé chez l’enfant |
| Oxyde de zinc | Similaire au TiO₂ - précipite, faible impact sur le corail | Non absorbé par voie cutanée | Recommandé pour un usage pédiatrique | |
| Nouveaux agents biologiques | Hybride organique | Données limitées | En cours d’investigation | Des formulations plus sûres en cours de développement |
Références :
Compte rendu rédigé par le Dr Paola Stefano (dermato-pédiatre, Argentine)
Intervenants : Dr Juan Carlos Lopez Gutierrez (Espagne), Dr Eulalia Baselga (Espagne), Dr Isabel Colmenero (Espagne), Dr María Rosa Cordisco (États-Unis)
Lors de cette session, le Dr Maria Rosa Cordisco a d’abord annoncé la publication, en espagnol, du livre « Anomalías vasculares en la infancia » (« Les anomalies vasculaires chez l’enfant »), auquel ont participé des spécialistes internationaux de la génétique, de la radiologie, de la dermatologie, de la pharmacologie et d’autres disciplines. L’intervenante a souligné l’importance du travail en équipes pluridisciplinaires pour le diagnostic, le traitement et le suivi de ces anomalies. Grâce aux progrès de la génétique ces dernières années, il a été possible de classer et de diagnostiquer les différentes anomalies et de mettre en place des thérapies ciblées face à ces cas complexes. Le Dr Natalia Torres a souligné que cet ouvrage est à jour des dernières avancées diagnostiques et thérapeutiques, ainsi que de la dernière classification ISSVA de 2025.
Le Dr Teplinsky est radio-pédiatre et coordonne le groupe consacré aux anomalies vasculaires à l’hôpital pédiatrique JP Garrahan et au centre des anomalies vasculaires au sein du sanatorium Mater Dei. Il a quant à lui annoncé la création d'une société ibéro-américaine dédiée aux anomalies vasculaires (SIAV, Sociedad Iberoamericana de Anomalías Vasculares). Cette société a été créée en septembre 2024, est établie en Espagne et regroupe les pays hispanophones. Elle a pour mission de promouvoir les connaissances en matière de diagnostic et de traitement des anomalies vasculaires et de favoriser la collaboration entre les différentes spécialités et les différents pays d’Amérique latine, ce qui contribuera à l’amélioration de la qualité de vie des patients. Un autre objectif de cette société est de travailler ensemble dans la même langue, afin de donner une nomenclature correcte aux anomalies vasculaires, tout en établissant des directives pour le diagnostic et le traitement et en organisant des réunions pour discuter des cas. L’intervenant a également insisté sur le fait que cette nouvelle société possède des liens avec ses sociétés mères : la SEAV (Société espagnole dédiée aux anomalies vasculaires) et l’ISSVA (Société internationale pour l'étude des anomalies vasculaires).
Intervenante : Dr Natalia Torres (Argentine)
Dermato-pédiatre. Hôpital Dr J P Garrahan Coordinateur du groupe interdisciplinaire consacré aux anomalies vasculaires - Hôpital Dr J P Garrahan - Argentine
Les intervenants ont présenté le cas d’une jeune fille de 12 ans, qui avait consulté pour des céphalées, des douleurs et une perte de fonction au niveau du bras. La patiente présentait également une macrocéphalie et des troubles cognitives. À l’examen dermatologique, elle présentait une lésion érythémato-télangiectasique d’aspect vasculaire accompagnée de trajets veineux sur l’avant-bras depuis ses premières années de vie, lésion qui a évolué avec la croissance de l’enfant. Une autre lésion était observée dans la région thoracique. La patiente avait subi deux embolisations et souhaitait obtenir un second avis.
L’échographie a montré une hypertrophie des tissus mous, ainsi que des vaisseaux dilatés au débit élevé. L’angiographie par résonance magnétique a également montré de multiples shunts artério-veineux dépendant des artères subclavière, axillaire et brachiale.
Parallèlement, la patiente présentait un dysfonctionnement ventriculaire gauche secondaire à son anomalie vasculaire, qui générait une surcharge volémique. C’est pourquoi elle a été traitée par énalapril et une nouvelle embolisation a été programmée.
Une biopsie cutanée a été pratiquée, confirmant le diagnostic de malformation artério-veineuse.
La patiente a reçu 50 mg/jour de thalidomide et une contraception a été recommandée. Elle a continué de présenter des douleurs chroniques et une perte progressive de la fonction au niveau du bras.
Le diagnostic présumé était un syndrome PHOST (syndrome hamartomateux lié à PTEN au niveau des tissus mous) associé à un syndrome tumoral hamartomateux lié à PTEN (PHTS). Une analyse génétique a donc été demandée et, en concertation avec le Dr Denise Adams, un traitement à base de sirolimus a été mis en place. Ce cas a évolué en des ulcères hémorragiques et des douleurs incontrôlables. Après une évaluation pluridisciplinaire, une amputation du bras a été décidée. La patiente a retrouvé sa fonction cardiaque. Elle continue un traitement par sirolimus pour sa lésion thoracique. Enfin, la mutation du gène PTEN a été confirmée.
Cette pathologie est sous-diagnostiquée et nécessite un diagnostic précoce pour mettre en place un traitement adapté, en sachant que des tumeurs peuvent apparaître à l’âge adulte.
Le Dr Juan Lopez Gutierrez a suggéré la création d’un registre de patients présentant des mutations de PTEN afin d’identifier les différentes manifestations et associations chez ces patients.
Intervenante : Dr Maria Laura Cossio (Chili)
L’intervenante a présenté une patiente chez qui une malformation artério-veineuse intracrânienne accompagnée d’une importante anomalie crânienne secondaire avait été diagnostiquée.
Il s’agissait d’un nouveau-né qui présentait des lésions érythémateuses congénitales sur le cuir chevelu et des convulsions à l’âge d’un mois. IRM : infarctus fronto-temporal droit avec hémorragies dans le parenchyme de l’hémisphère droit et déficience osseuse au niveau de la boîte crânienne.
Un traitement par sirolimus a été instauré lorsque les lésions du cuir chevelu ont commencé à saigner.
La lésion du cuir chevelu n’a pas pu faire l’objet d’une biopsie pour analyse génétique, en raison du risque d’hémorragie.
Le Dr Juan Carlos Lopez Gutierrez pense que des inhibiteurs de MEK tels que le tramétinib pourraient être indiqués. Il recommande une biopsie des lésions du cuir chevelu si possible ou peut-être une analyse génétique à partir d’un prélèvement sanguin.
Intervenante : Alejandro Celisv (Mexique)
Patient âgé de 29 ans, qui présente depuis l’âge de 16 ans une tumeur bleuâtre d’évolution lente sur la lèvre inférieure. À l'âge de 19 ans, des saignements importants ont été observés. Les vaisseaux nutritionnels ont alors fait l’objet d’une embolisation par coil, mais les saignements ont continué et ont nécessité une ligature des vaisseaux. Le patient a reçu du thalidomide pendant un an et son état est resté stable. Une intervention chirurgicale a ensuite été pratiquée, après embolisation, avec résection de la tumeur et reconstruction par lambeaux cutanés. Ce patient est actuellement sous thalidomide et demeure asymptomatique.
Parmi les commentaires, l’accent a été mis sur le traitement précoce et combiné des malformations artério-veineuses.
Intervenante : Dr Irene Lara Corrales (Canada)
L’intervenante a présenté un patient atteint de CM-AVM (malformation capillaire associée à une malformation artério-veineuse).
Ce patient avait été vu en consultation à l’âge de 6 ans pour une croissance asymétrique d’un pied, qui présentait une malformation des capillaires (CM).
L’analyse génétique a confirmé la mutation de RASA1, à la fois dans la biopsie cutanée et dans le prélèvement sanguin. Les analyses génétiques des deux parents se sont révélées négatives.
L’IRM du cerveau et de la colonne vertébrale a révélé une fistule artério-veineuse cérébrale.
La fistule du SNC a été traitée par embolisation, sans récidive à ce jour.
La CM AVM est une RASopathie à transmission autosomique dominante.
18 % des patients présentant des mutations de RAS 1 ont des malformations ou des fistules AV.
Le Dr Baselga suggère que les patients nouvellement diagnostiqués et les adolescents soient invités à passer une IRM du cerveau et de la colonne vertébrale avant leur sortie, même s'ils sont asymptomatiques.
Intervenante : Felipe Enrique Velasquez Valderrama (Pérou)
L’intervenant a évoqué un patient âgé d’un mois qui présentait une tumeur congénitale sur la cuisse, d’apparence vasculaire, érythémato-violacée, accompagnée d’une croûte centrale.
Ce patient a été hospitalisé pour une infection systémique. L’écho-doppler de la tumeur a montré une veine saphène épaissie, des branches collatérales et une tumeur à composante veineuse et artérielle.
Quelques jours plus tard, la tumeur a commencé à saigner. Malgré toutes les tentatives pour arrêter l’hémorragie, le patient est décédé des suites d’un saignement abondant.
Commentaires du Dr Colmenero : les hémangiomes congénitaux rapidement involutifs (RICH) peuvent avoir cette évolution fatale. Lorsque des vaisseaux artériels proéminents sont visibles à l’échographie, ils doivent être embolisés rapidement.
Session animée par : le Dr Agustina Vila Echague
Session co-animée par : le Dr Mirna Erendira Toledo Bahena et le Dr Héctor Cáceres Ríos
Intervenante : Betina Pagotto (Argentine)
L’acné est un trouble inflammatoire chronique de l’unité pilo-sébacée, qui touche principalement les adolescents, mais peut persister à l’âge adulte. D’après les estimations, environ 90 % de la population est touchée à un moment ou à un autre de sa vie. Les principaux facteurs de prédisposition sont l’âge, le type de peau, l’obésité et les antécédents familiaux.
La prévalence atteint presque 100 % à l’adolescence, puis diminue avec l’âge. L’impact de l’acné va au-delà de la peau : elle est associée à une altération de la qualité de vie, à la dépression et à une mauvaise estime de soi, d’où l’importance d’un traitement précoce, en particulier en cas d’acné inflammatoire.
La pathogénie de l’acné est multifactorielle :
Récemment, de nouveaux facteurs ont été identifiés :
Différentes technologies ont été utilisées pour le traitement de l’acné active, voire de ses séquelles :
Mécanismes d’action
Ces traitements, surtout lorsqu’ils sont associés correctement, peuvent améliorer la composante inflammatoire, réduire la colonisation bactérienne et traiter les séquelles en obtenant des résultats esthétiques remarquables.
Intervenante : Dr Agustina Vila Echague (Salvador)
Les malformations capillaires (MC ou taches de vin) sont des malformations vasculaires à faible débit, présentes dès la naissance. Elles sont dues à une mutation du gène GNAQ qui entraîne une ectasie progressive du plexus vasculaire superficiel au niveau de la peau. 0,3 % des nouveau-nés sont concernés.
Sur le plan clinique, différents sous-types cliniques sont observés, allant des macules plates et rose pâle, à des lésions violacées, hypertrophiques ou nodulaires. Un pourcentage important de ces lésions est associé à un syndrome de Sturge-Weber, qui représente environ 20 % de toutes les malformations vasculaires. Les signes de ce syndrome peuvent ne pas être présents dès la naissance, mais se manifester progressivement jusqu’à l’âge de 5 ans. C’est pourquoi il est essentiel de procéder à des examens cliniques et neurologiques pendant au moins les cinq premières années de vie des patients présentant des taches de vin sur le visage afin de confirmer ou d’infirmer la présence du syndrome.
Les MC peuvent être traitées par laser à colorant pulsé (PDL, 595 nm). Il est conseillé de commencer les traitements à un âge précoce, car les vaisseaux sont alors plus superficiels et plus petits.
Référence : He HY, Shi WK, Jiang JC, Gao Y, Xue XM. An exploration of optimal time and safety of 595-nm pulsed dye laser for the treatment of early superficial infantile hemangioma. Dermatol Ther. 2022 May;35(5):e15406. doi: 10.1111/dth.15406. Epub 2022 Mar 9. PMID: 35199898; PMCID: PMC9285537.
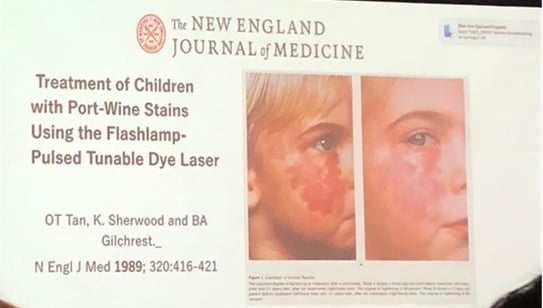
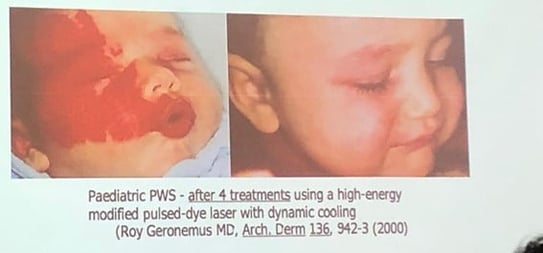
Référence : Geronemus R et al. High fluence modified pulsed dye laser photocoagulation with dynamic cooling of port wine stains in infancy. Arch Derm 2000; 136: 942–943
Intervenante : Héctor Cáceres Ríos (Pérou)
Dans un premier temps, l’intervenant a évoqué les hémangiomes infantiles, qui sont des tumeurs bénignes accompagnées d’une prolifération endothéliale. Ces hémangiomes apparaissent généralement dans les premières semaines de la vie et grandissent rapidement pendant les trois premiers mois, puis leur croissance reste stable ou très faible jusqu’à l’âge d’un an, avant de commencer à involuer et à diminuer lentement. Dans près de 50 % des cas, il existe des signes précurseurs : télangiectasies, macules anémiques ou taches bleutées.
Certaines lésions sont de petite taille, sans répercussion clinique, tandis que d’autres, situées à proximité d’organes vitaux tels que les yeux et la bouche, nécessitent un traitement.
Sur le plan clinique, elles peuvent être superficielles dans 60 % des cas (variante « fraise »), profondes (couleur bleutée) dans 15 % des cas, ou mixtes dans 25 % des cas.
Il est essentiel de les distinguer des processus néoplasiques tels que les lymphomes ou les rhabdomyosarcomes.
Quant à leur origine, les recherches ont montré que ces lésions partagent les mêmes marqueurs que le placenta, ce qui renforce la théorie d’une embolisation du tissu placentaire. L’expression de GLUT-1, de la mérosine, de FcYRII et de l’antigène Lewis Y, entre autres, a été détectée, ce qui confirme que l’hémangiome est un processus de vasculogenèse et d’angiogenèse, influencé par différents facteurs.
Traitements combinés : il a également évoqué la possibilité d’associer des traitements topiques et systémiques au laser.
Les connaissances actuelles concernant la génétique des anomalies vasculaires et la disponibilité de technologies laser efficaces permettent une approche plus précise et personnalisée. La mise en place précoce du traitement améliore les résultats cliniques et la qualité de vie des patients pédiatriques.
Références :
Asilian, Ali1,2,3; Mokhtari, Fatemeh1,3; Kamali, Atefeh Sadat1,3,4,; Abtahi-Naeini, Bahareh1,3; Nilforoushzadeh, Mohammad Ali2,5; Mostafaie, Shayan3,6. Pulsed dye laser and topical timolol gel versus pulse dye laser in treatment of infantile hemangioma: A double-blind randomized controlled trial. Advanced Biomedical Research 4(1):p 257, | DOI: 10.4103/2277-9175.170682
Kavitha K. Reddy MD, Francine Blei MD, Jeremy A. Brauer MD, Milton Waner MD, Robert Anolik MD, Leonard Bernstein MD, Lori Brightman MD, Elizabeth Hale MD, Julie Karen MD, Elliot Weiss MD, Roy G. Geronemus MD Retrospective Study of the Treatment of Infantile Hemangiomas Using a Combination of Propranolol and Pulsed Dye Laser. Dermatol Surg Volume39, Issue6. June 2013.Pages 923-933.https://doi.org/10.1111/dsu.12158
Intervenante : Dr Mirna Erendira Toledo Bahena (Mexique)
Le Dr Toledo Bahena a tout d’abord évoqué les progrès réalisés dans le domaine des lasers au cours des 30 dernières années, progrès qui ont permis de nouvelles stratégies thérapeutiques face aux affections cutanées courantes chez l’enfant. L’intervenante a souligné que le traitement au laser est une alternative non invasive aux options chirurgicales et que, dans de nombreux cas, ce traitement peut offrir de meilleurs résultats.
Quand il est pratiqué par des mains expertes, le traitement au laser s'est avéré sans danger pour les adultes et les enfants. Il s’agit là d’un aspect très important et il est essentiel de recevoir une formation spécifique au traitement des enfants.
Chez l’enfant et l’adolescent, le champ d’application de ce traitement a été étendu à une variété d’affections, y compris les lésions vasculaires et pigmentaires, ainsi que les maladies inflammatoires, les cicatrices, le vitiligo et également le retrait des tatouages et l’épilation.
Le laser fonctionne en émettant une lumière monochromatique de haute intensité, qui est absorbée par des structures bien précises de la peau appelées chromophores. Cette absorption génère une destruction thermique sélective de la cible sans endommager les tissus environnants. Dans les lésions vasculaires, le chromophore est l’hémoglobine et dans les lésions pigmentaires, la mélanine.
Dans les lésions pigmentaires, le chromophore est la mélanine ; dans les lésions vasculaires, c’est l’hémoglobine. L’absorption de la lumière varie de 250 à 1 200 nm, en fonction de la profondeur de la lésion.
Les lasers Q-switched ou picosecondes fragmentent le pigment pour qu’il soit éliminé par le système lymphatique. Ils sont idéaux face à de nombreuses affections que nous traitons en dermo-pédiatrie, mais également pour éliminer les tatouages.
Pour les lésions pigmentaires telles que le naevus d’Ota, le laser Q-switched est le traitement de référence. Les lasers Nd:YAG, à rubis ou Alexandrite sont également utilisés. Ils détruisent le pigment dermique par photoacoustique.
Une étude a rapporté qu’environ 5 séances de laser Alexandrite permettaient d’obtenir une efficacité de 50 % et entraînaient peu d’effets indésirables (entre 2 et 7,9 %). Le Dr Toledo Bahena a expliqué que, dans son hôpital, 15 patients (âgés de 3 à 16 ans, phototype IV) ont été traités, puis leur réponse a été évaluée après plusieurs séances de laser Q-switched Nd:YAG.
Les résultats :
• 45 % ont présenté une réponse excellente ;
• 13 % ont présenté une réponse modérée ;
• 25 % ont présenté une réponse insatisfaisante.
Un seul patient a présenté une hyperpigmentation résiduelle.
L’intervenante a montré plusieurs photos d’enfants qui ont été traités pour un nævus d’Ota et ont obtenu de bons résultats.
Elle a également parlé du laser à excimère face aux affections pigmentaires...
Bien qu’il ne s'agisse pas d’un laser à proprement parler, la lumière excimère (308 nm) est une technologie très utile face à des pathologies comme le vitiligo. Elle agit en induisant l’apoptose des lymphocytes et des kératinocytes, et stimule la migration des mélanocytes et la production de mélanine.
Il s’agit d’une option sans danger, qui agit uniquement sur l’épiderme, et qui est donc idéale pour les enfants et les patients à la peau sensible.
Références :
Sakio R, Ohshiro T, Sasaki K, Ohshiro T. Usefulness of picosecond pulse alexandrite laser treatment for nevus of Ota. Laser Ther. 2018 Dec 31;27(4):251–255. doi:10.5978/islsm.27_18-OR-22
Mejoría clínica de pacientes pediátricos con nevo de ota utilizando tecnología láser Q-Switched en el Hospital Infantil de México Federico Gómez. https://hdl.handle.net/20.500.14330/TES01000761986
Intervenante : Jean L. Bolognia (États-Unis)
Le Dr Jean L. Bolognia a proposé un voyage clinique et pathologique le long de la « route des taches bleues », de la mélanocytose dermique congénitale sacrée aux nævus bleus cellulaires, en mettant l’accent sur les aspects cliniques, histologiques, génétiques et les implications diagnostiques de ces lésions pigmentaires d’origine mélanocytaire. Elle a également évoqué les entités comme le nævus d’Ota, d’Ito, les formes acquises et congénitales, ainsi que l’association avec les syndromes neurocutanés, le potentiel malin et la prise en charge thérapeutique.
1. Mélanocytose dermique congénitale (MDC)
2. Nævus d’Ota et d’Ito
Nævus d’Ota : également appelé mélanocytose oculodermique. Il touche les dermatomes V1-V2, est généralement unilatéral et s’accompagne d’une atteinte oculaire (50 % dans les formes légères, jusqu’à 100 % dans les formes étendues).
Nævus d’Ito : similaire, mais à proximité du nerf brachial ; pas d’atteinte oculaire.
L’intervenante a également décrit le nævus bilatéral acquis associé à des macules de type Ota (ABNOM), également connu sous le nom de nævus de Hori. Cette mélanocytose dermique bénigne se caractérise par l’apparition de macules bleu-brun ou gris ardoise sur le visage, en particulier sur les joues, les tempes et le front. Elle est le plus souvent observée chez les femmes d’origine asiatique après 40 ans. L’ABNOM diffère du nævus d’Ota par son apparition plus tardive et l’absence d’atteinte de la conjonctive, de la muqueuse et de la membrane tympanique.
3. Aspects génétiques communs
4. Nævus bleu
Les termes « commun » et « cellulaire » se rapportent à l’histologie et non au tableau clinique.
Combinés : association d’un nævus en partie bleu (couleur grisâtre).
L’histologie est essentielle pour distinguer les formes bénignes des formes malignes.
5. Variantes et entités apparentées
La mélanocytose dermique congénitale et les différents types de nævus bleus représentent un large éventail de lésions mélanocytaires aux répercussions cliniques, génétiques et pronostiques diverses. Une connaissance détaillée de leur tableau clinique, de leur distribution anatomique, de leurs caractéristiques histologiques et de leurs associations syndromiques permet de poser un diagnostic précis, d’identifier les cas à risque de malignité et de mettre en place un suivi adapté, y compris une surveillance ophtalmologique et une éventuelle imagerie du SNC chez certains patients. L’identification de mutations de GNAQ/GNA11 et la perte de BAP1 sont des éléments clés pour comprendre la biologie de cette affection et son risque de transformation maligne.
Références :
Cordova A. The Mongolian spot: a study of ethnic differences and a literature review. Clinical Pediatrics 1981 vol 20: 714–719
Romagnuolo M, Moltrasio C, Gasperini S, Marzano AV, Cambiaghi S. Extensive and Persistent Dermal Melanocytosis in a Male Carrier of Mucopolysaccharidosis Type IIIC (Sanfilippo Syndrome): A Case Report. Children (Basel). 2023 Dec 13;10(12):1920. doi: 10.3390/children10121920. PMID: 38136122; PMCID: PMC10742075.
Intervenante : Dr Amy Paller (États-Unis)
Le prurit est une manifestation courante dans diverses dermatoses, mais sa prise en charge dans des maladies génétiques telles que l’ichtyose (désormais appelée troubles de la différenciation épidermique) et l’épidermolyse bulleuse (EB) représente un défi clinique considérable.
Jusqu’à 17 % des enfants et des adolescents présentent un prurit chronique, qui est encore plus fréquent en cas de maladie génétique au niveau de la peau. Des scores tels que le NRS (Numerical Rating Scale) ou l’EVA (échelle visuelle analogique) ont été validés pour quantifier l’intensité du prurit, et il existe des versions adaptées aux parents d’enfants qui ne peuvent pas s’auto-évaluer. Toutefois, l’intervenante insiste sur la nécessité de procéder à des évaluations plus globales qui tiennent compte de l’impact sur la santé physique, mentale et sociale.
Des dispositifs tels que des gants équipés de capteurs, des capteurs numériques et des systèmes acoustiques portables (par exemple, le capteur ADAM) ont été mis au point pour enregistrer les épisodes de grattage pendant le sommeil et les différencier d'autres mouvements.

Le prurit est transmis par les fibres nerveuses C et A-delta, dont les terminaisons atteignent l’épiderme. Ces neurones expriment des récepteurs clés tels que l’IL-4, l’IL-13 et l’IL-31 et communiquent de manière bidirectionnelle avec les kératinocytes et les immunocytes, amplifiant ou régulant le stimulus prurigineux.
Staphylococcus aureus résistant à la méticilline (SARM) induit un prurit chez des modèles murins en produisant de la protéase V8, qui active le récepteur PAR-1 au niveau des fibres nerveuses. Cette voie, indépendante de l’histamine et des IL, ouvre de nouvelles perspectives thérapeutiques par le biais des inhibiteurs topiques de PAR-1.
Jusqu’à 93 % des patients présentent un prurit. Les études sur la prégabaline ont montré un bénéfice en ce qui concerne la douleur neuropathique, mais peu d’effet sur le prurit. Dans les modèles murins, l’utilisation de modulateurs du système endocannabinoïde est explorée et donne des résultats prometteurs.
Une augmentation de la substance P a été documentée dans la peau des patients atteints d’une EB dystrophique, en corrélation avec l’intensité accrue du prurit. Les antagonistes des récepteurs de la neurokinine 1 (NK-1), tels que le serlopitant, ont montré une tendance à réduire le prurit dans des études pilotes.
Selon une enquête récente, 45 % des patients atteints d’une EB utilisent des produits à base de tétrahydrocannabinol/cannabidiol (THC/CBD), et 64 % d’entre eux font état d'une amélioration du prurit. Les récepteurs cannabinoïdes CB1 et CB2 sont présents dans les ganglions de la racine dorsale et les fibres cutanées, et des altérations de leur expression ont été identifiées chez des modèles animaux.
Traitements actuels : biothérapies et inhibiteurs de JAK
Cette biothérapie est un anticorps monoclonal humain ciblant la sous-unité du récepteur α de l’interleukine 4 (anti-IL-4Rα) approuvé dans le traitement de la dermatite atopique. Il a été évalué dans une étude ouverte chez des patients atteints d’épidermolyse bulleuse (n = 22). Après 16 semaines, une réduction significative du prurit modéré et sévère a été observée, et des améliorations objectives du sommeil ont été documentées à l’aide d’appareils d’enregistrement. La réponse était indépendante des taux d’IgE initiaux.
Dans un sous-groupe atteint d’épidermolyse bulleuse jonctionnelle (déficit en collagène VII), une réduction de plus de 4 points sur le score du prurit a été documentée, baisse qui a eu des impacts positifs sur l’autonomie et la qualité de vie. L’innocuité était favorable : des réactions locales minimes et un seul cas de conjonctivite légère.
Anti-IL-31R (némolizumab) : potentiel thérapeutique, notamment en raison de la corrélation entre l’IL-31 et le prurit dans l’EB.
Inhibiteurs de JAK : utilisés hors AMM (baricitinib, tofacitinib, etc.) avec de bons résultats dans la réduction du prurit et des lésions face à l’EB, malgré un profil de risque préoccupant chez les patients immunodéprimés.
Le prurit dans les maladies génétiques est multifactoriel et fait intervenir des mécanismes neuro-immunologiques complexes. L’intégration d’outils objectifs, associée à des traitements ciblés (biothérapies, cannabinoïdes, inhibiteurs de voies spécifiques), ouvre un nouveau paradigme dans la prise en charge personnalisée de ces patients. Des études supplémentaires sont nécessaires pour optimiser les stratégies thérapeutiques sûres et efficaces chez les enfants concernés.
Référence :
Deng L, Costa F, Blake KJ, Choi S, Chandrabalan A, Yousuf MS, Shiers S, Dubreuil D, Vega-Mendoza D, Rolland C, Deraison C, Voisin T, Bagood MD, Wesemann L, Frey AM, Palumbo JS, Wainger BJ, Gallo RL, Leyva-Castillo JM, Vergnolle N, Price TJ, Ramachandran R, Horswill AR, Chiu IM. S. aureus drives itch and scratch-induced skin damage through a V8 protease-PAR1 axis. Cell. 2023 Nov 22;186(24):5375-5393.e25. doi: 10.1016/j.cell.2023.10.019. PMID: 37995657; PMCID: PMC10669764.
Intervenant : Dr Giovanni Pellacani (Italia)
Cette session a abordé les critères les plus pertinents pour le diagnostic différentiel des nævus mélanocytaires, l’importance du suivi clinique et les indications pour l’exérèse. L’intervenant a principalement évoqué le mélanome, tumeur maligne extrêmement rare chez l’enfant. Cette rareté, associée à la grande variabilité clinique et dermoscopique des naevus chez l’enfant, pose d’importantes difficultés diagnostiques et thérapeutiques.
Utile pour identifier des schémas évocateurs d’une tumeur maligne, par exemple...
Lorsque les enfants sont en âge d’être scolarisés, des lésions peuvent apparaître et présenter :
Lésions présentant :
Dans ces cas, une exérèse diagnostique accompagnée de marges suffisantes est recommandée.
Présentation d’un cas clinique...
Le mélanome chez l’enfant est une entité rare, mais cliniquement pertinente.
Tout nævus congénital de taille moyenne ou grande doit être soigneusement évalué et suivi dans le temps.
L’examen clinique et la dermoscopie sont essentiels à la prise de décision.
L'exérèse selon des marges suffisantes doit être indiquée face à toute suspicion d’examen clinique ou dermoscopique atypique.
Il est essentiel à la fois de ne pas sous-estimer ni surestimer les lésions pigmentées chez l’enfant.
Référence :
Excised melanocityc lesions in children and adolescents-a 10 year survey. E Moscarella 1, I Zalaudek, L Cerroni, I Sperduti, C Catricalà, J Smolle, R Hofmann-Hellenhof, A Sgambato, G Pellacani, G Argenziano. Br J Dermatol. 2012 Aug;167(2):368-73. doi: 10.1111/j.1365-2133.2012. 10952.x
Intervenante : Dr Horacio Cabo (Argentine)
La pigmentation des ongles est une consultation dermatologique fréquente. Bien qu’il s’agisse le plus souvent de lésions bénignes, il existe un risque faible, mais significatif de mélanome sous-unguéal, même chez l’enfant. Cette présentation aborde la difficulté du diagnostic, l’utilisation de la dermoscopie et les principaux critères cliniques permettant de différencier une mélanonychie bénigne d’un mélanome.
Physiopathologie et tableau clinique
Mélanome sous-unguéal : épidémiologie et cas cliniques
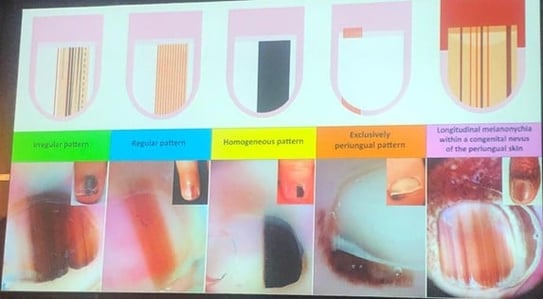
Intervenante : Dr Virginia Gonzalez (Argentine)
La dermoscopie n’est plus un outil exclusivement réservé à l’évaluation des lésions pigmentaires, mais est devenue une méthode essentielle pour le diagnostic de diverses dermatoses inflammatoires, infectieuses et parasitaires. Surnommée « le stéthoscope du dermatologue », son utilisation systématique après l’examen clinique permet d’améliorer la précision du diagnostic, d’éviter les biopsies inutiles et de faciliter le suivi thérapeutique.
Principes de l’analyse dermoscopique dans les maladies inflammatoires
Exemples cliniques remarquables
Psoriasis
Eczéma
Pityriasis rosé
Porokératose
Maladies granulomateuses (par exemple, sarcoïdose, rosacée granulomateuse)
Lichens et maladies prurigineuses
Gale (scabiose)
Pédiculose (poux)
Molluscum contagiosum
Verrues (HPV)
Coloration et fluorescence : nouvelles clés
La dermoscopie est un outil de diagnostic inestimable en dermatologie générale, et son utilisation devrait être étendue au-delà des lésions pigmentées.
L’incorporation de la lumière UV permet de détecter des fluorescences utiles dans de multiples pathologies inflammatoires et infectieuses.
La bonne utilisation de cet outil permet d’éviter les biopsies inutiles, d’améliorer le suivi thérapeutique et d’accroître la précision clinique.
Il est recommandé d’intégrer la dermoscopie dans l’évaluation de routine des dermatoses et de se familiariser avec les signes caractéristiques de chaque entité.
Intervenante : Dr Rosario Peralta (Argentine)
La dermoscopie est un outil essentiel pour l’évaluation non invasive des lésions vasculaires au niveau de la peau. Chez l’enfant, il permet une meilleure caractérisation des tumeurs et des malformations vasculaires, optimisant le diagnostic différentiel par rapport aux lésions mélanocytaires ou même malignes. L’identification de motifs vasculaires spécifiques facilite la classification et la prise en charge de ces lésions, souvent sans qu’une biopsie ne soit nécessaire.
1. Hémangiome infantile
- Lésion vasculaire bénigne la plus fréquente chez l’enfant.
- Lacunes rouge-violet bien définies et de tailles différentes.
- Motif homogène ou en mosaïque ; pas de structures supplémentaires.
- Évolution : les couleurs varient en fonction de la profondeur de la composante vasculaire.
2. Angiome en touffes
- Vaisseaux linéaires périphériques proéminents, souvent accompagnés de zones d’érythrose.
- Variabilité structurelle fréquente : des zones blanches à la structure particulière sont parfois observées.
3. Tumeur glomique
- Lésion douloureuse, bleuâtre ou noirâtre.
- Dermoscopie : zones bleu-violet, structure de voile blanc-bleu et parfois motif d’arc-en-ciel.
- Signes de thrombose : zones noires homogènes ou structures en « creux noirs ».
4. Angiokératome
- Lacunes rouges, bleues foncées ou noires, parfois accompagnées d’hyperkératose.
- Présence de zones blanchâtres et thromboses fréquentes.
- Diagnostic différentiel : mélanome métastatique ou mélanome nodulaire.
5. Lymphangiome (malformation lymphatique superficielle)
- Lacunes jaunâtres, blanchâtres ou rosâtres, parfois mélangées à des lacunes rouge-violet.
- Motif polymorphe : mélange de lacunes claires et hémorragiques.
- Dermoscopie UV : la fluorescence varie en fonction de la quantité de liquide.
6. Angiosarcome (à prendre en compte dans le diagnostic différentiel)
- Bien que rare chez l’enfant, il doit être envisagé en cas de tumeur vasculaire à croissance rapide.
- Dermoscopie : zones rougeâtres homogènes accompagnées de lignes vasculaires irrégulières et de zones d’ulcération.
- Il est important d’envisager un angiosarcome en cas de lésion atypique semblable à un hémangiome.
7. Malformations capillaires et veineuses
- Malformation capillaire : taches rouges, linéaires ou serpigineuses, selon qu'elles sont superficielles ou profondes.
- Malformation veineuse : lacunes bleuâtres ou violacées, sans structures spécifiques, souvent compressibles.
- Distribution selon la localisation des vaisseaux (horizontale ou verticale dans le derme superficiel ou profond).
Une interprétation correcte de ces résultats, associée au jugement clinique, permet d’éviter des actes inutiles tels que les biopsies chez les enfants et d’améliorer l’approche thérapeutique.
Intervenante : Dr Ramiro Cano (Argentine)
La trichoscopie est un outil non invasif qui a révolutionné l’approche diagnostique face à l’alopécie de l’enfant. Cet instrument permet d’évaluer le cuir chevelu et les tiges capillaires par dermoscopie, ce qui facilite le diagnostic différentiel entre les différentes étiologies de l’alopécie. Cette présentation portait sur les applications cliniques de la trichoscopie pour différencier les causes les plus courantes de l’alopécie en plaques chez l’enfant, principalement la teigne, la pelade et la trichotillomanie.
1. Approche diagnostique en trois étapes
Étape 1 : anamnèse et examen physique détaillé pour classer l’alopécie dans l'une des catégories suivantes...
Étape 2 : évaluation initiale à la trichoscopie pour déterminer s’il s’agit d’une...
Étape 3 : trichoscopie détaillée pour identifier des motifs spécifiques et confirmer le diagnostic clinique présumé.
2. Classification et motifs à la trichoscopie
trichotillomanie
3. Observations les plus utiles à la trichoscopie pour le diagnostic différentiel
|
cheveux en tire-bouchon, en zigzag, en bloc, en code morse. |
|
cheveux en points d’exclamation, duvet, cheveux en cercle, effilés. |
|
cheveux en poussière, forme de V, cheveux en flammes, hémorragies ponctuelles. |


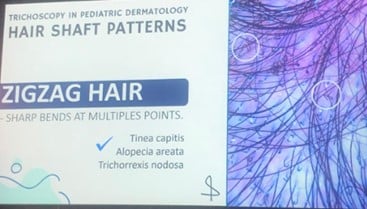
La trichoscopie est une technique utile et accessible pour le diagnostic et le suivi de l’alopécie chez l’enfant, en particulier en ambulatoire. Bien que de nombreuses observations soient communes à différentes affections, certains schémas ont une valeur diagnostique spécifique élevée. Une approche structurée, reposant sur l’anamnèse, l’examen physique et une trichoscopie ciblée, permet :
Les dermato-pédiatres doivent impérativement se familiariser avec les principaux motifs observés à la trichoscopie afin d’optimiser la prise en charge de ces affections.
Intervenante : Dr Gabriel Salerni (Argentine)
L’intervenant a présenté une sélection de cas cliniques observés dans la population pédiatrique, dans le but de mettre en évidence les schémas cliniques et dermoscopiques pertinents dans le diagnostic différentiel des lésions nodulaires et pigmentées. Les sujets abordés allaient d’entités bénignes de résolution spontanée telles que le granulome idiopathique de la face à des pathologies plus graves telles que le mélanome de l’enfant.
Patiente : fillette de 9 ans présentant un nodule érythémateux de 2 cm sur la joue, évoluant depuis 3 semaines, sans antécédents de traumatisme ni de piqûre.
Référence :
Errichetti E et al. Dermoscopy of idiopathic facial aseptic granuloma (IFAG): an observational controlled study Int Dermatol 2025 Feb; 64(2):422-424
Cas chez les enfants et les adolescents, typiquement sous forme de nodules rouges ou pigmentés au niveau du visage ou des extrémités.

Référence :
Lallas A, Apalla Z, Papageorgiou C, Evangelou G, Ioannides D, Argenziano G. Management of Flat Pigmented Spitz and Reed Nevi in Children. JAMA Dermatol. 2018 Nov 1;154(11):1353-1354. doi: 10.1001/jamadermatol.2018.3013.
Kerner M, Jaimes N, Scope A, Marghoob AA. Spitz nevi: a bridge between dermoscopic morphology and histopathology. Dermatol Clin. 2013 Apr;31(2):327-35. doi: 10.1016/j.det.2012.12.009. Epub 2013 Jan 30. PMID: 23557659.
Adolescent de 16 ans présentant une lésion violacée saignante au niveau du genou.
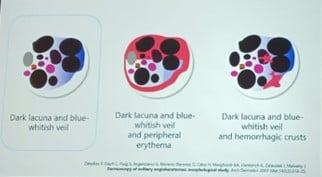
Référence
Zaballos P, Daufí C, Puig S, Argenziano G, Moreno-Ramírez D, Cabo H, Marghoob AA, Llambrich A, Zalaudek I, Malvehy J. Dermoscopy of solitary angiokeratomas: a morphological study. Arch Dermatol. 2007 Mar;143(3):318-25. doi: 10.1001/archderm.143.3.318. PMID: 17372096.
Cas inhabituel d’un garçon de 12 ans présentant une lésion polymorphe au niveau de la jambe depuis 3 mois.
La classification a été revue...
L'utilisation de la méthode ABCD modifiée a été discutée :
D : de novo.
Deux cas chez des enfants de 4 ans.
Intervenants : Bruno Ferrari (Argentine), Dr Carla Torres Zegarra (États-Unis)
- Le molluscum contagiosum (MC) est une infection virale infantile courante causée par un poxvirus qui touche la peau et parfois les muqueuses.
- Cette affection prend la forme de papules ombiliquées, généralement asymptomatiques, situées n’importe où sur le corps.
- Cette maladie bénigne disparaît sans traitement chez les patients immunocompétents.
- Le MC disparaît généralement spontanément dans les 6 à 12 mois, mais peut durer jusqu'à 18, voire 30 mois.
- Au cours de son évolution, une inflammation locale accompagnée de signes d’eczéma (phénomène du « début de la fin ») peut apparaître, généralement avant la disparition des lésions.
- Les « cicatrices » ne sont généralement pas définitives.
- Dans la plupart des cas, aucun traitement actif n’est nécessaire.
- Les traitements disponibles (cryothérapie, imiquimod, curetage, injections intralésionnelles) peuvent être douloureux, être sources d’angoisse, laisser des cicatrices et nécessiter de multiples consultations médicales.
- Il n’existe aucune donnée probante démontrant que le traitement accélère de manière significative la résolution par rapport à l’observation.
- Revue Cochrane 2017 : aucune supériorité claire n’a été trouvée que ce soit entre les traitements, ou par rapport à l’observation.
- Les études soulignent que de nombreux traitements ont une efficacité limitée (30-40 %) et sont associés à des récidives.
- Les actes douloureux génèrent de l’anxiété chez les enfants et une aversion pour les consultations médicales futures.
- Les multiples séances de traitement représentent une charge émotionnelle et financière pour les familles.
- Le MC est légèrement contagieux, puisque le taux de transmission intrafamiliale est estimé à 30-40 %.
- Il n'est pas recommandé de restreindre les activités des enfants (par exemple, l’école, la natation).
- Des mesures d’hygiène de base sont conseillées : éviter de se gratter, couvrir les lésions enflammées, ne pas partager les articles d’hygiène personnelle.
- Patients immunodéprimés.
- Infections étendues ou réfractaires.
- Atteinte faciale ou génitale ayant un impact esthétique ou fonctionnel.
- Lésions accompagnées d’un eczéma secondaire sévère.
- Le molluscum contagiosum est une infection virale de résolution spontanée chez la plupart des enfants en bonne santé.
- Le traitement actif n’est pas systématiquement nécessaire et peut présenter plus de risques que de bénéfices.
- L’observation clinique doit être considérée comme la première ligne de traitement chez les patients en bonne santé.
- Il est essentiel d’informer les parents et les aidants concernant l’évolution naturelle de la maladie et d’éviter les traitements inutiles.
Référence : van der Wouden JC, van der Sande R, Kruithof EJ, Sollie A, van Suijlekom-Smit LW, Koning S. Interventions for cutaneous molluscum contagiosum. Cochrane Database Syst Rev. 2017 May 17;5(5):CD004767. doi: 10.1002/14651858.CD004767.pub4. PMID: 28513067; PMCID: PMC6481355.
Intervenante : Dr Maria Gnarra Buethe (États-Unis)
Le thème central était la prise en charge de la douleur, l’anxiété et le vécu global des patients pédiatriques lors des actes dermatologiques mineurs.
La détresse lors des actes de dermatologie pédiatrique représente un défi clinique majeur, tant pour les patients que pour leur entourage familial. L’intervenante a présenté une approche pluridisciplinaire visant à réduire la douleur et l’anxiété et à améliorer le vécu des enfants grâce à des interventions avant, pendant et après les actes pratiqués.
1. Préparation avant l’acte de dermatologie
Il est recommandé de commencer l’orientation des patients et des aidants avant le jour J. L’intervention d’un spécialiste de la vie de l’enfant, si possible, améliore la compréhension et réduit l’anxiété. Ce processus peut également être réalisé dans la salle d’intervention, pendant l’examen des consentements.
2. Organisation de l’environnement chirurgical
La préparation du matériel hors du champ de vision de l’enfant et le fait que tout soit prêt pour un acte efficace (< 30 secondes dans le cas des biopsies à l’emporte-pièce) sont essentiels pour réduire la détresse.
3. Positionnement du patient
Différentes techniques d’immobilisation confortable, adaptées à l’âge du patient, sont décrites...
Enfants en bas âge : enveloppés (emmaillotés) dans des champs.
Enfants plus âgés : positions ergonomiques sur les genoux de la personne qui s’occupe de l’enfant, de manière à pouvoir accéder aux différentes zones anatomiques requises.
4. Techniques de distraction
La distraction active (par exemple, les jeux vidéo) s’est avérée plus efficace que la sédation légère (midazolam) et la distraction passive (par exemple, les dessins animés) pour réduire à la fois la douleur et l’anxiété. Il est recommandé de se familiariser au préalable avec les applications et leur adéquation en fonction du site concerné (mains libres si l’acte sera pratiqué sur les membres).
5. Outils de distraction supplémentaires
Les jouets sensoriels et la réalité virtuelle (VR) ont été évoqués. La VR et les casques antibruit offrent des avantages similaires et sont tous deux efficaces pour réduire l’anxiété périopératoire.
6. Validation et renforcement positif
Le langage doit viser à renforcer le courage de l’enfant et éviter les associations négatives (« c’était douloureux »). L’accent est mis sur l’utilisation de questions de distraction et de déclarations validant le ressenti.
7. Maîtrise de la douleur
Nouveau-nés : le contact peau à peau, l’allaitement et la solution de saccharose diminuent les signes de douleur (grimace faciale, fréquence cardiaque).
Anesthésies topiques :
Prudence en cas de méthémoglobinémie chez les nourrissons.
Amélioration de l’anesthésie topique : une plus grande efficacité a été documentée quand ces anesthésiques sont appliqués après une cryothérapie, qui altère la barrière épidermique.
8. Anesthésie par infiltration
Utiliser des petites aiguilles.
La lidocaïne est moins douloureuse quand elle est chaude que quand elle est froide.
La lidocaïne tamponnée (avec du bicarbonate de sodium) diminue la douleur associée à l’infiltration sans preuve évidente de perte de puissance ou de stabilité.
Technique d’injection : commencer dans le derme profond et avancer superficiellement.
9. Méthodes complémentaires
Refroidissement local : glace, chloroéthane.
Vibrations (théorie du portillon) : le dispositif doit être placé à proximité du site chirurgical et entre ce dernier et le cerveau.
Cryothérapie ludique au niveau du cuir chevelu : utilisation de ballons d’eau congelés pour l’analgésie avant l’infiltration.
10. Sédation et anesthésie générale
Protoxyde d’azote : couramment utilisé en odontologie pédiatrique, efficace pour la sédation légère, nécessite une surveillance du risque d’hypoxémie.
Anesthésie générale : les parents doivent être informés de la mise en garde de la FDA concernant les enfants de moins de 3 ans pour les interventions longues (> 3 h) ou répétitives, telles que les traitements au laser face aux malformations capillaires.

Favoriser un environnement détendu et calme pour soulager l’anxiété des patients.
Appliquer des anesthésies topiques chaque fois que cela est nécessaire pour réduire l’inconfort.
Injecter l’anesthésie par infiltration lentement, en commençant par des niveaux plus profonds pour une meilleure tolérance.
L’utilisation de techniques de distraction, d’applications mobiles, de musique, de conversations ou d’interactions avec l'aidant peut être efficace.
Intervenante : John McGrath (Royaume-Uni)
Les génodermatoses constituent un large groupe d’affections cutanées héréditaires, dont beaucoup présentent une morbidité élevée et nécessitent des approches diagnostiques et thérapeutiques complexes. Plus de 8 000 maladies mendéliennes sont reconnues à l’heure actuelle, dont plus de 1 000 ont des manifestations cutanées. Cette présentation a permis de faire le point sur les avancées en matière de diagnostic moléculaire et de stratégies thérapeutiques émergentes, particulièrement face à l’épidermolyse bulleuse (EB) et aux affections apparentées.
Exemple : maladie associée à la cobalamine J - maladie autosomique récessive du métabolisme de la vitamine B12 entraînant une hyperpigmentation progressive, qui peut être traitée avec succès par la vitamine B12. Le diagnostic a été posé grâce au NGS, qui a mis en évidence le gène ABCD4. Ces patients non traités courent un risque accru d’accident vasculaire cérébral à partir de la vingtaine.
Référence : Takeichi T, Hsu CK, Yang HS, Chen HY, Wong TW, Tsai WL, Chao SC, Lee JY, Akiyama M, Simpson MA, McGrath JA. Progressive hyperpigmentation in a Taiwanese child due to an inborn error of vitamin B12 metabolism (cblJ). Br J Dermatol. 2015 Apr;172(4):1111-5. doi: 10.1111/bjd.13413. Epub 2015 Feb 27. PMID: 25234635.
L’intervenant a également évoqué la complexité thérapeutique de l’épidermolyse bulleuse en raison de son étiopathogénie. L’EB dystrophique est associée à une altération du collagène de type VII accompagnée d’une formation déficiente des fibrilles d’ancrage. En plus des dommages structurels, il existe une forte composante inflammatoire systémique, induite par le TGF-β, qui favorise la fibrose et le carcinome épidermoïde.
Face aux génodermatoses, et en particulier face à l’EB, nous sommes passés d’une approche purement symptomatique à une ère de médecine de précision et de thérapies ciblées. L’identification moléculaire des altérations génétiques a joué un rôle clé dans la mise au point de thérapies ciblées, dont certaines sont curatives. Toutefois, l’accessibilité, le coût et la personnalisation du traitement restent des obstacles majeurs. Une approche globale est nécessaire, combinant le traitement principal, le contrôle de l’inflammation et la prise en charge des signes et symptômes, tous selon les priorités du patient.
Intervenante : Dr Cristina Has (Allemagne)
La pharmacogénétique et la pharmacogénomique (PGx) sont des disciplines en pleine évolution qui étudient l’influence de la variabilité génétique individuelle sur la réponse aux médicaments. Alors que la pharmacogénétique se concentre sur l’influence de gènes individuels, la pharmacogénomique prend en compte de multiples interactions génétiques. Ces domaines permettent de progresser vers une médecine personnalisée, présentant une plus grande efficacité thérapeutique et un risque moindre d’effets indésirables, notamment de réactions cutanées graves (SCAR) telles que le syndrome de Stevens-Johnson (SJS) et la nécrolyse épidermique toxique (NET).

Référence : Kabbani et al. Pharmacogenomics in Practice: A Review and Implementation Guide. Frontiers in Pharmacology, 18 de mayo de 2023. DOI: 10.3389/fphar.2023.1189976
Histoire et évolution
Le terme « pharmacogénétique » a vu le jour en 1959.
Jalons : découverte des enzymes du cytochrome P450 qui contrôlent le métabolisme de la plupart des médicaments et des gènes HLA associés aux réactions d’hypersensibilité.
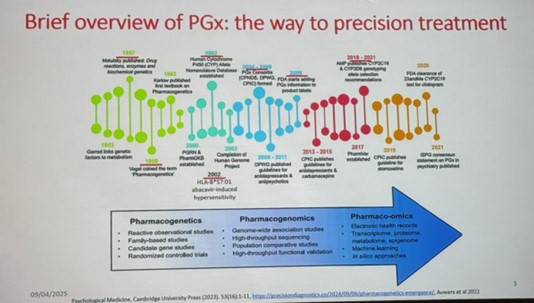
Événements majeurs dans l’émergence de la pharmacogénomique en psychiatrie. AMP, Association of Molecular Pathology ; CPIC, Clinical Pharmacogenetics Implementation Consortium ; CPNDS, Canadian Pharmacogenomics Network for Drug Safety ; DPWG, Dutch Pharmacogenetics Working Group ; FDA, Food and Drug Administration ; ISPG, International Society of Psychiatric Genetics ; PGRN, Pharmacogenomics Global Research Network ; PGx, pharmacogénomique ; PharmGKB, Pharmacogenomics Knowledge Base ; PharmVar, Pharmacogene Variation Consortium.
Études : d’observation, familiales, gènes candidats, essais cliniques.
Techniques modernes : étude d'association pangénomique (GWAS), séquençage à haut débit (HTS), technologies multi-omiques (génomique, transcriptomique, protéomique, métabolomique, etc.), intelligence artificielle.
Étapes nécessaires : recherche fondamentale → validation → bases de données → directives cliniques → mise en œuvre.
Des consortiums internationaux tels que le CPIC® (Clinical Pharmacogenetics Implementation Consortium) ou PharmGKB® émettent des directives fondées sur des données probantes (par exemple) qui sont accessibles à tous.


Référence : Auwerx, Chiara et al.From pharmacogenetics to pharmaco-omics: Milestones and future directions. Human Genetics and Genomics Advances, Volume 3, Issue 2, 100100
Modèle sur place (directement dans l’établissement) : un ou plusieurs gènes et des médicaments bien précis sont testés avant le traitement ou lorsque le patient ne répond pas au traitement ou a présenté des réactions indésirables.
Préventif : modèle préventif dans lequel un large profil génétique est étudié, indépendamment des antécédents cliniques du patient.
Méthodes : panels de gènes candidats, exome ou génome entier.
La prescription personnalisée en temps réel nécessite un processus complexe : consentement éclairé, extraction, interprétation et ajustement du traitement.
Spécialistes impliqués : pharmacogénéticiens et équipes pluridisciplinaires.
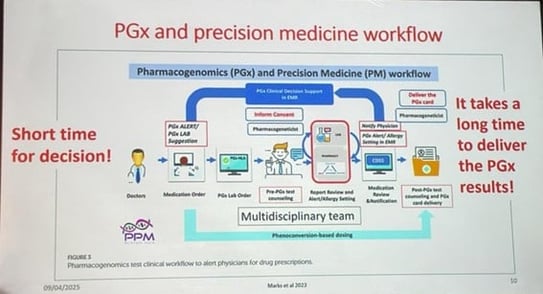
Référence : Marks et al. Updates in SJS/TEN: collaboration, innovation, and community. Front. Med., 10 October 2023.Sec. Dermatology.Volume 10 - 2023 https://doi.org/10.3389/fmed.2023.1213889
Médicaments ayant des implications génétiques
Exemple de l’azathioprine : un déficit héréditaire en thiopurine méthyltransférase (TPMT) peut induire une toxicité sévère ; les tests génétiques sont utiles, mais ne détectent pas tous les cas → une surveillance clinique étroite est nécessaire.
Réactions cutanées sévères (SCAR)
Exemples : SJS/NET.
Mortalité élevée (jusqu'à 50 % chez les adultes).
Associés à plus de 80 % à des médicaments tels que l’allopurinol, les anticonvulsivants aromatiques, les antibiotiques sulfamidés, les AINS, les antirétroviraux.
Mécanisme physiopathologique
Réaction immunitaire de type IV médiée par les lymphocytes T cytotoxiques.
Facteurs de risque : allèles des gènes HLA, troubles du métabolisme des médicaments (par exemple, CYP2C9), infections virales, interactions médicamenteuses.
Variabilité parmi la population
Les allèles des gènes HLA à risque varient en fonction des origines ethniques (par exemple, HLA-B15:02 chez les Asiatiques pour la carbamazépine, HLA-B57:01 chez les Européens pour l’abacavir).
Pas d’approche universelle → nécessite une adaptation locale.
Cas cliniques et tests
Exemple d’un patient souffrant d’une dépression majeure face à laquelle plusieurs médicaments ont été inefficaces → amélioration après le test de PGx.
Tests chez l’enfant (Toronto) : jusqu'à 80 % de variants exploitables après séquençage génomique.
Mise en œuvre effective
Essais réussis en psychiatrie, oncologie, cardiologie.
Remboursement dans certains pays européens, mais utilisation clinique encore limitée.
La pharmacogénétique permet une médecine personnalisée plus efficace et plus sûre.
Une mise en œuvre clinique efficace nécessite une formation médicale continue, des ressources technologiques, une validation scientifique et une adaptation à la variabilité génétique parmi la population.
En dermatologie, les SCAR représentent une application critique à fort impact clinique et préventif.
L’avenir de la médecine personnalisée comprend des tests préventifs intégrés dans les dossiers médicaux partagés, afin d’établir des listes de risques personnalisées pour chaque patient.
Références :
Cohn I, Manshaei R, Liston E, et al. Assessment of the Implementation of Pharmacogenomic Testing in a Pediatric Tertiary Care Setting. JAMA Network Open, 2021 ;4(5) :e2110446
DOI : 10.1001/jamanetworkopen.2021.10446Europe PMC+3
Barker, C.I.S., Groeneweg, G., Maitland-van der Zee, A.H., Rieder, M.J., Hawcutt, D.B., Hubbard, T.J., Swen, J.J., & Carleton, B.C. (2021). Pharmacogenomic testing in paediatrics: Clinical implementation strategies. British Journal of Clinical Pharmacology, 88(10), 4297–4310
Intervenante : Maria Cecilia Rivitti Machado (Brésil)
L’hidradénite suppurée (HS) est une maladie inflammatoire chronique et récurrente du follicule pileux, et non des glandes sudoripares comme on le pensait auparavant. Cette affection se manifeste typiquement par des nodules, des abcès et des tunnels (voies fistuleuses), principalement dans les zones intertrigineuses. Malgré son poids clinique et psychosocial important, elle reste sous-diagnostiquée, en particulier chez l’enfant et l’adolescent, où son incidence semble augmenter.
Maladie inflammatoire chronique et évolutive du follicule pileux.
Elle se caractérise par la présence de nodules inflammatoires douloureux, d’abcès et de tunnels dans des localisations typiques telles que les aisselles, l’aine, les fesses et la région sous-mammaire.
Les lésions réapparaissent ≥ 2 à 3 fois au cours d’une période de six mois.
Doubles comédons et nodules dans les deux aisselles :
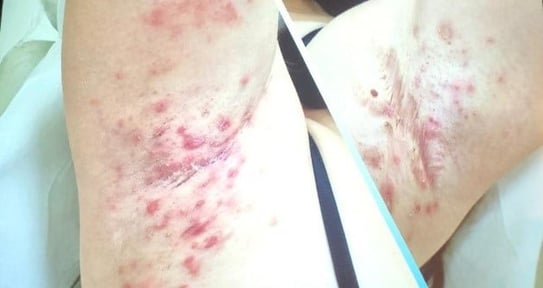
Cicatrices retractiles et tunnels dans les aisselles :
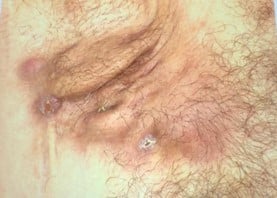
L’HS n’est pas une maladie rare, bien que sa prévalence varie en fonction de la région et de la population étudiée.
Prévalence plus élevée chez les adolescents et les jeunes adultes (10-40 ans).
Incidence élevée chez les adolescents d’origine africaine aux États-Unis et dans les populations du Brésil et de la Corée.
Une augmentation des cas graves est observée dans la population pédiatrique.
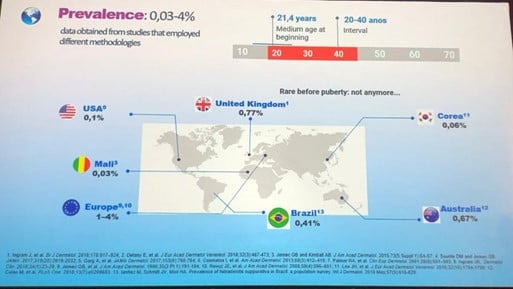

Le diagnostic est souvent tardif (> 12 ans), malgré des antécédents familiaux dans un tiers des cas.
Les patients consultent souvent plusieurs médecins avant que le bon diagnostic ne soit posé.
Présence de nodules fermes et enflammés (< 1 cm), souvent difficiles à reconnaître dans les premiers stades.
Abcès fluctuants et douloureux, parfois confondus avec des furoncles.
Tunnels (fistules dermiques ou sous-cutanées) qui peuvent être multiples, drainants ou secs, et comporter plusieurs orifices.
Lésions résiduelles : cicatrices atrophiques et comédons doubles.
Répartition anatomique typique : aisselles, aine, région fessière, région sous-mammaire.
Il est important de distinguer l’HS de la folliculite superficielle : cette dernière ne laisse pas de cicatrices atrophiques ni de comédons caractéristiques.
Dans les cas avancés, l’HS peut coexister avec une cellulite disséquante du cuir chevelu.
L’HS est une maladie évolutive : avec le temps, les lésions s’étendent et les dommages tissulaires s’accumulent.
La douleur est une caractéristique essentielle, tout comme un prurit occasionnel.
Une progression a été documentée chez deux tiers des patients après quatre ans de suivi.
L’impact n'est pas seulement physique : l’HS nuit significativement à la qualité de vie, à la productivité et aux relations interpersonnelles.
Importance d’un diagnostic précoce.
Il existe une « fenêtre d’opportunité » pendant laquelle un diagnostic et un traitement précoces peuvent limiter les dommages progressifs.
L’échographie cutanée peut être un outil utile pour améliorer la précision du diagnostic.
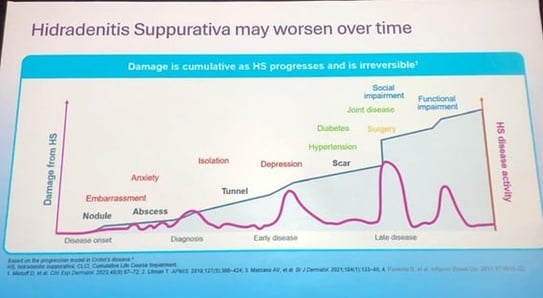
L’hidradénite suppurée est une maladie inflammatoire folliculaire grave et sous-diagnostiquée qui peut débuter à l’adolescence et évoluer rapidement si elle n’est pas détectée à temps. Le diagnostic clinique doit tenir compte de la morphologie des lésions, de leur répartition et de leur récurrence. Compte tenu de son impact physique et psychosocial cumulé, il est essentiel d’accroître la sensibilisation médicale, en particulier dans le domaine de la dermatologie pédiatrique, et d’assurer un suivi et un traitement adaptés dès les premiers stades de la maladie.
Intervenante : Dr Virginia Ruth Lopez Gamboa (Argentine)
L’hidradénite suppurée (HS) est une maladie inflammatoire chronique, récurrente et évolutive du follicule pileux, d’origine auto-inflammatoire, qui a un impact physique et psychosocial important. Il est essentiel de comprendre sa pathogenèse pour améliorer les stratégies diagnostiques et thérapeutiques, en particulier dans les formes précoces de la maladie, y compris chez l’enfant et l’adolescent.
Aspects fondamentaux de la pathogenèse de l’HS
L’HS n’est pas une infection. Elle n’est pas due à un manque d’hygiène et n’est pas déterminée par les origines ethniques.
Il s’agit d’une maladie auto-inflammatoire systémique complexe qui s’accompagne d’une dysrégulation immunitaire et d’une altération du devenir des cellules souches.
1. Théorie génétique
- Héritage complexe, aspect génétique dans 50 à 70 % des cas (principalement chez les femmes).
- Quelques mutations détectées :
- gènes de la gamma-sécrétase (voie NOTCH).
- Polymorphismes des récepteurs du TNF, de l’IL-1 et de l’IL-6.
- SOX9, facteur de transcription dans les cellules souches du follicule pileux, qui joue un rôle clé :
2. Théorie immunocellulaire
- Elle fait entrer en jeu des cellules telles que...
- Les cellules dendritiques, les lymphocytes Th1 et Th17, les neutrophiles et les plasmocytes.
- Une sécrétion excessive de cytokines pro-inflammatoires.
- Rôle des fibroblastes et des kératinocytes dans les phases chroniques : fibrose et cicatrisation aberrante.
- Ces mécanismes sont la cible des biothérapies actuellement approuvées.
3. Théorie hormonale
- L’inactivation incomplète du chromosome X chez les femmes est proposée comme cause du dysfonctionnement immunitaire.
- Dans ce contexte, le SOX9 régulé par les androgènes est modifié.
- L’adiposité augmente la conversion des androgènes en œstrogènes, modulant ainsi l’inflammation.
- Cela explique l’utilisation de médicaments tels que la spironolactone, le finastéride ou la metformine dans certains cas.
D’après le modèle traditionnel, ce processus est initié par le bouchon folliculaire.
Les données actuelles semblent montrer que l’obstruction est précédée par une inflammation dermique, ce qui crée un cercle vicieux.
Le processus se déroule ainsi : inflammation → bouchon → rupture → inflammation supplémentaire → formation de tunnels et de cicatrices.
L’HS est une maladie multifactorielle dont les mécanismes génétiques, immunologiques et hormonaux sont liés entre eux.
L’identification précoce des formes légères, en particulier chez l’enfant et l’adolescent, peut prévenir la progression et les séquelles permanentes.
SOX9 semble être une molécule centrale dans la pathogenèse.
Il est essentiel de personnaliser l’approche thérapeutique en tenant compte des facteurs déclencheurs et du stade clinique.
Le mécanisme de déclenchement principal reste inconnu et des recherches cliniques et translationnelles supplémentaires sont nécessaires.
Intervenante : Dr Ximena Wortsman (Chili)
L’hidradénite suppurée est une maladie inflammatoire chronique, dévastatrice et sous-diagnostiquée qui touche les follicules pileux dans les zones intertrigineuses. Par le passé, elle était considérée comme une maladie des glandes apocrines, mais des preuves récentes ont montré que son origine est liée à une perturbation folliculaire. L’échographie cutanée est devenue un outil de diagnostic essentiel pour la détection précoce de cette maladie, l’évaluation de son activité, l’orientation du traitement et la planification chirurgicale.
1. Avantages de l’échographie cutanée à haute fréquence
Elle permet une visualisation détaillée des couches de la peau, des follicules pileux, des glandes et des trajets fistuleux.
La résolution spatiale axiale est meilleure que celle du scanner ou de l’IRM pour les structures cutanées.
Elle détecte des altérations qui ne sont pas cliniquement visibles, ce qui permet un diagnostic plus précoce.
2. Nouvelles découvertes concernant la physiopathologie de l’HS
La maladie prend naissance dans les follicules pileux et non dans les glandes apocrines.
La rupture folliculaire contribue à la formation d’épanchements de liquide et de tunnels inflammatoires.
Des fragments de kératine et de tiges de cheveux ont été observés dans ces tunnels, ce qui est associé à une sévérité supérieure.
3. Protocole d’échographie et critères de diagnostic
Il existe des protocoles standardisés pour différentes régions anatomiques.
Les critères échographiques comprennent les structures kystiques, les épanchements, les trajets fistuleux et les changements d’échogénicité.
La classification échographique a été mise à jour pour inclure les sous-stades (3A et 3D) et le nombre de régions touchées.
4. Valeur de l’échographie en tant qu’outil de stadification et biomarqueur
Utile pour déterminer avec précision le degré d’inflammation active.
Il permet de différencier l’HS des affections apparentées (par exemple, les abcès ou les folliculites récurrentes).
Dans plus de 80 % des cas chez l’adulte (et 90 % chez l’enfant), l’utilisation de l’échographie modifie l’approche thérapeutique.
5. Suivi et évaluation de la réponse au traitement
Cet examen permet d’évaluer par doppler les changements d’échogénicité, l’affaissement du tunnel et la diminution de la vascularisation après le traitement.
Utile pour vérifier l’efficacité des biothérapies, des antibiotiques et de la photothérapie dynamique.
6. Planification chirurgicale et actes guidés par échographie
Amélioration de la délimitation des marges chirurgicales, ce qui peut réduire les récidives.
L’échographie guide les infiltrations intralésionnelles de corticoïdes, ce qui garantit la précision et évite les effets indésirables.
7. Validation internationale de l’utilisation de l’échographie dans le contexte de l’HS
Les récentes directives chiliennes et le consensus international valident l’utilisation de l’échographie dans le cadre de l’algorithme diagnostique et thérapeutique face à l’HS.
Un accord de plus de 95 % a été obtenu sur les éléments évalués (critères de diagnostic, stadification, surveillance, actes guidés et utilité pour la recherche).
L’échographie cutanée à haute fréquence est un outil validé, reproductible et très efficace pour le diagnostic, la stadification, le suivi thérapeutique et la planification des actes et interventions chez les patients atteints d’hidradénite suppurée. Son utilisation devrait devenir standard, notamment en raison de sa capacité à détecter la maladie à un stade précoce, à guider les décisions cliniques et à optimiser la prise en charge pluridisciplinaire.
Intervenante : Dr Jacek Szepietowski (Pologne)
L’hidradénite suppurée (HS) est une maladie inflammatoire chronique de la peau caractérisée par des lésions douloureuses, récurrentes et handicapantes qui touchent principalement les zones intertrigineuses. Malgré un tableau clinique bien connu, le poids subjectif et psychosocial associé à la maladie est souvent sous-estimé. Cette présentation abordait les conséquences émotionnelles, sociales et psychologiques de l’HS, en particulier chez l’enfant et l’adolescent, en soulignant la nécessité d’une approche interdisciplinaire pour améliorer la qualité de vie des patients.
L’HS se manifeste non seulement par des lésions cutanées visibles, mais aussi par des symptômes subjectifs tels que des douleurs intenses.
La douleur est directement corrélée à la gravité clinique selon les échelles Hurley et IHS4.
Plus de 80 % des patients font état de douleurs importantes.
L’HS est perçue par les patients comme une maladie « misérable », « insupportable », qui détruit le bien-être physique et émotionnel.
L’impact sur la qualité de vie est profond, parce que cette maladie nuit à la santé physique et mentale, à la vie sociale et à l’estime de soi.
Il existe de nombreux outils validés pour évaluer la qualité de vie dans le cadre de l’HS, mais nombre d’entre eux ont été validés uniquement chez l’adulte.
La qualité de vie diminue proportionnellement selon le nombre de zones touchées et la gravité du stade clinique.
Des études limitées portant sur des adolescents atteints d’HS ont montré une prévalence plus élevée de l’anxiété, de la dépression et de l’alexithymie (difficulté à identifier et à exprimer ses émotions).
Des problèmes d’autodestruction passive, de démotivation et de consommation problématique de substances ont également été identifiés.
L’HS entraîne une stigmatisation sociale marquée, comme avec d’autres dermatoses visibles telles que la dermatite atopique ou l’alopécie.
Cette stigmatisation nuit à l’intégration sociale, aux relations interpersonnelles et à la perception de soi.
L’HS a un impact significatif sur la sexualité, en particulier chez les adolescents qui commencent leur vie sexuelle.
Des niveaux élevés d’insatisfaction à l’égard de la vie sexuelle et des difficultés à établir des relations intimes ont été rapportés.
Il existe une forte corrélation entre le manque de satisfaction à l’égard de la vie, l’anxiété, la dépression et la perception de la prise en charge de la maladie.
Une bonne relation médecin-patient basée sur la confiance peut améliorer considérablement les résultats thérapeutiques.
L’intervenant a souligné la nécessité de traitements efficaces et personnalisés.
Il recommande une approche interdisciplinaire, faisant appel à des dermatologues, des rhumatologues, des psychologues et des psychiatres.
Le soutien psychologique est essentiel pour améliorer l’adaptation à la maladie et la qualité de vie.
L’HS est bien plus qu’une maladie de peau : elle représente un poids physique, émotionnel et social important. Les patients doivent être entendus non seulement concernant leurs symptômes cliniques, mais aussi concernant leur vécu. La prise en charge globale doit comprendre la gestion clinique, le soutien psychosocial et l’amélioration de l’estime de soi et de la capacité à fonctionner. En tant que médecins, notre rôle doit aller au-delà du traitement dermatologique et englober une vision holistique qui accompagne les patients de la souffrance à la stabilisation et au bien-être.
Intervenante : Dr Renata Magalhaes (Brésil)
L’hidradénite suppurée (HS) est une maladie inflammatoire chronique et invalidante dont la manifestation chez l’enfant et l’adolescent représente un défi diagnostique et thérapeutique. Bien que traditionnellement considérée comme une maladie de l’adulte jeune, des cas d’apparition précoce sont de plus en plus souvent reconnus, même avant 12 ans, ce qui souligne la nécessité d’approches thérapeutiques spécifiques et opportunes dans cette tranche d’âge.
Dans un centre de référence comptant plus de 200 patients atteints d’HS, 15 % ont signalé des symptômes avant l’âge de 12 ans, et 15 % entre 12 et 18 ans.
Chez l’adolescent, la maladie tend à présenter une évolution plus agressive et un impact important sur la qualité de vie.
Les cas cliniques ont montré une apparition dans l’enfance et une progression sévère, dont un patient qui est passé de lésions légères à une maladie sévère en l’espace de sept ans.
L’identification de ces comorbidités permet une intervention plus complète et plus précoce.
Un diagnostic et un traitement précoces sont essentiels pour infléchir l’évolution de la maladie.
Le fait de retarder le début des biothérapies peut réduire significativement le taux de réponse.
Une étude italienne a montré qu’un retard de plus de 10 ans est associé à un risque deux fois plus élevé d’échec du traitement.
Utile dans les stades précoces ou dans les cas de maladie légère.
Options : clindamycine topique, résorcine (bien qu’elle ne soit pas officiellement approuvée), supplémentation en zinc (utilisation empirique).
En première ligne dans les cas modérés à sévères.
Ils comprennent la céfalexine, la doxycycline (à partir de 8 ans), la clindamycine et la rifampicine (avec prudence).
Principalement envisagés dans les cas d’acné sévère coexistante.
L’isotrétinoïne est utile, malgré des résultats variables ; l’acitrétine peut être envisagée dans des cas bien précis.
Données limitées, mais peut être envisagée dans les cas présentant des signes d’hyperandrogénie ou de résistance à l’insuline.
Cette option est celle pour laquelle il existe le plus de données probantes chez les patients âgés de ≥ 12 ans.
Principaux agents utilisés :
La chirurgie peut être envisagée chez certains patients, idéalement après stabilisation par un traitement médical.
Exemple : patient de 15 ans souffrant d’une atteinte de l’aisselle droite, traitée par biothérapie, avant une exérèse chirurgicale ayant permis de bons résultats.
Les traitements au laser et à la lumière (laser CO₂, Nd:YAG) peuvent être utiles en complément.
Prise en charge pluridisciplinaire indispensable : dermatologie, rhumatologie, psychologie, nutrition.
Le traitement de l’hidradénite suppurée chez l’enfant et l’adolescent représente une occasion unique d’infléchir l’évolution de la maladie et d’améliorer le pronostic à long terme. Le dépistage précoce, la prise en charge globale des comorbidités et l’instauration en temps utile de traitements efficaces, y compris les biothérapies, sont les piliers fondamentaux de l’approche actuelle. Bien que les données soient encore limitées, en particulier chez les enfants de moins de 12 ans, les nouvelles directives commencent à intégrer des recommandations spécifiques pour cette tranche d’âge, ce qui constitue une avancée importante dans la personnalisation du traitement.
Intervenante : Dr Mario Chaves, Chirurgien (Brésil)
L’hidradénite suppurée (HS) est une maladie inflammatoire chronique de l’unité pilo-sébacée, qui est souvent sous-diagnostiquée et retarde le traitement adapté. Chez l’enfant et l’adolescent, un retard dans l’approche chirurgicale compromet le pronostic et permet une évolution vers des formes plus sévères. Cette intervention abordait l’importance d’une intervention chirurgicale opportune, les options thérapeutiques disponibles et le rôle des technologies complémentaires dans l’optimisation des résultats.
La chirurgie doit être envisagée à un stade précoce, même chez l’adolescent, afin de prévenir l’évolution vers des stades avancés (Hurley III).
La chirurgie doit être décidée en fonction de l’étendue, de la localisation, de la gravité et des comorbidités du patient.
Il est essentiel de ne pas interférer avec le calendrier scolaire des enfants et des adolescents.
Élimination des masses inflammatoires, des débris kératosiques et du tissu de granulation chronique.
Contrôle du processus infectieux et réduction du risque de récidive.
Incision et drainage des abcès.
Deroofing et unroofing (techniques de recouvrement et ablation du « toit » des tunnels).
Excision large selon des marges latérales de 1 à 2 cm et couverture par des lambeaux ou des greffes.
Fermeture primaire dans la mesure du possible, en particulier pour les lésions localisées.
Hémorragie, infection, cicatrice hypertrophique, rétraction, déhiscence et récidive.
Laser CO₂ : utile pour l’ablation ou l’exérèse de lésions chroniques, permet une lésion thermique minimale et une meilleure visualisation. Favorise la cicatrisation en deuxième intention.
Pression négative (vide) : indiquée en cas d’incision chirurgicale à haut risque, réduit le risque d’infection et de déhiscence.
Exemples cliniques pédiatriques...
Cas d’adolescents présentant des lésions axillaires, inguinales et périnéales traitées par excision large et reconstruction par lambeaux V-Y ou fermeture primaire.
Résultats postopératoires fonctionnels et esthétiques satisfaisants.
La chirurgie représente un outil fondamental dans la prise en charge de l’hidradénite suppurée, en particulier chez les jeunes patients. Une indication précoce peut ralentir la progression de la maladie, réduire la charge inflammatoire et améliorer la qualité de vie. Il est essentiel d’adopter une approche pluridisciplinaire, en tenant compte de la santé mentale, du soutien psychologique et du contexte social de l’enfant ou adolescent. L’utilisation de technologies telles que le laser CO₂ et la thérapie par pression négative permet d’optimiser les résultats chirurgicaux et de réduire les complications. Un traitement chirurgical précoce, bien planifié et personnalisé peut transformer radicalement le pronostic des patients atteints d’HS.
Session animée par : Dr Catherine C. McCuaig (Canada)
Session co-animée par : Dr Ana María Saénz (Venezuela) et Dr Josaine Sanjinés (Bolivie)
Intervenante : Dr Josaine Sanjinés (Bolivie)
L’intervenante a passé en revue la physiopathologie, l’épidémiologie, les manifestations cliniques et les options thérapeutiques actuelles face au molluscum contagiosum et aux verrues dues au papillomavirus humain (HPV), deux infections virales cutanées courantes chez l’enfant. Malgré une résolution habituellement spontanée, la prise en charge de ces infections peut s’avérer difficile, en particulier dans les cas multiples, symptomatiques ou localisés dans des zones visibles.
Dû à un poxvirus spécifique à l’homme.
Il se transmet par contact direct avec la peau infectée, par auto-inoculation ou par des fomites.
La transmission via l’eau n’a pas été démontrée, bien que le MC ait été associé à des activités telles que la natation.
Prévalence chez les enfants américains : environ 62 %.
Plus fréquents entre 0 et 16 ans.
Période d'incubation : 2 semaines à 6 mois.
Lésions nacrées, de couleur chair, ombiliquées, de 1 à 10 mm.
Phénomène de Kœbner dans les zones ayant subi un traumatisme.
Dans le cas de la dermatite atopique, on peut observer une hypersensibilité et une dissémination importante.
Immunosuppression : VIH, greffes, chimiothérapie (lésions plus étendues et réfractaires).
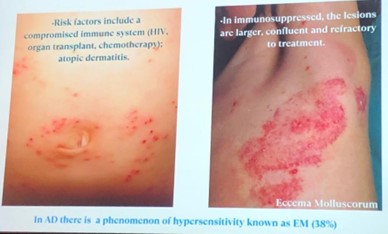
Observation des lésions non symptomatiques ou éparses.
Le signe d’une inflammation périlésionnelle peut indiquer une résolution imminente.
Références :
Keam SJ. Berdazimer Topical Gel, 10.3%: First Approval. Drugs. 2024 Mar;84(3):363-368. doi: 10.1007/s40265-024-02012-9. PMID: 38409574.
Paller AS, Green LJ, Silverberg N, Stripling S, Cartwright M, Enloe C, Wells N, Kowalewski EK, Maeda-Chubachi T. Berdazimer gel for molluscum contagiosum in patients with atopic dermatitis. Pediatr Dermatol. 2024 May-Jun;41(3):438-444. doi: 10.1111/pde.15575. Epub 2024 Feb 27. PMID: 38413239.
Verrues communes : lésions hyperkératosiques sur le visage et les extrémités.
Verrues plantaires : surface lisse et points sombres (capillaires thrombosés).
Condylomes acuminés : dans la région génitale et périanale.
Verrues buccales : sur les lèvres, les gencives, le palais ou la langue.
Le molluscum contagiosum et les verrues virales sont des infections courantes, bénignes et de résolution spontanée chez l’enfant. Le choix du traitement doit être personnalisé, en tenant compte de l’âge du patient, de la localisation, des symptômes, du nombre de lésions et du statut immunitaire. Il existe plusieurs options approuvées, mais une simple observation est également possible dans de nombreux cas. La communication avec les parents et un suivi adapté sont essentiels pour une prise en charge réussie et sûre.
Intervenante : Dr Catherine C. McCuaig (Canada)
Ces dernières années, le traitement topique des maladies inflammatoires de la peau telles que la dermatite atopique et le psoriasis a considérablement évolué. De nouvelles molécules aux mécanismes d’action innovants ont été approuvées, notamment des inhibiteurs de la phosphodiestérase-4 (PDE4), des inhibiteurs de JAK (janus kinase) et des agonistes du récepteur des hydrocarbures aryliques (AhR). Ces traitements promettent d’améliorer considérablement la prise en charge clinique, en particulier chez l’enfant. Toutefois, le coût élevé et la disponibilité limitée restent des obstacles majeurs.
1. Inhibiteurs de la PDE4
2. Inhibiteurs topiques de JAK
Effets indésirables : irritation locale (< 1 %), quelques réactions folliculaires de type KP.
3. Modulateurs du récepteur des hydrocarbures aryliques (AhR)
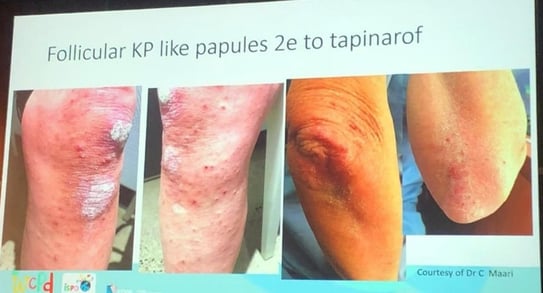
Considérations cliniques et comparatives
De nouveaux traitements topiques offrent des alternatives précieuses et efficaces pour la prise en charge de la dermatite atopique et du psoriasis, y compris chez l’enfant et l’adolescent.
Défis actuels : manque d’études comparatives directes, preuves limitées concernant les associations thérapeutiques et coût élevé. L’avenir s’annonce prometteur grâce à des molécules innovantes qui pourraient redéfinir le traitement topique des maladies inflammatoires chroniques en dermatologie pédiatrique.
Intervenante : Dr Ana María Saénz (Venezuela)
L’épidermolyse bulleuse (EB) désigne un groupe de maladies génétiques rares caractérisées par une fragilité extrême de la peau, provoquant des cloques et des plaies lors de traumatismes minimes. La prise en charge de cette pathologie représente un défi majeur, en particulier dans les pays aux ressources limitées, car elle nécessite une approche pluridisciplinaire. Au cours de ce congrès de dermatologie pédiatrique, de nouvelles avancées en matière de traitements topiques innovants ont été présentées, des thérapies géniques aux solutions accessibles d’origine naturelle.
Le traitement topique de l’EB a considérablement progressé, offrant de nouveaux espoirs, notamment avec l’approbation de la première thérapie génique in vivo. Toutefois, la plupart de ces traitements sont inaccessibles dans de nombreuses régions en raison de leur coût élevé. Les alternatives telles que l’extrait d’écorce de bouleau représentent une option efficace et possible dans des contextes où les ressources sont limitées. Il est essentiel de continuer à promouvoir la recherche, la collaboration internationale et un soutien complet aux patients afin de parvenir à une approche plus équitable et plus efficace face à cette maladie complexe.
Intervenante : Dr Irene Lara Corrales (Canada)
Cette présentation portait sur les traitements topiques approuvés au cours des cinq dernières années pour la prise en charge de l’acné vulgaire et de l’hidradénite suppurée (HS). Ces pathologies partagent des mécanismes physiopathologiques similaires : principalement l’occlusion folliculaire et l’inflammation secondaire, ce qui justifie leur analyse conjointe. Bien que de nombreux traitements systémiques soient disponibles, l’optimisation des options topiques est essentielle, en particulier pour les patients atteints d’une forme légère de ces maladies ou dans le cadre de stratégies d’association ou d’entretien.
Les données démontrent que ce traitement ne génère pas d’exposition systémique significative, contrairement à sa forme orale.
Deux essais de phase III ont confirmé son efficacité pour ce qui est de réduire les lésions inflammatoires et non inflammatoires, avec une bonne tolérance et innocuité après 52 semaines.
Elle figure dans les nouvelles directives thérapeutiques et bénéficie d’une recommandation élevée et d’un niveau de certitude modéré.
Premier anti-androgène topique approuvé face à l’acné ; bloque l’action de la dihydrotestostérone (DHT) au niveau des récepteurs des androgènes dans les sébocytes.
Des études menées chez des adolescents et des adultes ont montré son efficacité et un profil de tolérance favorable, bien que son utilisation puisse être limitée par son coût élevé.
Recommandée dans certaines conditions, selon un niveau de preuve élevé dans les nouvelles directives.
Polythérapie topique qui améliore la tolérance du peroxyde de benzoyle.
Efficace face à l’acné modérée à sévère, comparable ou supérieure à d’autres associations thérapeutiques.
Fortement recommandé selon une certitude modérée dans les directives.
Premier traitement topique à trois composants approuvé face à l’acné.
Des études menées chez des adultes et des adolescents ont montré une supériorité par rapport aux formes et aux associations doubles, avec une bonne tolérance.
Elle ne figure pas encore dans les directives en raison de son approbation récente.
Il n’existe actuellement aucun traitement topique approuvé spécifiquement face à l’HS, mais des essais sont en cours...
Des directives américaines pour la prise en charge médicale de l’HS, comprenant des recommandations spécifiques pour l’enfant et l’adolescent, ont été récemment publiées.
Dans le domaine de l’acné, la mise au point de nouvelles formulations topiques a permis d’élargir l’arsenal thérapeutique grâce à des produits plus précis, efficaces et sûrs.
Bien que le coût et l’observance restent des défis cliniques, ces progrès permettent une stratification personnalisée du traitement.
Face à l’hidradénite suppurée, il n’existe pas encore de traitement topique appuyé par des données solides, même si les études actuelles sont prometteuses.
Il est essentiel de surveiller les approbations futures et les résultats des essais cliniques en cours.
Intervenante : Dr Felipe Enrique Valderrama(Pérou)
La pelade et le vitiligo sont des maladies inflammatoires chroniques auto-immunes qui touchent fréquemment les enfants et les adolescents. Bien que distinctes sur le plan clinique, ces deux affections partagent des mécanismes pathogènes communs et des difficultés thérapeutiques similaires. Cette présentation abordait les options thérapeutiques topiques les plus pertinentes chez les enfants, en mettant l’accent sur les inhibiteurs de JAK en tant que nouvelle alternative prometteuse.
Maladie auto-immune avec prédisposition génétique.
Elle peut avoir une évolution légère, modérée ou sévère (totale, universelle, diffuse).
Diagnostic clinique complété par une trichoscopie : points noirs, cheveux en point d’exclamation, cheveux cassés.
Évaluation de la gravité à l’aide de l’échelle SALT.
Corticoïdes topiques et intralésionnels : traitement de première ligne, sans danger pour les enfants.
Analogues des prostaglandines : (bimatoprost, latanoprost) pour le cuir chevelu et les cils, bien que les données probantes soient limitées.
Inhibiteurs topiques de JAK (tofacitinib, ruxolitinib) : nouvelle option en cas d’échec des corticoïdes.
Minoxidil topique : adjuvant utile.
Autres modalités...
Dans les cas étendus (> 50 %) : traitement systémique par corticoïdes ou immunomodulateurs (méthotrexate, entre autres).
Fillette de 10 ans présentant une pelade étendue, réfractaire aux corticoïdes et au méthotrexate.
Traitement réussi avec le tofacitinib 5 mg deux fois par jour : amélioration de 60-70 % du score SALT en quelques mois.
Fréquence accrue du vitiligo segmentaire.
Forte association avec la dermatite atopique et les antécédents familiaux de maladies auto-immunes.
Classification : segmentaire, non segmentaire, mixte ou hors catégorie.
Plusieurs mécanismes : prédisposition génétique, auto-immunité, stress oxydatif et théories neurogéniques.
Théorie convergente : réunion des hypothèses expliquant la perte de viabilité des mélanocytes.
Indiqués lorsque < 10 % de la surface corporelle est touchée.
Corticoïdes topiques : mométasone, fluocinolone, utilisés de manière intermittente pour réduire les effets indésirables locaux.
Inhibiteurs de la calcineurine : tacrolimus, pimécrolimus, en particulier sur le visage et les zones sensibles.
Inhibiteurs topiques de JAK : ruxolitinib crème approuvé par la FDA (utilisation chez l’enfant encore à l’étude).
Patiente pédiatrique atteinte de vitiligo sur la lèvre supérieure, traitée par ruxolitinib topique et photothérapie, avec une repigmentation de 80 % en 2 mois.
Dans les cas étendus : photothérapie UVB à bande étroite - modalité la plus couramment utilisée.
Chirurgie (greffes d’épiderme par bulles de succion) : option pour les zones résistantes (lèvres, visage).
La pelade et le vitiligo partagent des mécanismes pathogènes tels que l’auto-immunité et le stress oxydatif.
Le choix du traitement doit reposer sur l’évaluation clinique et la gravité.
Les corticoïdes topiques et les inhibiteurs de la calcineurine restent les piliers du traitement initial.
Les inhibiteurs topiques de JAK, tels que le tofacitinib et le ruxolitinib, semblent être des alternatives prometteuses de par leur efficacité et leur profil de tolérance chez l’enfant.
L’association avec la photothérapie peut améliorer les résultats thérapeutiques.
Intervenante : Fernanda Bellodi Schmidt (États-Unis)
Bien que les traitements topiques soient généralement considérés comme sûrs, en particulier en pédiatrie, une mauvaise utilisation peut avoir des conséquences graves. Cette présentation a mis en évidence les risques de toxicité aiguë associés aux médicaments topiques fréquemment utilisés en dermatologie pédiatrique. Des cas cliniques réels ont montré comment des facteurs tels que l’âge, l’état de la barrière cutanée, la posologie et la technique d’application peuvent contribuer à l’apparition d’effets indésirables systémiques significatifs.
La peau des enfants présente des différences importantes par rapport à celle des adultes...
La couche cornée est immature jusqu’à l’âge de 2 à 5 ans.
L’épiderme est plus fin et contient moins de lipides.
Le rapport entre la surface corporelle et le poids est plus élevé.
Ces caractéristiques favorisent l’absorption percutanée et le risque de toxicité.
1. Anesthésiques topiques (lidocaïne/prilocaïne - EMLA®, lidocaïne - LMX®)
2. Alcools et antiseptiques
3. Peroxyde d’hydrogène
4. DEET (diéthyl-méta-toluamide, insecticide topique)
5. Acide salicylique
Intervenante : Dr Lisa Weibel (Suisse)
L’intervenante a présenté les avancées récentes en dermatologie pédiatrique, en se concentrant exclusivement sur les observations cliniques, sans évoquer les aspects thérapeutiques et génétiques. Cette présentation portait sur une sélection de dix publications scientifiques mettant en évidence de nouvelles entités cliniques, des modèles phénotypiques inhabituels et des associations pertinentes ayant un impact en matière de diagnostic. Les résultats les plus importants sont décrits ci-dessous.
1- Nævus mélanocytaire congénital corymbiforme segmentaire
(Segmental corymbiform congenital melanocytic naevi)
2- Syndrome vasculaire orthostatique chez l’enfant
a. Lésions urticariformes accompagnées d’une érythrocyanose qui sont remplacées par des macules anémiques lorsque le patient est en position orthostatique.
b. Une étude canadienne a rapporté 42 cas ; prédominance chez les filles, association fréquente avec le TDAH (50 % des cas) et symptômes de dysautonomie (60 %) tels que l’intolérance à la position orthostatique. Des cas ont également été décrits chez des nourrissons.
c. Les bêta-bloquants et les antihistaminiques n’ont pas donné de bons résultats. L’évolution est bénigne, et une résolution spontanée est observée dans la plupart des cas après 3 à 4 ans.
3- Phototoxicité associée au voriconazole - phénotype de type xeroderma pigmentosum
a. Cas chez des patients immunodéprimés, y compris des enfants atteints d’un syndrome de Down traités par voriconazole.
b. Le voriconazole peut induire une phototoxicité, mais il a également été associé à un risque élevé de carcinome épidermoïde agressif et même de mélanome chez les enfants et les adultes.
c. Le phénotype cutané des patients est remarquablement similaire à celui observé chez les personnes atteintes d’un xeroderma pigmentosum (XP).
d. Il a été démontré que le médicament ne modifie pas directement l’expression des gènes impliqués dans la réparation de l’ADN (contrairement au XP), mais qu’il réduit la réparation en modifiant la densité de la chromatine, ce qui empêche le système de réparation d’accéder à l’ADN endommagé.
e. Cet effet indésirable du voriconazole peut être inversé par l’administration concomitante d’inhibiteurs de l’histone désacétylase, tels que l’acide valproïque, la ribostatine, entre autres.
Références :
AK Haylett, S Felton, DW Denning, LE Rhodes.Voriconazole‐induced photosensitivity: photobiological assessment of a case series of 12 patients British Journal of Dermatology, 2013
Alberdi Soto, M., Aguado Gil, L., Pretel Irazabal, M., Bonaut Iriarte, B., Irarrázabal Armendariz, I., Lera Imbuluzqueta, J. M., … Ivars, M. (2014). Accelerated photoaging induced by voriconazole treated with Q-switched Nd:YAG laser: Case report and review of the literature. Journal of Cosmetic and Laser Therapy, 16(6), 314–316. https://doi.org/10.3109/14764172.2014.957215
Miller DD, Cowen EW, Nguyen JC, McCalmont TH, Fox LP. Melanoma Associated With Long-term Voriconazole Therapy: A New Manifestation of Chronic Photosensitivity. Arch Dermatol. 2010;146(3):300–304. Doi:10.1001/archdermatol.2009.362DD Arch Dermatol 2010
CowenEW, Nguyen JC, Miller DD, et al.Chronic phototoxicity and aggressive squamous cell carcinoma of the skin in children and adults during treatment with voriconazole. J Am Acad Dermatol 2010;62:31–7.
4- À partir de combien de lésions considère-t-on qu’il y en a trop ? Seuils cliniques pour l’évaluation génétique.
a. Nous savons que certaines lésions cutanées, lorsqu’elles sont présentes en grand nombre, peuvent être associées à des maladies sous-jacentes. Or pour nombre de ces lésions, le seuil numérique qui devrait nous alerter n’est pas bien défini.
Nombre de lésions proposé pour suspecter une maladie systémique :
5- MiTES (Mid-facial Toddler Excoriation Syndrome)
a. Ulcères auto-infligés dans la région centro-faciale chez des enfants de moins d’un an, présentant des excoriations symétriques en forme de X.
b. Résolution spontanée (environ 5 ans), laissant des cicatrices atrophiques, à différencier de l’insensibilité congénitale à la douleur (ICD), dans laquelle le toucher est normal, ainsi que la pression et la température, mais aucune douleur n’est perçue.
c. Tous deux associés à des variantes du gène PRDM12, ils diffèrent par l’expansion des répétitions de polyalanine dans ce gène.
6- Leucoplasie linguale transitoire chez l’enfant
a. Plaque blanchâtre impossible à retirer sur le dos de la langue, qui s’arrête à la pointe de cette dernière.
b. Non associée à Candida ou à une pathologie systémique.
c. Résolution spontanée au début de l’alimentation solide.
Référence :
Lam JM, Schwieger-Briel A, Nguyen T, Torrelo A. Transient infantile lingual leukoplakia: An underrecognized cause of white tongues in infancy. Pediatr Dermatol. 2024 May-Jun;41(3):476-479. doi: 10.1111/pde.15576. Epub 2024 Feb 27. PMID: 38413200.
7- Nævus épidermique verruqueux de type Blaschko lié à PTEN
a. Patient présentant un nævus verruqueux linéaire, une macrocéphalie, un retard de développement (dysplasie corticale à l’IRM) et une cataracte. La biopsie a révélé un nævus sébacé, mais l’analyse génétique a montré une variante germinale du gène PTEN.
b. Diagnostic : syndrome hamartomateux lié à PTEN, prenant la forme d’un mosaïcisme. Il est possible de parler de nævus linéaire lié à PTEN ou de nævus linéaire de Cowden. La principale caractéristique de ce nævus est qu’il est très verruqueux, papillomateux et qu’il présente une composante hyperkératosique.
Il faut garder à l’esprit qu’un nævus épidermique linéaire verruqueux associé à une macrocéphalie peut présenter une mutation de PTEN et doit donc faire l’objet de contrôles et d’un suivi dans le cadre de protocoles de surveillance oncologique.
8- Nævus épidermique épidermolytique : pratiquer une biopsie ou non ?
a. Faible risque de transmission de l’ichtyose épidermolytique chez les parents présentant des nævus étendus.
b. Le conseil génétique est très compliqué dans ce contexte, car le risque de transmission varie énormément, de 0 % quand aucune cellule gonadique n'est touchée, à 50 % quand toutes les cellules gonadiques sont touchées chez l’un des parents.
Le conseil génétique est également difficile parce que les techniques actuelles d’investigation de l’atteinte des gonades ne sont pas réalisables (par exemple chez les femmes) ou ne permettent pas de déterminer de manière fiable le degré d’atteinte des gonades.
c. Il est recommandé de pratiquer une biopsie au niveau des lésions étendues afin d’évaluer le risque et d’envisager un conseil génétique.
9- Syndrome de la peau parcheminée
a. Durcissement de la peau depuis l’enfance, accompagné d’une hypertrichose et d’une atteinte des articulations (douleurs articulaires ou restriction des mouvements, en raison de l’atteinte des fascias et des articulations sous-jacentes).
b. Diagnostic clinique différentiel : sclérodermie localisée (avec atrophie annexielle) et le nævus conjonctival.
c. Le diagnostic nécessite des données cliniques et histologiques ainsi que des examens d’imagerie.
10- Comment prélever le meilleur échantillon de gale : sous la lumière de Wood
Traditionnellement, en dermoscopie polarisée, le signe caractéristique de la gale est le « signe delta », qui représente les parties antérieures de l’acarien Sarcoptes scabiei (tête et pattes avant). Cependant, cette méthode ne permet pas toujours de visualiser l’ensemble du corps de l’acarien.
En ajoutant la dermoscopie UV (réglée sur une lumière de 365 nm), les auteurs ont observé que le corps entier de l’acarien émettait une fluorescence brillante, qui prenait la forme d’une structure ovale ou sphérique. Cette découverte a été surnommée le « signe de la balle ». Cette technique améliore la visualisation de l’acarien en éliminant les interférences telles que les squames, ce qui permet une identification plus claire du parasite.
Référence :
Aslan Yürekli. A new sign with UV dermoscope in the diagnosis of scabies: Ball sign. Skin Res Technol. 2023;29:e13336
Ces résultats cliniques récents soulignent l’importance d’une observation dermatologique minutieuse, en particulier en pédiatrie. Plusieurs des schémas décrits ont un impact en matière de diagnostic, de pronostic et de génétique, et sont à prendre en compte dans la pratique clinique quotidienne. L’approche clinique doit être complétée, si nécessaire, par des examens histologiques et moléculaires afin de parvenir à un diagnostic précis et d’éclairer le suivi adapté de ces patients.
Intervenante : Lawrence Eichenfield (États-Unis)
Mise à jour thérapeutique en dermatologie pédiatrique : avancées récentes face à la dermatite atopique, au psoriasis et la pelade
Ces dernières années ont été marquées par des progrès remarquables dans le développement et l’autorisation de traitements dermatologiques chez l’enfant et l’adolescent, en particulier face aux maladies chroniques et inflammatoires telles que la dermatite atopique, le psoriasis et la pelade. Cette présentation passait en revue les résultats récents d’essais cliniques multicentriques et d’études d’extension qui ont élargi l’arsenal thérapeutique chez ces patients, en mettant en évidence les traitements topiques et systémiques et leur impact clinique au-delà de la gestion de la peau.
Traitements topiques non stéroïdiens
• Tapinarof : agoniste des récepteurs des hydrocarbures aryliques, autorisé aux États-Unis à partir de l’âge de 2 ans. Effet anti-inflammatoire, antioxydant et de régénération épithéliale. Résultats prometteurs dans les études en tant que traitement d’entretien, avec une rechute en moyenne 75 jours après l’élimination.
• Roflumilast : inhibiteur de la PDE4 autorisé sous forme de crème à 0,15 % à partir de l’âge de 6 ans. Efficacité plus modeste, mais excellente tolérance et utilisation proactive efficace (281 jours en moyenne sans récidive).
• Ruxolitinib topique : inhibiteur de JAK approuvé à partir de l’âge de 12 ans ; résultats similaires chez les enfants âgés de 2 à 12 ans. Efficacité élevée comparativement aux corticoïdes topiques, mais restrictions quant au pourcentage de la surface corporelle pouvant être traité.
Traitements systémiques
La dermatologie pédiatrique connaît actuellement une révolution thérapeutique, grâce à des avancées cliniques significatives reposant sur des collaborations internationales. De nouveaux agents topiques non stéroïdiens et des thérapies systémiques ciblées ont amélioré non seulement la prise en charge cutanée de maladies comme la DA et le psoriasis, mais aussi les comorbidités systémiques et la qualité de vie. L’intervenant a donc souligné l’importance de la formation continue des pédiatres et des professionnels de santé en ce qui concerne la nouvelle prise en charge de ces pathologies.
Intervenante : Dr Brigitte Dréno (France)
Cette présentation abordait les progrès réalisés quant à la compréhension du microbiome cutané et de son rôle clé dans l’homéostasie de la peau et dans les maladies inflammatoires, infectieuses et néoplasiques. L’intervenante a souligné l’équilibre dynamique entre les bactéries commensales et pathogènes, l’influence du micro-environnement cutané sur la virulence bactérienne et les progrès de la bactériothérapie en tant qu’approche thérapeutique émergente.
Toute perturbation chronique (comme les dommages causés par les UV) peut induire une dysbiose, et donc une perte de diversité bactérienne et une augmentation des profils de virulence chez des bactéries auparavant commensales.
Microvésicules extracellulaires bactériennes
Le microbiome cutané est un écosystème dynamique essentiel à l’homéostasie de la peau. Les bactéries commensales participent non seulement à la défense contre les pathogènes, mais modulent également l’inflammation, la cicatrisation et même la prévention du cancer de la peau. De nouvelles stratégies thérapeutiques (comme la bactériothérapie, l’utilisation de vésicules extracellulaires et la modulation du micro-environnement) ouvrent un champ prometteur en dermatologie, tant pour la prévention que pour le traitement des maladies inflammatoires et néoplasiques. La clé sera de préserver la diversité et l’équilibre du microbiome.
Référence :
Lee YB, Byun EJ, Kim HS. Potential Role of the Microbiome in Acne: A Comprehensive Review. J Clin Med. 2019 Jul 7;8(7):987. doi: 10.3390/jcm8070987. PMID: 31284694; PMCID: PMC6678709.
C. Cheung, C. Mias, U. Lancien, S. Corvec, V. Mengeaud, A. Khammari, H. Duplan, B. Dreno,
333 Different proinflammatory profiles of Cutibacterium acnes IA1 extracellular vesicles from healthy and acne skin: modulation by Myrtacine and Celastrol, Journal of Investigative Dermatology,Volume 144, Issue 12, Supplement,2024,Page S285
Cros MP, Mir-Pedrol J, Toloza L, et al. New insights into the role of Cutibacterium acnes-derived extracellular vesicles in inflammatory skin disorders. Sci Rep. 2023;13:16058. doi:10.1038/s41598-023-43354-w
Jin C, Lagoudas GK, Zhao C, Bullman S, Bhutkar A, Hu B, et al. Commensal microbiota promote lung cancer development via γδ T cells. Cell. 2019;176(5):998–1013.e16. doi:10.1016/j.cell.2018.12.040.
Intervenante : Dr Ilona Frieden (États-Unis)
Nouvelle classification ISSVA (2024)
Malformations capillaires : les sous-types mis en évidence
Malformation capillaire dite de la « tache de vin » : bien délimitée, saturée, souvent sur le visage, présentant parfois une composante réticulée.
Pertinence clinique de cette classification
Référence : https://vascern.eu/group/vascular-anomalies/clinical-decision-support-t…
Référence : Borst A. Targeted medical therapies for vascular anomalies. Hematology Am Soc Hematol Educ Program. 2024 Dec 6;2024(1):709-717. doi: 10.1182/hematology.2024000599. PMID: 39644074; PMCID: PMC11665586.
Référence :
Bradley, Flora et al. A retrospective multicenter cohort study of differences in clinical characteristics of Infantile Hemangiomas in preterm and term infants: Prematurity increases risk of permanent cutaneous sequelae. JAAD 2025, Volume 92, Issue 3, Pages 546-553. doi: 10.1016/j.jaad.2024.09.066
Échec du traitement par bêta-bloquants